Рассчитать количество раствора: Расчет объема раствора — онлайн калькулятор
Как рассчитать расход раствора для штукатурки стен — Механизированная штукатурка на vc.ru
{«id»:13956,»url»:»\/distributions\/13956\/click?bit=1&hash=218824c4468d1ad16ead721c4569ab95b5415e06001032a32c34f904cb106363″,»title»:»\u041a\u0430\u043a \u0440\u043e\u0434\u0438\u0442\u0435\u043b\u044e-\u0430\u0439\u0442\u0438\u0448\u043d\u0438\u043a\u0443 \u0438\u0437\u0431\u0430\u0432\u0438\u0442\u044c\u0441\u044f \u043e\u0442 \u043c\u0443\u043a \u0432\u044b\u0431\u043e\u0440\u0430: \u0441\u0435\u043c\u044c\u044f \u0438\u043b\u0438 \u0440\u0430\u0431\u043e\u0442\u0430″,»buttonText»:»\u0423\u0437\u043d\u0430\u0442\u044c»,»imageUuid»:»cbf3e8d3-863a-5b81-9dd9-f0c431721801″}
При любых строительных и ремонтных работах используется штукатурка – выравнивание стен, устранение дефектов, мелких трещин, стыков и многое другое. Современные составы используются практически для любой работы, поэтому потребитель имеет возможность выбора из широкого ассортимента.Однако перед закупкой материала нужно четко понимать, какой расход смеси будет приходиться на один квадратный метр.
597 просмотров
Какие факторы нужно учесть?
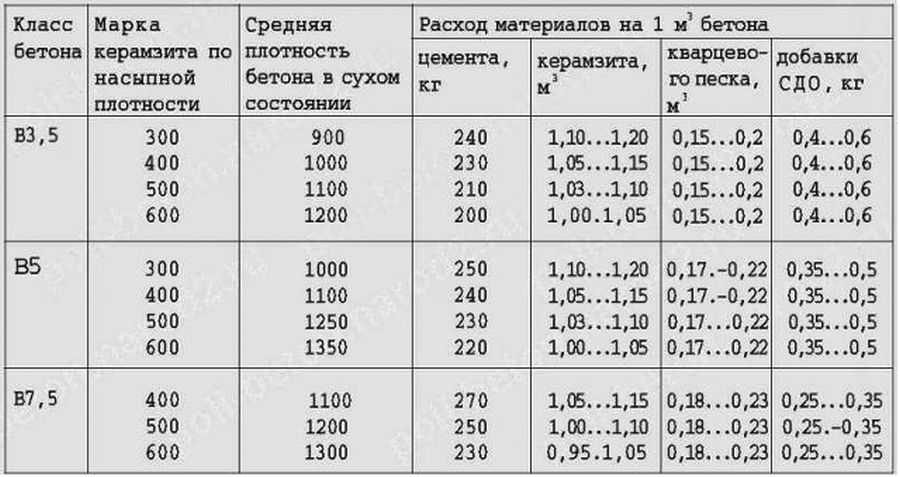
Стоит учитывать, что многие производители указывают на упаковках с сухой смесью расчет на 1 квадратный метр слоя толщиной до 10 мм. Все дальнейшие расчеты следует производить с учетом этого показателя.Для примера мы рассмотрим обычную гипсовую штукатурку или любые другие «легкие» смеси на основе гипса. На общий расход будет влиять несколько важных факторов:• Свойства и особенности готового состава.• Рабочее основание – наличие дефектов, трещин или кривизны поверхности.Важно. Учитывайте, что от вертикального и горизонтального уровня будет зависеть количество материала. Если отклонения слишком большие, то разумно использовать гипсокартонные плиты. Как правило, стены выравнивают штукатуркой до критической кривизны в 2.
Алгоритм вычислений.
Профессионалы чаще всего используют специальный алгоритм, который позволяет быстро оценить примерный расход состава на стенку или квадратный метр. Для этой цели нужно выполнить несколько действий:• Шаг 1 – очистить поверхность от дефектов, старого материала и подготовить основание под работу.• Шаг 2 – установить специальные маяки, которые позволяют точно определить кривизну поверхности. Как правило, на одной плоскости ставится минимум 2-3 маяка. Также используется лазерный уровень.• Шаг 3 – проводятся замеры с обозначением главных точек, которые позволяют точно определить степень отклонения от нормы.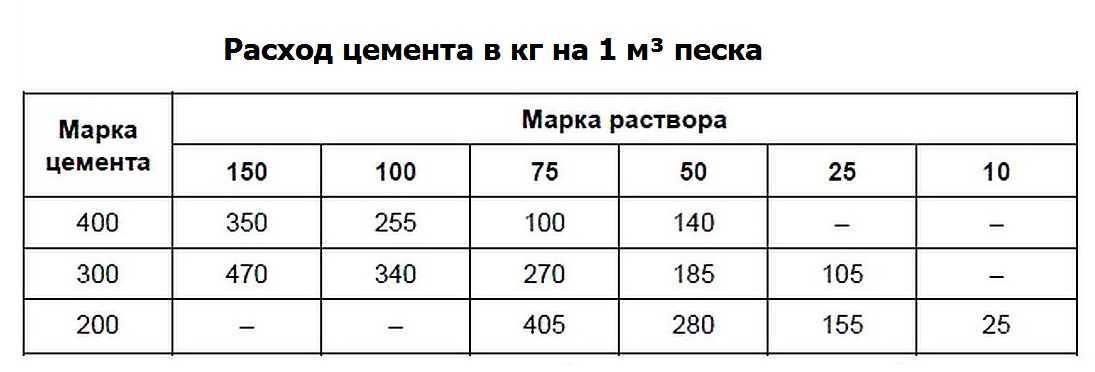
Стандартный расход гипсовой штукатурки.
Стоит отметить, что для всех смесей используется разный расход, но чаще всего на слой толщиной до 1 мм уходит примерно 900 грамм сухой смеси на квадратный метр. Но вы должны понимать, что это усредненное значение.В зависимости от производителя и марки штукатурки этот показатель может отличаться – до 100 грамм в большую и меньшую сторону. Обычно мастер смотрит на прописанные производителем регламентированные условия по потреблению.Использовать можно и стандартную формулу, которая подойдет для большинства составов. Например, если нам нужно покрыть штукатуркой поверхность стены площадью 15 квадратных метров с толщиной покрытия до 5 мм. В таком случае используется формула:• 0.9х15х5 = 67.5 кг.Конечно, это примерное значение и расход может быть больше из-за кривизны стен или наличия крупных дефектов. Таким образом, можно рассчитать не самый точный, но примерный расход.
Благодарим за прочтение!
Надеемся наша статья была для вас полезной. Если у вас остались вопросы или требуется помощь квалифицированных специалистов, мы непременно вам поможем! Будем рады видеть вас на нашем сайте whitezip.ru
Калькулятор цементного раствора – расчет объема и количества компонентов для приготовления раствора для кладки, стяжки
Строим дом » Строительный калькулятор » Калькулятор строительных работ » Онлайн калькулятор расчета цементного раствора – объем, состав, пропорции
В строительстве используется масса различных цементных
растворов, расчет объема и пропорций которых имеет определяющее значение.
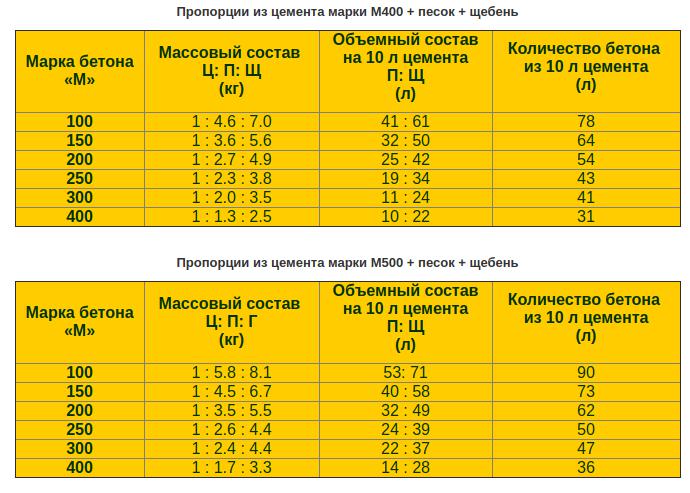
Калькулятор позволит рассчитать, сколько цемента, песка и воды нужно для приготовления 1 м3 цементно-песчаного раствора.
Процедура расчета составляющих компонентов раствора не сложная, если воспользоваться онлайн калькулятором. Заполнив поля можно моментально получить точный расчет количества цемента, песка и воды для приготовления цементного раствора заданной марки, от М25, до М100.
Обратите внимание, фракция, чистота и плотность материала повлияют на качество цементного раствора.
К сожалению, в мобильной версии сайта калькулятор не работает, для расчета перейдите на компьютерную (полную) версию.
| Объем раствора: | м3 | |
| Марка раствора: | М25М50М75М100 | |
| Итог: | ||
| Цемент: | 0 | |
| Песок: | 0 | |
| Вода: | 0 | |
14 442
0
Рекомендуем статьи на похожие темы
Калькулятор расчета объема бетона – как рассчитать, сколько необходимо цемента, песка, щебня и воды на 1 м3 или определенный объем бетона с учетом. ..
..
Программа-калькулятор расчета бетона и арматуры для фундамента – как рассчитать, сколько бетона нужно на фундамент (кубатура), по периметру, глубине,…
Калькулятор расчета ламината онлайн. Программа для подсчета расхода и количества ламината по площади с учетом схемы укладки – прямой и от угла (по…
Расчет расхода напольного покрытия: керамическая плитка, линолеум, паркет, паркетная доска, ламинат, ковролин. С помощью калькулятора можно посчитать…
Калькулятор обоев по площади, по периметру, с раппортом, по длине и ширине стен комнаты, с учетом окон и дверей. Как рассчитать количество рулонов…
Оставьте свой комментарий
Новое Советы
Показать все
Популярное Обсуждения
mc kirill
(2) Строительство дома из арболита (арболитовых блоков) – технология возведения, от фундамента до крыши
Строительство дома из арболита (арболитовых блоков) – технология возведения, от фундамента до крыши
Такая ситуация, мне начали строить дом из арболита, но наделали кучу ошибок по кладке (ниже фото).

Ваня таганский
(1) Утепление входной металлической двери – правильная теплоизоляция своими руками
Утепление входной металлической двери – правильная теплоизоляция своими руками
Бюджетный способ утеплить китайскую дверь от дяди Вани. В отличие от обычной пустотелой двери, в китайской хотя бы бумага внутри. Конечно, эти соты из прессованного картона мало помогут в мороз, но
penoplexman
(6) Входные двери с терморазрывом – металлические термодвери для частного дома
Входные двери с терморазрывом – металлические термодвери для частного дома
Установил термодверь в декабре 2015 года. До этого стояла стальная дверь, утепленная внутри полотна и по периметру. Температура в коридоре была ниже, нежели в комнатах (коридор отапливаемый).
 После
Послеadmin
(9) Монтаж водосточной системы своими руками – установка водостоков для крыши
Монтаж водосточной системы своими руками – установка водостоков для крыши
Пытались помочь в рамках своей компетенции.Раз уж комплектующие Деке, то разумно будет согласовать эти вопросы с ними.Да, в скором будущем на сайте будет отдельный материал по расчетам водосточной
Леонид-
(9) Монтаж водосточной системы своими руками – установка водостоков для крыши
Монтаж водосточной системы своими руками – установка водостоков для крыши
У Docke эти странные требования заложены в pdf инструкцию по монтажу водосточной системы. Формулу я вывел сам, это не сложно, задачка в пределах школьного курса геометрии. Дело в том, что я купил их
admin
(9) Монтаж водосточной системы своими руками – установка водостоков для крыши
Монтаж водосточной системы своими руками – установка водостоков для крыши
Не уверенны, что сможем дать однозначный ответ насчет градусов.
 Откуда вообще эта формула, на сайте Деке не нашли.
Спросили у ребят, которые профильно занимаются монтажом водостоков. Сказали, что
Откуда вообще эта формула, на сайте Деке не нашли.
Спросили у ребят, которые профильно занимаются монтажом водостоков. Сказали, чтоЛеонид-
(9) Монтаж водосточной системы своими руками – установка водостоков для крыши
Монтаж водосточной системы своими руками – установка водостоков для крыши
Интересно, что те же Дёке, несмотря на свои рекомендации, дают фотографии своих монтажных работ по крутым скатам, которые явно им противоречат (фото). Там скаты смотрят в жёлоб, а не поверх него. Моя
Леонид-
(9) Монтаж водосточной системы своими руками – установка водостоков для крыши
Монтаж водосточной системы своими руками – установка водостоков для крыши
Спасибо за развёрнутый ответ, но он не во всём разъясняет проблему, поэтому уточню вопрос. На прилагаемых рисунках, взятых из рунета, показано то самое поперечное сечение, о котором я говорю, с
admin
(4) Установка забора из сетки рабицы своими руками – пошаговая инструкция
Установка забора из сетки рабицы своими руками – пошаговая инструкция
В описанном вами случае, нужно использовать квадратный профиль с сечением не менее 100х100 мм.
 Ввиду того, что планируется посадка вьющихся растений желательно устанавливать одинаковый профиль по
Ввиду того, что планируется посадка вьющихся растений желательно устанавливать одинаковый профиль поadmin
(2) Как сделать калитку из сетки рабицы для дачи своими руками
Как сделать калитку из сетки рабицы для дачи своими руками
Выбирается индивидуально, но согласно логике, распашная калитка и ворота из рабицы (как и любые другие) должны открываться наружу. Объясняется несколькими причинами. Первая – при экстренной ситуации,
Химические вещества, молярные и массовые проценты
Растворы представляют собой гомогенные (равномерно распределенные) смеси двух или более химических веществ. Растворы могут существовать в виде твердых тел, жидкостей или газов.
Все растворы содержат растворитель и одно или несколько растворенных веществ. Растворитель, часто вода, является наиболее распространенным химическим веществом. Растворенное вещество — это химическое вещество (я), которое менее распространено.
Приготовление растворов
Как растворять твердые вещества и уменьшать масштабы экспериментов
Для проведения экспериментов вам часто потребуется растворять растворенные вещества в твердой форме, чтобы получить растворы определенной концентрации (сила измеряется диссоциацией ионов). Запланируйте один час на каждые 2-4 решения, которые вам нужно подготовить. Вам понадобятся весы для взвешивания растворенного вещества и мерный цилиндр для измерения растворителя (если это вода).
Во-первых, определите концентрацию (весовой процент или молярность, см. ниже) и количество (миллилитров) раствора, который вам нужен, из вашей лабораторной процедуры. Во-вторых, рассчитайте необходимое количество растворенного вещества в граммах, используя одну из приведенных ниже формул. Затем взвесьте растворенное вещество и добавьте его в стакан для смешивания. Наконец, мерным цилиндром измерьте необходимый объем воды в миллилитрах и добавьте его в химический стакан. Перемешивайте раствор, пока все химикаты не растворятся.
Разбейте твердые комки химиката с помощью ступки и пестика или осторожно раздавите молотком в пластиковом пакете. Химические вещества растворяются быстрее при осторожном нагревании раствора и перемешивании.
Если для экспериментов требуется большое количество химикатов, можно уменьшить масштаб. Уменьшение масштаба снижает угрозы безопасности, затраты на химикаты и утилизацию отходов.
Большинство экспериментов можно сократить, разделив растворенное вещество и растворитель на коэффициент по вашему выбору. Например, эксперимент, требующий 50 г растворителя и 250 мл воды, можно уменьшить в 10 раз, чтобы в нем использовалось только 5 г растворителя и 25 мл воды. Вы можете упростить масштабирование, используя стаканы меньшего размера, пробирки и другое измерительное оборудование.
При приготовлении химических растворов всегда используйте соответствующее защитное оборудование.
Как приготовить молярные растворы
Молярные (М) растворы основаны на количестве молей химического вещества в одном литре раствора.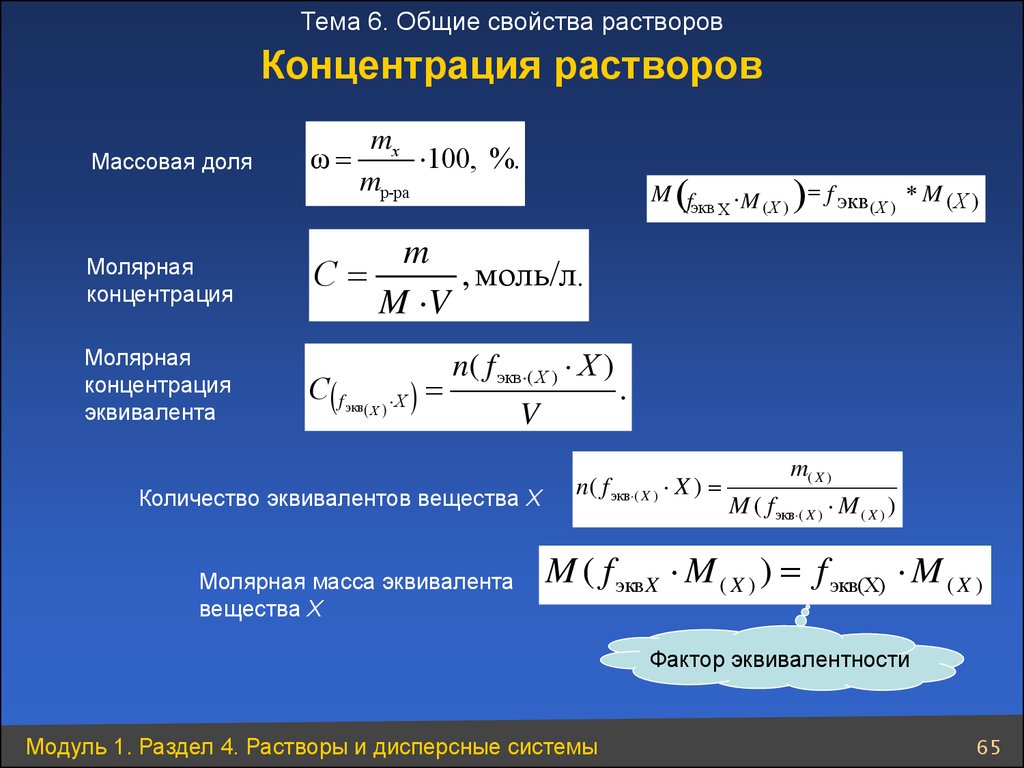 Моль состоит из 6,02×10 23 молекул или атомов. Молекулярная масса (MW) — это масса одного моля химического вещества. Определите молекулярную массу с помощью таблицы Менделеева, добавив атомную массу каждого атома в химическую формулу.
Моль состоит из 6,02×10 23 молекул или атомов. Молекулярная масса (MW) — это масса одного моля химического вещества. Определите молекулярную массу с помощью таблицы Менделеева, добавив атомную массу каждого атома в химическую формулу.
Пример: для молекулярной массы CaCl 2 , добавьте атомную массу Ca (40,01) к массе двух Cl (2 x 35,45), чтобы получить 110,91 г/моль. Следовательно, 1М раствор CaCl 2 состоит из 110,91 г CaCl 2 , растворенных в достаточном количестве воды, чтобы получился один литр раствора.
Когда молекулярная масса растворенного вещества известна, вес химического вещества, растворяемого в растворе, для молярного раствора менее 1 М рассчитывается по формуле:
- грамма химического вещества = (молярность раствора в молях/литр) x (молекулярная масса химиката в г/моль) x (мл раствора) ÷ 1000 мл/литр
Например, чтобы приготовить 100 мл 0,1 М раствора CaCl 2 , используйте предыдущую формулу, чтобы узнать, сколько CaCl 2 вам нужно:
- грамма CaCl 2 = (0,1) x (110.
 91 ) х (100) ÷ (1000) = 1,11 г
91 ) х (100) ÷ (1000) = 1,11 г
Теперь можно приготовить раствор: растворите 1,11 г CaCl 2 в воде, достаточном для приготовления 100 мл раствора. Необходимое количество воды будет чуть меньше 100 мл.
Весы и мерная колба используются для приготовления молярных растворов. Процедура приготовления молярного раствора в мерной колбе вместимостью 100 мл следующая:
- Рассчитайте массу растворенного вещества, необходимого для приготовления 100 мл раствора, используя приведенную выше формулу.
- Взвесьте необходимое количество растворенного вещества с помощью весов.
- Перенесите растворенное вещество в чистую сухую мерную колбу на 100 мл.
- Медленно добавьте дистиллированную воду в мерную колбу. При этом вымойте все растворенное вещество на дно колбы. Продолжайте добавлять воду, пока не достигнете отметки 100 мл на горлышке колбы.
- Поместите пробку в колбу и осторожно вращайте колбу, пока все растворенное вещество не растворится.

Если у вас нет мерной колбы, вместо нее можно использовать мерный цилиндр на 100 мл. Просто добавьте растворенное вещество в градуированный цилиндр, а затем добавьте дистиллированную воду, пока не достигнете отметки 100 мл в боковой части цилиндра.
Как приготовить весовые проценты (вес.%) растворов
В весовых процентах растворов вес растворенного вещества делится на вес раствора (растворенное вещество + вода) и умножается на 100. Поскольку плотность воды равна 1 г/мл, формула для расчета количества растворенного вещества, которое необходимо смешать для получения раствора в процентах по массе:
- г растворенного вещества = (масс.% раствора) x (мл воды) ÷ (100 – масс.% раствора)
Например, чтобы приготовить 100 мл 10% раствора NaCl (поваренной соли), используйте предыдущую формулу, чтобы узнать, сколько NaCl вам нужно:
- грамма NaCl = (10) x (100) ÷ (100 – 10) = 11,1 г
Теперь можно приготовить раствор: растворите 11,1 г NaCl в 100 мл воды.
Создайте собственное решение для следующих проектов:
Frozen Bubbles
Rainbow Reaction
Биологический тест на токсичность
Гальваническое покрытие: ключ с медным покрытием
Реакции в растворе — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 239
Раствор состоит из двух или более веществ, растворенных в жидкой форме. Не путать со смесью , которая является гетерогенной — существует множество веществ с различной структурой — растворы гомогенны, что означает, что атомы растворенного вещества равномерно распределены по всему растворителю (например, вода, этанол). Думайте об этом как о сравнении чашки (растворенной) сахарной воды и чашки воды с кубиками лего в ней. Растворенное вещество — это вещество, растворенное в растворе, а растворитель — вещество, осуществляющее растворение.
Думайте об этом как о сравнении чашки (растворенной) сахарной воды и чашки воды с кубиками лего в ней. Растворенное вещество — это вещество, растворенное в растворе, а растворитель — вещество, осуществляющее растворение.
пр.
Раствор NaCl в воде Смесь кубиков лего и воды
Примечание. Все растворы являются смесями, но не все смеси являются растворами.
Растворители
Вода (H 2 O) является наиболее распространенным растворителем, используемым для растворения многих соединений или приготовления кофе. Другие распространенные растворители включают скипидар (разбавитель для краски), ацетон (средство для снятия лака для ногтей) и этанол (используется в некоторых духах). Такие растворители обычно содержат углерод и называются органическими растворителями. Растворы с водой в качестве растворителя называются водными растворами; у них есть особые свойства, которые рассматриваются здесь.
Растворенные вещества
Различные химические соединения растворяются в растворенных веществах в разной степени. Некоторые соединения, такие как сильная соляная кислота (HCl), полностью диссоциируют в растворе на ионы. Другие, такие как слабое основание аммиак (NH 3 ), только частично диссоциируют. Однако другие соединения, такие как спирт, вообще не диссоциируют и остаются соединениями. В лабораторных реакциях часто участвуют кислоты и основания, которые более подробно описаны здесь.
Некоторые соединения, такие как сильная соляная кислота (HCl), полностью диссоциируют в растворе на ионы. Другие, такие как слабое основание аммиак (NH 3 ), только частично диссоциируют. Однако другие соединения, такие как спирт, вообще не диссоциируют и остаются соединениями. В лабораторных реакциях часто участвуют кислоты и основания, которые более подробно описаны здесь.
Концентрация
Концентрация – это мера количества растворенного вещества в определенном количестве растворителя. Знание концентрации раствора важно, среди прочего, для определения силы кислоты или основания (pH). Когда концентрация растворенного вещества настолько велика, что он больше не растворяется, раствор считается насыщенным.
Ученые часто используют молярность для измерения концентрации.
молярность = моль/литр
Поскольку стехиометрия реакции зависит от молярных соотношений, молярность является основным показателем концентрации.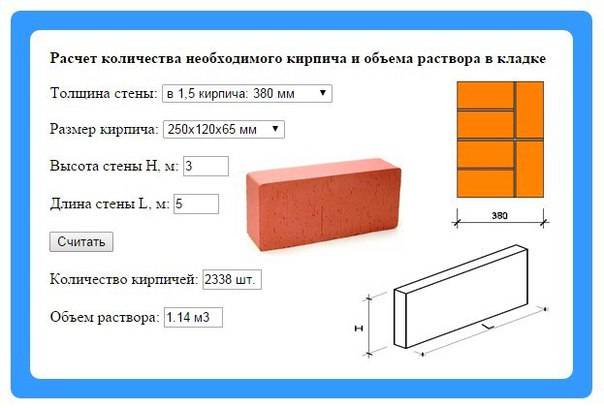
Менее распространенная единица концентрации называется моляльностью .
Моляльность = моль/кг растворителя
Ученые иногда используют моляльность для измерения концентрации, поскольку объемы жидкости незначительно изменяются в зависимости от температуры и давления. Однако масса остается неизменной и может быть точно измерена с помощью весов. Коммерческие концентрированные продукты обычно выражают в процентах по массе; например, техническая концентрированная серная кислота, содержащая 93-98% H 2 SO 4 по массе в воде (Hill, Petrucci 116).
Приготовление раствора
Растворы, используемые в лаборатории, обычно готовят либо из твердых растворенных веществ (часто солей), либо из исходных растворов.
Чтобы приготовить раствор из твердых растворенных веществ, сначала рассчитайте, сколько молей растворенного вещества содержится в желаемых растворах (используя молярность). Рассчитайте необходимое количество твердого вещества в граммах, используя необходимые моли и молярную массу растворенного вещества, и взвесьте необходимое количество.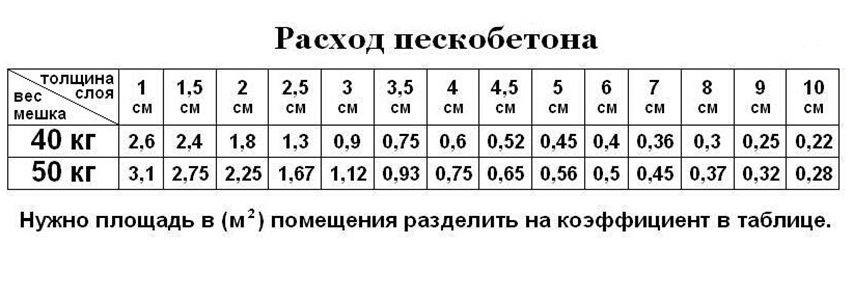 Перенесите растворенное вещество в емкость (предпочтительно в мерную колбу, которая наиболее точно измеряет объем раствора, указанный на колбе) и добавьте небольшое количество растворителя. Тщательно перемешайте, чтобы растворенное вещество растворилось. Как только растворенное вещество растворится, добавьте оставшийся растворитель, чтобы получить раствор нужного объема, и тщательно перемешайте.
Перенесите растворенное вещество в емкость (предпочтительно в мерную колбу, которая наиболее точно измеряет объем раствора, указанный на колбе) и добавьте небольшое количество растворителя. Тщательно перемешайте, чтобы растворенное вещество растворилось. Как только растворенное вещество растворится, добавьте оставшийся растворитель, чтобы получить раствор нужного объема, и тщательно перемешайте.
Например, чтобы получить 0,5 литра 0,5-молярного NaCl:
1. Умножьте концентрацию (0,5 моль/литр) на нужный объем раствора (0,5 литра), чтобы найти необходимое количество молей NaCl.
0,5 моль/литр * 0,5 литра = 0,25 моля NaCl
2. Умножьте количество молей NaCl на его молярную массу (58,44 г/моль), чтобы найти необходимое количество растворенного вещества в граммах.
(0,25 моль NaCl) * (58,44 г/моль) = 14,61 г NaCl
Приготовление раствора определенной концентрации из исходного раствора называется разбавлением. При разбавлении раствора имейте в виду, что добавление растворителя к раствору изменяет концентрацию раствора, но не количество уже присутствующего растворенного вещества.
Чтобы разбавить раствор известной концентрации, сначала определите количество молей растворенного вещества в растворе, умножив молярность на объем (в литрах). Затем разделите на желаемую молярность или объем, чтобы найти необходимый объем или концентрацию.
Используемое уравнение простое:
M 1 V 1 = M 2 V 2
M 1 и В 1 — концентрация и объем исходного ) раствор для разбавления; М 2 и V 2 — желаемая концентрация и объем конечного раствора.
Стехиометрия раствора
Для реакций, протекающих в растворах:
- Рассчитайте количество молей реагирующего растворенного вещества, умножив концентрацию (молярность) на объем раствора (литры)
- Определите предельный реагент, если он есть
- Следуйте стехиометрическому процессу.
- Преобразуйте полученные моли растворенного вещества обратно в молярность путем деления на общий объем в литрах раствора, использованного в реакции.

- В случае реакций с участием ионов (например, в реакциях между сильными кислотами и основаниями) исключите ионы-спектаторы из общего ионного уравнения. Ионы-спектаторы не реагируют в уравнениях.
- Если концентрация не указана, а указаны молярная масса и объем, используйте плотность (граммы/литр), чтобы найти количество растворенного вещества в граммах, а затем переведите его в моли.
Ссылки
- Хилл, Петруччи. Общая химия: комплексный подход, второе издание. Нью-Джерси: Прентис Холл, 19 лет.99.
- Петруччи, Харвуд, Херринг, Мадура. Общая химия: принципы и современные приложения, девятое издание. Нью-Джерси: Прентис Холл, 2007. .
Внешние ссылки
- en.Wikipedia.org/wiki/Solvent
- http://en.Wikipedia.org/wiki/Molar_concentration
Проблемы
- Раствор готовят путем растворения 44,6 г ацетона (OC(CH 3 ) 2 ) в воде с получением 1,50 л раствора.
 Какова молярность полученного раствора?
Какова молярность полученного раствора? - Для определенной лабораторной процедуры требуется 0,025 M H 2 SO 4 . Сколько миллилитров 1,10 M H 2 SO 4 нужно развести в воде, чтобы приготовить 0,500 л 0,025 M H 2 SO 4 ?
- Образец насыщенного NaNO 3 (водный) составляет 10,9 М при 25 градусах Цельсия. Сколько граммов NaNO 3 содержится в 230 мл этого раствора при той же температуре?
- Стакан со 175 мл 0,950 М NaCl оставляют открытым на некоторое время. Если к концу периода времени объем раствора в стакане уменьшился до 137 мл (потеря объема происходит за счет испарения воды), какова будет полученная концентрация раствора?
- Учащийся готовит раствор, растворяя 15,0 мл этанола (C 2 H 5 OH) в воде, чтобы получить раствор объемом 300,0 мл. Рассчитайте концентрацию (молярность) этанола в растворе. (плотность = 0,789 г/мл)
Решения
1.


 После
После Откуда вообще эта формула, на сайте Деке не нашли.
Спросили у ребят, которые профильно занимаются монтажом водостоков. Сказали, что
Откуда вообще эта формула, на сайте Деке не нашли.
Спросили у ребят, которые профильно занимаются монтажом водостоков. Сказали, что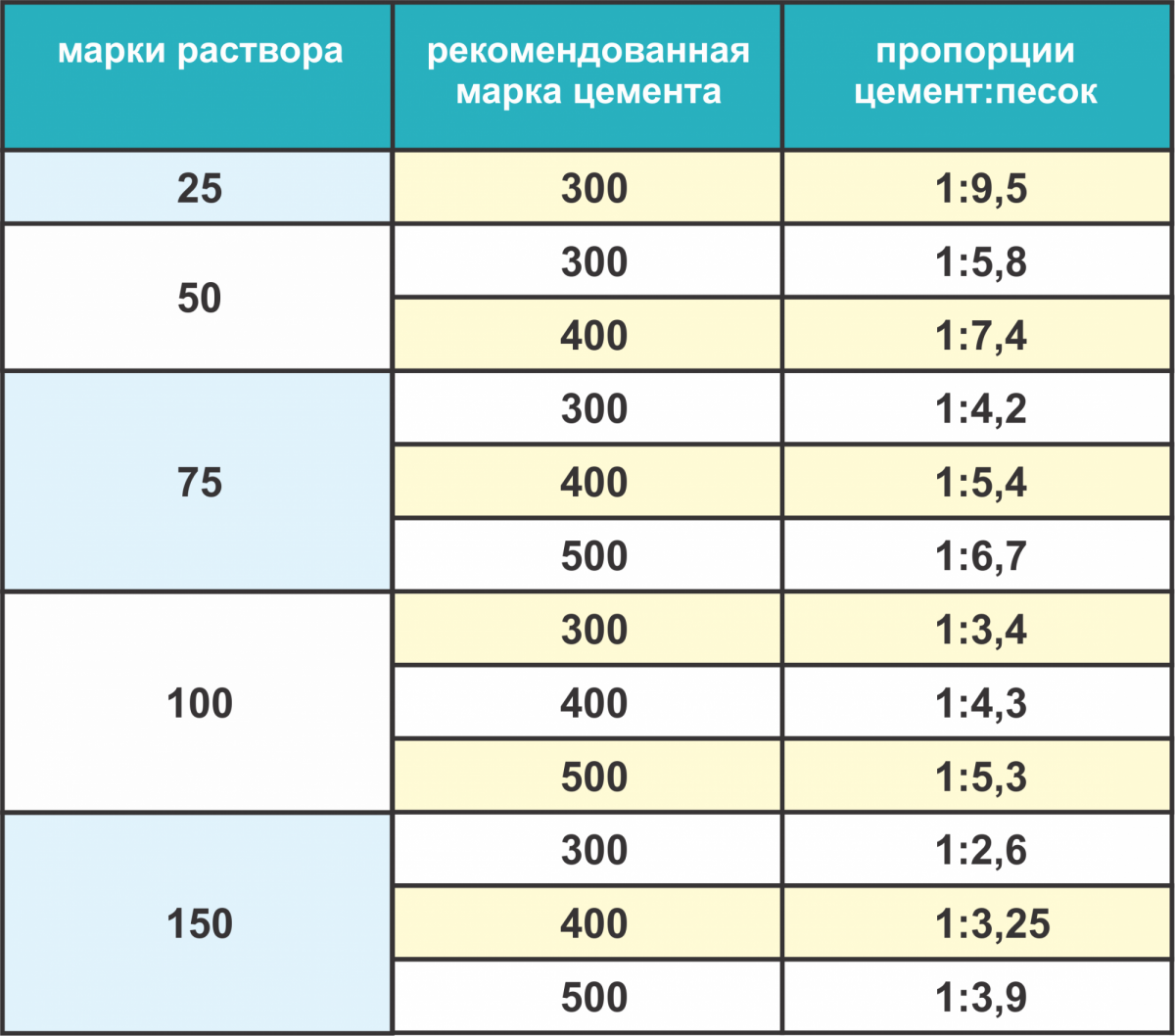 Ввиду того, что планируется посадка вьющихся растений желательно устанавливать одинаковый профиль по
Ввиду того, что планируется посадка вьющихся растений желательно устанавливать одинаковый профиль по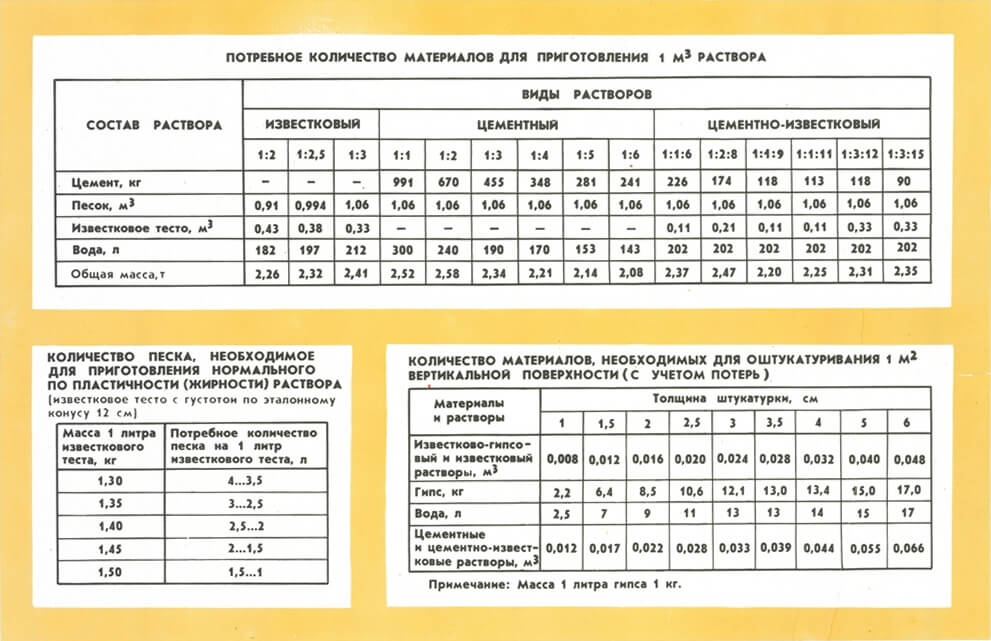 91 ) х (100) ÷ (1000) = 1,11 г
91 ) х (100) ÷ (1000) = 1,11 г
 Какова молярность полученного раствора?
Какова молярность полученного раствора?