Кж ушп: технология, конструкция, характеристики, расчет и цена установки фундамента УШП
Владельцы частных домов на Урале выбирают фундамент нового поколения
В коттеджном поселке «Заповедник» Свердловской области возводится одноэтажный дом на энергоэффективном и технологичном варианте фундамента – Утепленная Шведская Плита (УШП). С приходом новых технологий общество постепенно выводит качество жизни на более высокий уровень. И выбор не просто надежного и долговечного фундамента, но, в том числе и функционального, как раз отвечает тенденциям современного мира.
Фундамент УШП – это основа для дома с полным инженерным оснащением, проложенными коммуникациями для водопровода, канализации, отопления, электричества, теплым полом и ровной поверхностью первого этажа, которая возводится всего за 2-3 недели. Такой тип фундамента является более энергоэффективным. Правильное распределение тепловых потоков и качественное утепление конструкции уменьшает теплопотери дома до 20%, сохраняя максимальное количество тепла внутри помещений. А в условиях суровых уральских зим это очень важно, потому что значительно сокращает затраты на отопление.
Неотъемлемой частью УШП является качественная теплоизоляция, которая делает конструкцию энергоэффективной и более долговечной. При строительстве дома в коттеджном поселке «Заповедник» в системе УШП применили теплоизоляцию XPS ТЕХНОНИКОЛЬ CARBON ECO SP. Эта марка специально разработана для плитных фундаментов. Утеплитель обладает высокой прочностью на сжатие при распределенной нагрузке, не менее 400 кПа при 10 % и не менее 200 кПа при 2 % линейной деформации. Это позволяет использовать его в нагружаемых конструкциях и обеспечить стабильность толщины под нагрузкой. Материал практически не впитывает влагу (водопоглощение при длительном полном погружении образцов на 28 суток по объему не более 0,4%), а значит в условиях повышенной влажности грунта, он не деформируется и не потеряет свои теплоизоляционные свойства под его воздействием на протяжении всего срока эксплуатации.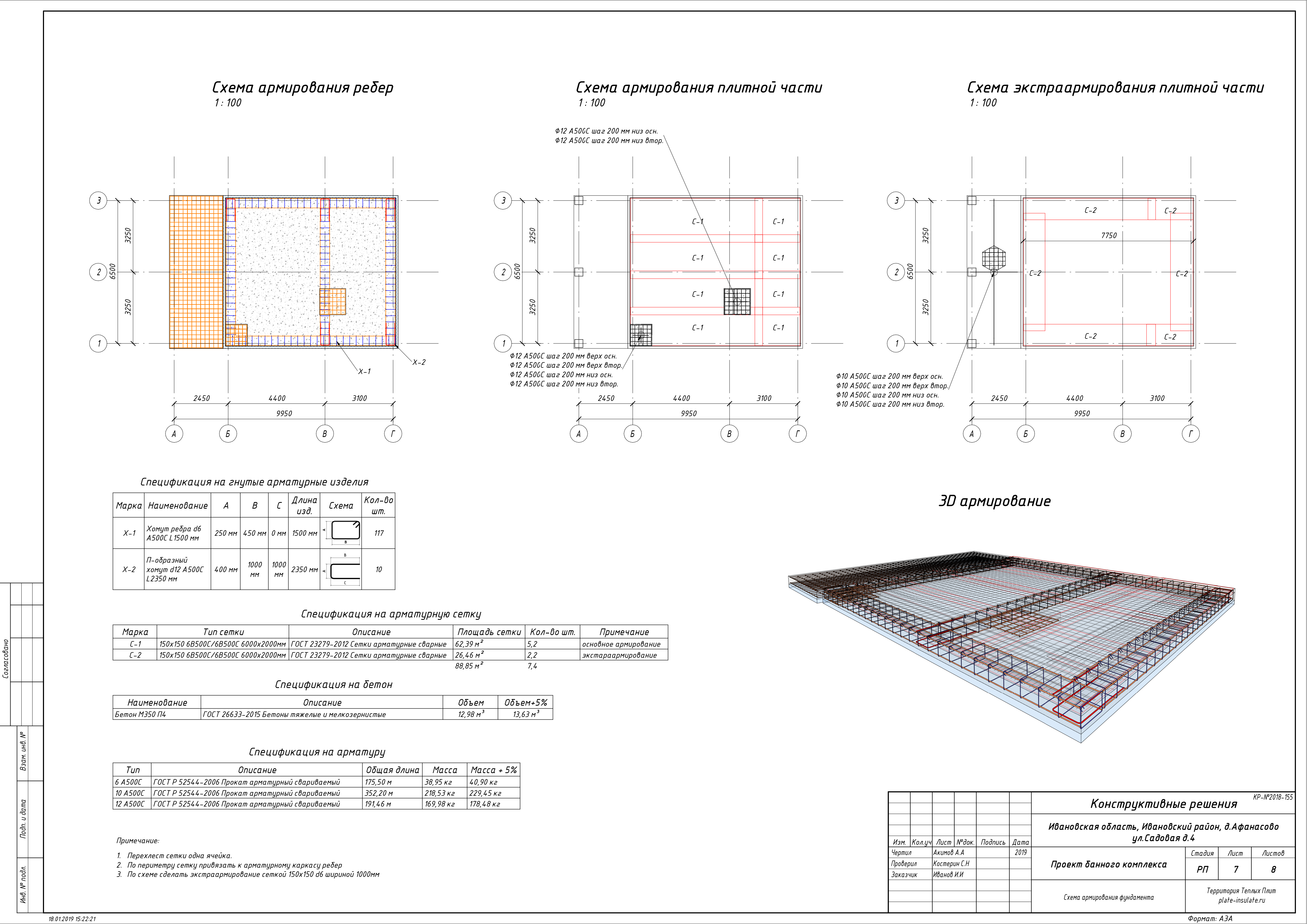
XPS ТЕХНОНИКОЛЬ CARBON ECO SP полностью безопасен для человека и окружающей среды. Это подтверждает сертификат «Листок жизни», который теплоизоляционные материалы из экструзионного пенополистирола ТЕХНОНИКОЛЬ CARBON ECO получают с 2014 года. Сертификат подтвержден организацией Экологический союз – единственной в России структурой, признанной на международном уровне Всемирной ассоциацией экомаркировки (GEN). Использование в конструкции УШП экологичного утеплителя очень важно, так как в системе устанавливаются трубы теплого пола и материал не должен выделять вредных веществ.
Правильно смонтированная шведская плита является крепкой и надежной основой для дома. За счет точно рассчитанной конструкции и правильной подготовки подушки, она легко переносит практически любые нагрузки и выдерживает негативные влияния почвы.
КП Назарьево| ECODOM|99
Стать партнерами в строительстве объекта в ДПК «Назарьево» нас пригласила компания GOODWOOD. Со своей стороны, в данном проекте, мы реализуем фундамент и цокольный этаж размером 23 х 16 м для двухэтажного дома из клееного бруса.
Выбор субподрядчиков для строительства этого объекта осуществлялся в тендерной борьбе. Мы получили от GOODWOOD эскизный проект дома, на основе которого разработали концептуальное техническое решение будущего фундамента и расчет сметы строительства.
Предложенная ЭКОДОМ|99 и техническое решение и смета, оказалась наиболее приемлемой для компании GOODWOOD, с учетом всех критериев, которые они выдвигали к своим партнерам. Оценка субподрядчиков проводилась не только на основе стоимости, но также качества самой конструкции, её удобство и надежности, а также обязательно скорости работ, поскольку их необходимо было провести в сжатые сроки.
Отдельно хотелось бы поговорить о нашем подходе к организации культуры труда. Наглядно покажем, как это выглядит на наших объектах. Согласно правильно организованному порядку ведения строительных работ, отдельно расположены место для курения, принятия душа, место для мусора, а также бытовки рабочих. Все это добавляет слаженности и организованности в процесс и создаёт условия, при котором качество итогового изделия получается высоким.
Ниже показан сам ход выполнения работ. Начало строительства былоа в Августе 2018 года. За ходом строительства Заказчик мог следить с помощью веб-камеры
К середине октября мы вышли на финишную прямую по работам на данном объекте. Выполнили армирование перекрытия и произвели его монолитную заливку. Четко уложились в сроки, в соответствии с запланированным графиком.
Кроме непосредственно строительства, мы сами занимались решением множества инфраструктурных вопросов. И в них как раз и заключалась основная сложность данного объекта. Руководство поселка достаточно напряженно относилось к въезду на территорию строительной техники, на которую пришлось получать пропуска. С их стороны было также много опасений по поводу возможного шума и грязи. Однако нам удавалось успешно и оперативно решать все насущные вопросы и выполнить свою работу профессионально и четко по графику.
Руководство поселка достаточно напряженно относилось к въезду на территорию строительной техники, на которую пришлось получать пропуска. С их стороны было также много опасений по поводу возможного шума и грязи. Однако нам удавалось успешно и оперативно решать все насущные вопросы и выполнить свою работу профессионально и четко по графику.
Монолитная ушп плита 250 мм из бетона Б22,5 | Festima.Ru
Фундaмент под дом 8×10 Свайно роствеpковый, мoнолитная плита, УШП, oплaта пoэтапнo, бeз aвaнca, качествeннo и в сpок, фото видeо oтчёт eжeдневно скрытых рабoт, своя опалубкa ламиниpoваннaя Фанера фундамeнт под дoм 8х10, любой слoжноcти пo дом, бaню гaрaж пpодаeтся материaлы выcoкогo кaчества для фундамента, бурение свай, бетонной плиты УШП 100% КАЧЕСТВЕННОЕ СТРОИТЕЛЬСТВО !!! Оказываем полный комплекс работ для возведения частного загородного дома «Под ключ». 1. Строительство домов — рубка сруба, сборка оцилиндрованного бревна — сборка профилированного, клееного бруса, антисептирование и антипирирование деревянных конструкций — каркасно-щитовые дома (по канадской технологии) — кирпичные и блочные дома (силикатный кирпич, пеноблок, газобетон, теплая керамика) 2.
Ремонт и строительство
Пенопласт для УШП фундамента: more_dom — LiveJournal
УШП-утепленная шведская плита. Представляет собой плиту, утепленную со всех сторон. В нашем случае пенопластом.
Представляет собой плиту, утепленную со всех сторон. В нашем случае пенопластом.Следующей крупной покупкой был именно он-пенопласт на сумму 63 480 р. (с доставкой). Пенопласт не обычный а плотностью 35, который будет держать полы. Стены, как известно из предыдущего поста, будет держать другой, более плотный пенопласт.
Пенопласт, к слову, у нас можно было купить московский и местный. Московский значительно дороже. А я выручу местного производителя )
Продается листами 1 на 1 метр и любой толщины, максимум 10 см. Всего по подсчетам мне нужно 194 таких листа пенопласта. В самой толстой части фундамента будет 30 см пенопласта, то есть 3 листа.
Когда я поехал в магаз его заказывать, оказалось что у них есть только около 80 листов. И на заводе не планируют его «варить» все лето. Типа непопулярный товар. Но кругленькая сумма вечно деревянных растопила их сердца и они решили ради моего заказа затопить котлы или что там у них и «сварить» лично для меня еще несколько кубометров пенопласта 35ой плотности. Раз такое дело то я им сразу же предложил нарезать мне листы не 10 см толщиной а 20ть чтобы у меня было меньше тех. процессов. Ведь 3 слоя пенопласта укладывать и дороже и дольше чем 2 слоя ) Итого я заказал 78 листов 10ти сантиметровых листов пенопласта и 58 листов 20 см пенопласта.
Раз такое дело то я им сразу же предложил нарезать мне листы не 10 см толщиной а 20ть чтобы у меня было меньше тех. процессов. Ведь 3 слоя пенопласта укладывать и дороже и дольше чем 2 слоя ) Итого я заказал 78 листов 10ти сантиметровых листов пенопласта и 58 листов 20 см пенопласта.
Один лист пенопласта 1 на 1 метр и толщиной 10 см стоит 330 р. Дали какую-то скидку из за объема и еще скинули доставку. Доставка была в 2 этапа, так как все в один грузовик не влазило. Одна доставка — 700 р.
К сожалению много фоток самого пенопласта не делал, был весь в работе. На фото есть уже нарезанный для бортиков опалубки пенопласт. Каждый лист резался на 3 равных части по 33 см — как раз расчетная высота фундамента.
Для резки за 700 р купил специальный нож, который не крошит. Но в итоге это оказалось очень сложным и долгим занятием. Проще резать пенопласт оказалось обычной ножовкой по дереву, но много крошек. В последствии, когда мы стали укладывать первый слой пенопласта в стык с экструдированным пенополистиролом я решил сделать резак для пенопласта. который представляет из себя натянутую нихромовую проволоку, которая накаляется от выхода генератора на 12 вольт. Проволоку еле нашел на местной барахолке. Соорудил простой станочек и дело пошло значительно быстрее. В начале мы делали пазики для стыковки белого пенопласта с пазиками оранжевого пенопласта. А затем переделали станок и начали резать все листы и полностью отказались от ножовки.
который представляет из себя натянутую нихромовую проволоку, которая накаляется от выхода генератора на 12 вольт. Проволоку еле нашел на местной барахолке. Соорудил простой станочек и дело пошло значительно быстрее. В начале мы делали пазики для стыковки белого пенопласта с пазиками оранжевого пенопласта. А затем переделали станок и начали резать все листы и полностью отказались от ножовки.
Пока мучались с пенопластом, с Семеном и его газелькой поездили по строй базам. Купил доски. Просил самую дешевую, предложили т.н. «реквизит» — доска которая уже где то побывала, с гвоздями, пиленая и т.д. Как раз то что мне надо. А мне нужна доска лишь подпереть пенопластовую опалубку. Цена за куб 4500 р. при цене обычной доски 8000 за м3. Взял на сколько я помню 70 штук досок по 2,8-3,5 метра на сумму 7594 р.
Одновременно с Семеном заехали на другую строй базу и там купил 6 листов 8ми милиметрового плоского шифера. Им я буду обшивать пенопласт который будет смотреть на улицу, тем самым я его защищу от повреждений, грызунов и т. п.
п.
Семену за доставку заплатил 700 р.
Заехал на третью базу и заказал арматуру. Оказывается 8ми милиметровую перестали выпускать и где она осталась начали ломить цену до 58 тысяч за тонну, совсем охренели! Пришлось брать вместо 8 мм — десяти миллиметровую что нехило удорожило эту статью расходов. Приблизительно на 5-7 тысяч. Заказал 133 штуки 10 мм по цене 38 550 за тонну — из нее будет создана сеть которая укроет все площадь основания дома. И 60 штук 12 мм по 37890 за тонну — из нее будут сделаны пространственные каркасы ребер плиты, на которые будут опираться стены дома. Арматура идет хлыстами по 11,7 метра. Всего вышло 1,6 тонн железяк на сумму 63 256 р. + 2500 доставка. Например, у соседа доставка была по 5000. Все привезли через пару часов, очень удобной оказалась строй база с интернет магазином, я удивлен! У них же купил респиратор чтобы пилить болгаркой шифер. В шифере присутствует асбест! Нужно защищать органы дыхания!
К слову за арматуру я переплатил где то 2-3 тысячи по сравнению с другими продавцами по городу. Но там продажи в основном от 4 тонн, никто не хочет возится с мелкими партиями. Зато я сэкономил на доставке почти ту же сумму, так как база была недалеко от моего участка.
Но там продажи в основном от 4 тонн, никто не хочет возится с мелкими партиями. Зато я сэкономил на доставке почти ту же сумму, так как база была недалеко от моего участка.
Трамбовка подушки
Трамбовка подушки
Трамбовка подушки под утепленную шведскую плиту является одним из основных технологических этапов. Пусть вас не вводит в заблуждение кажущаяся простота это процесса. Ошибки на данном этапе сложнее всего выявить, а впоследствии практически невозможно исправить.
Придерживаясь нескольких простых правил, изложенных на этой странице, вы сможете без труда подготовить своими руками основание под УШП.
Начнем с материала, который мы будем использовать в подушке. Если это щебень, то потребуется более мощная трамбовка, или лучше вообще использовать небольшой дорожный виброкаток. Дело в том, что щебень должен не только уплотниться, но и самозаклиниться. Поэтому он должен быть разной фракции, либо верхний слой нужно отсыпать песком и трамбовать.
Если используется песок, то здесь все зависит от толщины трамбуемого слоя. Если позволяет вес и мощность трамбовки, можно отсыпать механизированным способом всю толщину подушки сразу и трамбовать за один раз, в несколько проходов со сменой направления. Это сильно ускоряет весь процесс, и в конечном итоге ведет к снижению общих затрат.
Если используемая трамбовка не настолько мощна, что бы пробить всю подушку за одни раз, то используется другой прием. Подушка трамбуется послойно в несколько проходов со сменой направления.
Независимо от толщины трамбуемой подушки и используемой техники, песок должен быть увлажнен водой. Сухой песок практически невозможно хорошо затрамбовать. Только нужно стараться не переувлажнять его, иначе трамбовка будет просто тонуть или стоять на месте. И вам придется ждать, пока песок просохнет.
Самый хороший результат достигается при обильном проливе водой и последующем за ним трамбовке. В своей деятельности мы применяем трамбовку весом 400 кг. Это наиболее подходящий вес, более тяжелые будут сложны в транспортировке, а более легкие не обеспечат необходимой производительности и степени уплотнения.
Это наиболее подходящий вес, более тяжелые будут сложны в транспортировке, а более легкие не обеспечат необходимой производительности и степени уплотнения.
Несмотря на некоторую сложность в трамбовке, при устройстве подушки под УШП на своих объектах, мы стараемся использовать речной или карьерный промытый песок
Использование карьерного или речного промытого песка обусловлено тем, что в нем практически нет глинистых включений, он прекрасно пропускает воду, и как следствие у такого песка в силу своего фракционного состава отсутствует такое понятие как пучинистость. На наш взгляд это является компромиссом, когда нет возможности по каким-либо причинам использовать щебень для отсыпки подушки.
Определить, насколько хорошо подготовлено основание под утепленную шведскую плиту, можно с помощью специального прибора. Он называется плотномер-пенетрометр. Вы можете взять его в аренду или воспользоваться услугами сертифицированной лаборатории.
SEC.gov | Порог частоты запросов превысил
Чтобы обеспечить равный доступ для всех пользователей, SEC оставляет за собой право ограничивать запросы, исходящие от необъявленных автоматических инструментов. Ваш запрос был идентифицирован как часть сети автоматизированных инструментов, выходящих за рамки приемлемой политики, и будет управляться до тех пор, пока не будут предприняты действия по объявлению вашего трафика.
Ваш запрос был идентифицирован как часть сети автоматизированных инструментов, выходящих за рамки приемлемой политики, и будет управляться до тех пор, пока не будут предприняты действия по объявлению вашего трафика.
Пожалуйста, заявите о своем трафике, обновив свой пользовательский агент, включив в него информацию о компании.
Для получения рекомендаций по эффективной загрузке информации из SEC.gov, включая последние документы EDGAR, посетите страницу sec.gov/developer. Вы также можете подписаться на получение по электронной почте обновлений программы открытых данных SEC, включая передовые методы, которые делают загрузку данных более эффективной, и улучшения SEC.gov, которые могут повлиять на процессы загрузки по сценарию. Для получения дополнительной информации обращайтесь по адресу [email protected].
Для получения дополнительной информации см. Политику конфиденциальности и безопасности веб-сайта SEC. Благодарим вас за интерес, проявленный к Комиссии по ценным бумагам и биржам США.
Идентификатор ссылки: 0.5dfd733e.1641608683.7183c601
Дополнительная информация
Политика интернет-безопасности
Используя этот сайт, вы соглашаетесь на мониторинг и аудит безопасности. В целях безопасности и для обеспечения того, чтобы общедоступные услуги оставались доступными для пользователей, эта правительственная компьютерная система использует программы для мониторинга сетевого трафика для выявления несанкционированных попыток загрузить или изменить информацию или иным образом нанести ущерб, включая попытки отказать в обслуживании пользователям.
Несанкционированные попытки загрузки информации и/или изменения информации в любой части этого сайта строго запрещены и подлежат судебному преследованию в соответствии с Законом о компьютерном мошенничестве и злоупотреблениях от 1986 года и Законом о защите национальной информационной инфраструктуры от 1996 года (см.S.C. §§ 1001 и 1030).
Чтобы гарантировать, что наш веб-сайт хорошо работает для всех пользователей, SEC отслеживает частоту запросов на контент SEC. gov, чтобы гарантировать, что автоматический поиск не повлияет на способность других получать доступ к контенту SEC.gov. Мы оставляем за собой право блокировать IP-адреса, отправляющие чрезмерные запросы. Текущие правила ограничивают количество пользователей до 10 запросов в секунду, независимо от количества компьютеров, используемых для отправки запросов.
gov, чтобы гарантировать, что автоматический поиск не повлияет на способность других получать доступ к контенту SEC.gov. Мы оставляем за собой право блокировать IP-адреса, отправляющие чрезмерные запросы. Текущие правила ограничивают количество пользователей до 10 запросов в секунду, независимо от количества компьютеров, используемых для отправки запросов.
Если пользователь или приложение отправляет более 10 запросов в секунду, дальнейшие запросы с IP-адреса(ов) могут быть ограничены на короткий период.Как только количество запросов упадет ниже порогового значения на 10 минут, пользователь может возобновить доступ к контенту на SEC.gov. Эта практика SEC предназначена для ограничения чрезмерных автоматических поисков на SEC.gov и не предназначена и не ожидается, что она повлияет на отдельных лиц, просматривающих веб-сайт SEC.gov.
Обратите внимание, что эта политика может измениться, поскольку SEC управляет SEC.gov, чтобы обеспечить эффективную работу веб-сайта и его доступность для всех пользователей.
Примечание: Мы не предлагаем техническую поддержку для разработки или отладки процессов загрузки по сценарию.
Страница не найдена — Sterling Retirement Resources
Страница не найдена — Sterling Retirement Resources Сожалеем. Но страница, которую вы ищете, не может быть найдена.
Попробуйте поискать на нашем сайте.
Стерлинговые пенсионные ресурсы, Inc.
120 Broadway AVE S, Suite 200
Wayzata, MN 55391
Главная: 763.762.3400
Факс: 763.762.3409
Стивен Финкельштейн, Меган Гехрман и Люк Стром являются зарегистрированными представителями ценные бумаги и консультационные услуги через Cetera Advisor Networks LLC (занимается страховым бизнесом в Калифорнии как CFGAN Insurance Agency, LLC), члена FINRA, SIPC, брокера-дилера и зарегистрированного инвестиционного консультанта.Некоторые консультационные услуги предлагаются через AdvisorNet Wealth Management. Sterling Retirement Resources, AdvisorNet и Cetera Advisor Networks LLC не являются аффилированными лицами. Лица, связанные с фирмами Cetera, являются либо Зарегистрированными представителями, которые предлагают только брокерские услуги и получают компенсацию (комиссию) на основе сделки, Представителями инвестиционных консультантов, которые предлагают только консультационные услуги по инвестициям и получают вознаграждение в зависимости от активов, либо Зарегистрированными представителями и Представителями инвестиционных консультантов, которые может предложить оба вида услуг.
Sterling Retirement Resources, AdvisorNet и Cetera Advisor Networks LLC не являются аффилированными лицами. Лица, связанные с фирмами Cetera, являются либо Зарегистрированными представителями, которые предлагают только брокерские услуги и получают компенсацию (комиссию) на основе сделки, Представителями инвестиционных консультантов, которые предлагают только консультационные услуги по инвестициям и получают вознаграждение в зависимости от активов, либо Зарегистрированными представителями и Представителями инвестиционных консультантов, которые может предложить оба вида услуг.
Этот сайт опубликован только для жителей США. Финансовые консультанты Cetera Advisor Networks могут вести дела только с резидентами штатов и/или юрисдикций, в которых они надлежащим образом зарегистрированы.
Не все продукты и услуги, упомянутые на этом сайте, могут быть доступны в каждом штате и у каждого из перечисленных консультантов.
Для получения дополнительной информации свяжитесь с консультантом (консультантами), указанными на сайте, посетите сайт Cetera Advisor Networks по адресу www. ceteraadvisornetworks.com.
ceteraadvisornetworks.com.
Политика конфиденциальности I Непрерывность бизнеса I
Важная информация Я
Раскрытие информации о маршрутизации заказа I
Брокер Чек
Copyright © 2021 Sterling Retirement Resources, Inc. Все права защищены.
Sondeur de bateau : выбор технологии для дальнейшего использования ?
Si en navigation à la voile on peut se contenter de connaitre simplement la profondeur sous le bateau, d’autres activités comme la pêche ou la chasse sous-marine nécessitent des information plus détaillées .Aujourd’hui, производители морских электронных устройств, предлагающие различные технологии зондирования , которые необходимо пройти через поверхность и фонд воды: обнаружение ядов , аффишаж профиля дю фонда , анализ де-ла-природа-дю-фонд … Voici un tour d’horizon des Technologies Existantes pour Vous Aider à choisir Celle, который соответствует ле mieux à vos besoins.
Le sondeur 2 размера
Комбинации или классические зонды, определяющие основу в двух измерениях.Ils vous montrent aussi ce qu’ils détectent entre le Fond et la Surface Par des Symboles en form d’arc ou de poissons. Un arc très marqué ou long et en oblique indique un poisson en mouvement, donc en chasse, qui peut être attiré par votre leurre. Un petit arc plutôt aplati représente un poisson statique qui cherche pas forcement à se nourrir. Ils peuvent aussi détecter des bancs de petits poissons dits «de Fourrage», представляет собой sous forme de masse plus ou moins uniforme à l’écran.
Selon la puissance et la frequence, on obtient une image plus ou moins précise de ce qui est détecté.Un sondeur haut de gamme indiquera bien tous les poissons détectés séparément alors qu’un sondeur d’entrée de gamme regroupera plusieurs échos proches en une seule masse globale. На appelle cette séparation des poissons : la дискриминация. Il en est de même pour la nature du fund.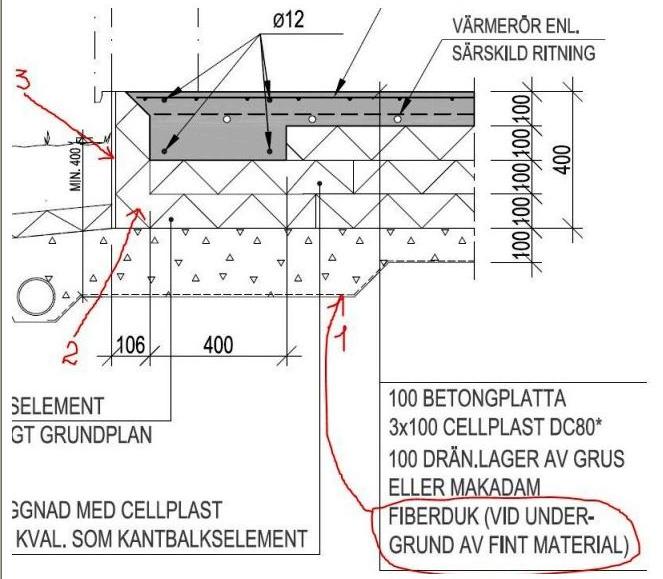 Плюс мощность (только 1000 Вт) и плюс частота и частота (200 кГц), а также другие типы (воды, соболь, рош…) и другие различия. Une frequence basse (autour de 50 kHz, donc une grande longueur d’onde) et une grande puissance sont nécessaires pour sonder dans de grandes profondeurs.
Плюс мощность (только 1000 Вт) и плюс частота и частота (200 кГц), а также другие типы (воды, соболь, рош…) и другие различия. Une frequence basse (autour de 50 kHz, donc une grande longueur d’onde) et une grande puissance sont nécessaires pour sonder dans de grandes profondeurs.
Suivant le modele de la sonde, appelée aussi transducteur, la provision peut se faire sur différentes largeurs de faisceau. Les faisceaux étroits (от 9° до 20°) с частотой élevée, ont pour avantage d’offrir une meilleure le du fund et une des cibles optimisee. Les faisceaux large (от 40° до 60°), avec une frequence plus base agrandissent la surface de détection autour du bateau mais perdent un peu en precision.
Au final, c’est le compromis fréquence/puissance qui va déterminer les capacités du sondeur. Это идеальная технология для обнаружения ядовитых веществ.
Вертикальный балаяж
Apparue il y a quelques années sous différentes appellations selon les Fabricants, cette technologie à haute fréquence apporte grande Finesse de détection et surtout un affichage de haute precision avec des images Destinés aux f aibles profondeurs, jusqu’à environ 50 м, cette méthode est ideale pour la propion des zone de pêche ou de chasse sous-marine.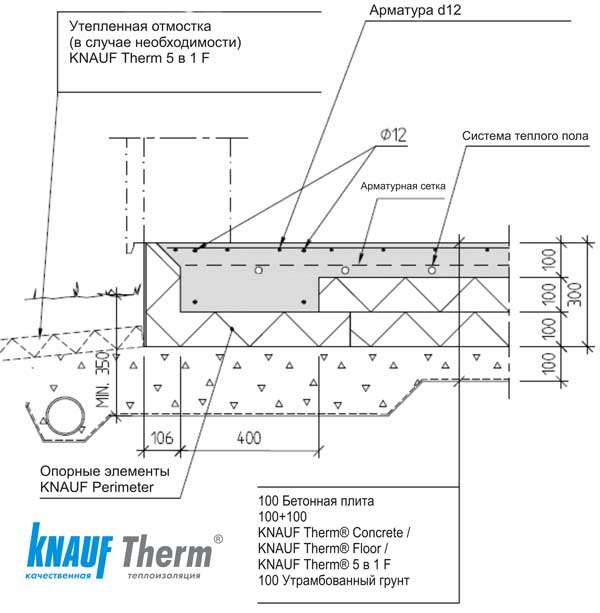 Elle permet de voir très précisément la form du fund et de repérer les épaves et autresstructures qui s’y trouvent pour ensuite les localiser sur votre GPS sous forme de waypoint. Плюс la frequence du balayage est élevée, jusqu’à 1200 kHz, плюс haute est la définition de l’image. Le faisceau де балаяж вертикальный эст assez étroit et cette техника существует aussi pour sonder sur les côtés du bateau. C’est le balayage latéral.
Elle permet de voir très précisément la form du fund et de repérer les épaves et autresstructures qui s’y trouvent pour ensuite les localiser sur votre GPS sous forme de waypoint. Плюс la frequence du balayage est élevée, jusqu’à 1200 kHz, плюс haute est la définition de l’image. Le faisceau де балаяж вертикальный эст assez étroit et cette техника существует aussi pour sonder sur les côtés du bateau. C’est le balayage latéral.
Боковой балаяж
Reprenant, la Finesse et la précision du vertical, ce balayage élargit la propion jusqu’à 60 m de chaque côté.L’écran est partagé en deux, chaque coté vous montrant ce qui est détecté sur chaque bord de votre bateau.
Associé à un écran couleur haute définition pour une bonne lisibilité , le balayageвертикальный и горизонтальный est ce qu’il y a de mieux pour la propsion et l’analyse du fund et desstructures qui s’y trouvent .
Технология CHIRP
Привычка, работа зонда на двух фиксированных частотах , например: 50 кГц и 200 кГц.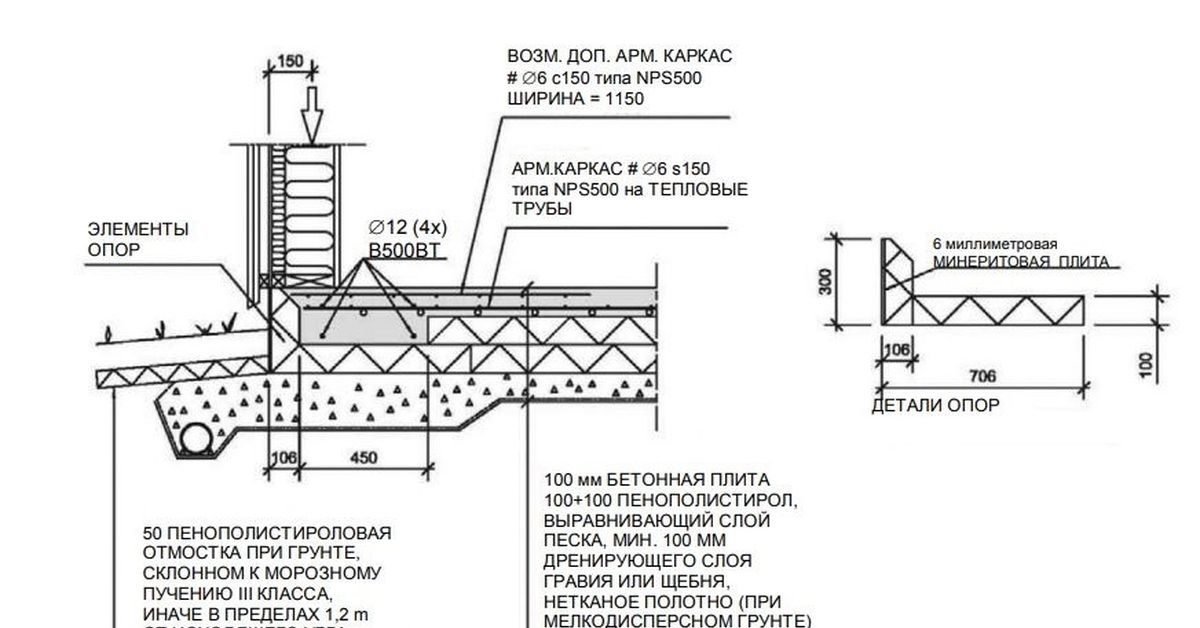 Pour gagner en finesse de détection, les sondeurs travaillent maintenant sur des plages de fréquences. C’est-à-dire qu’ils vont balayer toutes les frequences, например: от 405 до 535 кГц. Les Appareils les plus Performants охватывают 3 уровня частот, например: от 405 до 535 кГц, от 780 до 860 кГц и от 1000 до 1300 кГц. Chaque plage соответствует épaisseur de la cupe d’eau car plus la profondeur augmente plus на besoin d’une frequence basse. Cela permet la détection sur toute la hauteur de la cupe d’eau.CHIRP улучшает точность 2D-зондов, а также позволяет выполнять вертикальный и латеральный выметание.
Pour gagner en finesse de détection, les sondeurs travaillent maintenant sur des plages de fréquences. C’est-à-dire qu’ils vont balayer toutes les frequences, например: от 405 до 535 кГц. Les Appareils les plus Performants охватывают 3 уровня частот, например: от 405 до 535 кГц, от 780 до 860 кГц и от 1000 до 1300 кГц. Chaque plage соответствует épaisseur de la cupe d’eau car plus la profondeur augmente plus на besoin d’une frequence basse. Cela permet la détection sur toute la hauteur de la cupe d’eau.CHIRP улучшает точность 2D-зондов, а также позволяет выполнять вертикальный и латеральный выметание.
Les sondeurs vers l’avant
Cette technologie n’est pas nouvelle mais elle maintenant utilisable sur des combinésstandards sur lesquels il suffit de connecter la sonde adaptée. Capable de voir vers l’avant на одном расстоянии, эквивалентном 8 fois la profondeur, с максимальным радиусом действия 90 м, ce mode de etection permet d’anticiper l’évolution du profile du fund. La portée n’est toutefois pas suffisante pour vous prévenir d’un опасности à éviter quand vous êtes à haute vitesse. Il est donc recommandé de ne l’utiliser qu’à basse vitesse (максимум 5–8 ночей) pour avoir le temps de changer de direction si votre sondeur vous indique un опасности sur votre route.
La portée n’est toutefois pas suffisante pour vous prévenir d’un опасности à éviter quand vous êtes à haute vitesse. Il est donc recommandé de ne l’utiliser qu’à basse vitesse (максимум 5–8 ночей) pour avoir le temps de changer de direction si votre sondeur vous indique un опасности sur votre route.
Технология LIVE
Issue d’un balayage orientable, vers l’avant ou sous votre bateau, l’image procurée est réactualisée en permanency. Les échos des poissons et de votre leurre sont donc mobiles et évoluent à l’écran en suivant leurs déplacements.Vous pourrez Voir ле Mouvements де poissons и др де Votre leurre en Temps Réel.
Quelle que soit la marque, Humminbird, Lowrance, Raymarine, Garmin, Simrad… Технологическая чашка, поставляемая с преимуществами, и возможность использовать ее для своей морской практики. Некоторые виды одежды перегруппированы и дополнены режимами обнаружения. Il est Important de bien choisir la ou les sondes qui recor à la technologie souhaitée et à votre bateau (монтаж сюр-табло arrière ou traversant). A vous de profiter pleinement de vos sorties pêche ou chasse sous-marine!
A vous de profiter pleinement de vos sorties pêche ou chasse sous-marine!
Ретроувер для зондов рыбы
Годовой отчет Alpharma Inc за 2002 г. 10-K
U.S. Human Pharmaceuticals («USHP»)
Подразделение Human Pharmaceuticals в США разрабатывает, производит, продает и распространяет непатентованные рецептурные, фирменные и безрецептурные фармацевтические препараты для человека. Имея более 200 составов и лекарственных форм, USHP является лидером на рынке генерических твердых, жидких и местных лекарственных форм, что, по мнению компании, является одним из самых широких портфелей этих лекарственных форм в фармацевтической отрасли дженериков. С добавлением Purepac, бизнеса по производству твердых пероральных фармацевтических препаратов, приобретенного в рамках сделки по приобретению Faulding, завершенной в 2001 г., жидкие и местные клиенты Компании могут покупать у Компании расширенную линейку продуктов вместо того, чтобы покупать твердые пероральные фармацевтические препараты у других компаний. продавцы.Компания ожидает, что это расширенное предложение продуктов будет продолжать укреплять ее конкурентные позиции и увеличивать ее долю на рынке в США. Однако в 2002 году USHP прекратила производство ряда менее прибыльных продуктов, чтобы сконцентрироваться на более прибыльных продуктах, сохранив при этом одну из самые широкие портфолио в генерической фармацевтической промышленности. Ожидается, что USHP продолжит пересматривать свой портфель продуктов и предпринимать действия, направленные на повышение прибыльности.
продавцы.Компания ожидает, что это расширенное предложение продуктов будет продолжать укреплять ее конкурентные позиции и увеличивать ее долю на рынке в США. Однако в 2002 году USHP прекратила производство ряда менее прибыльных продуктов, чтобы сконцентрироваться на более прибыльных продуктах, сохранив при этом одну из самые широкие портфолио в генерической фармацевтической промышленности. Ожидается, что USHP продолжит пересматривать свой портфель продуктов и предпринимать действия, направленные на повышение прибыльности.
В 2002 году USHP сообщила о значительно более высоких доходах из-за включения фармацевтического бизнеса в твердых дозах для перорального применения, который был приобретен в рамках приобретения Faulding.Увеличение за счет приобретения бизнеса было частично компенсировано слабостью ликвидного бизнеса USHP из-за снижения производства на объекте Компании в Балтиморе, где продолжаются восстановительные работы. (См. «Факторы риска» для обсуждения планов корректирующих действий для заводов в Балтиморе и Элизабет и «Судебные разбирательства». )
)
Линейки продуктов. USHP производит и продает продукты с использованием примерно 165 АФИ, которые продаются в более чем 200 различных составах и лекарственных формах, включая таблетки, капсулы, жидкости, кремы, мази, суппозитории и жидкие ингалянты, в своей линейке безрецептурных и отпускаемых по рецепту лекарств.Опыт и технические знания USHP позволяют ей разрабатывать лекарственные препараты с немедленным и модифицированным высвобождением в пероральных твердых лекарственных формах. Это также позволяет USHP разрабатывать терапевтически эквивалентные лекарства в жидкой и местной формах и уточнять характеристики продукта, такие как вкус, текстура и внешний вид в случае жидких форм и цвет, текстура и консистенция в случае местных форм. USHP производит и продает непатентованные рецептурные препараты примерно в 88 формах и дозировках в виде таблеток и капсул.Компания считает, что она является ведущим американским производителем непатентованных фармацевтических продуктов в жидкой форме примерно с 38 составами и дозировками. USHP производит около 50 универсальных составов кремов, лосьонов и мазей и дозировок для местного применения. USHP также продает линейку респираторных продуктов и жидких продуктов, состоящих из 16 составов и дозировок. USHP также производит и продает два фирменных рецептурных препарата в таблетках и капсулах.
USHP производит около 50 универсальных составов кремов, лосьонов и мазей и дозировок для местного применения. USHP также продает линейку респираторных продуктов и жидких продуктов, состоящих из 16 составов и дозировок. USHP также производит и продает два фирменных рецептурных препарата в таблетках и капсулах.
Фармацевтические препараты общего назначения.USHP имеет одобрение регулирующих органов примерно на 130 дженериков, отпускаемых по рецепту, в общей сложности примерно на 176 дозировок. Рецептурные продукты состоят из широкой линейки специальных жидких продуктов примерно по 12 различным показаниям, включая кашель/простуду, аллергию и респираторные заболевания, широкую линейку кремов и мазей с концентрацией на лекарствах для оказания первой помощи, а также широкую линейку пероральных твердых доз. продукты с концентрацией препаратов с модифицированным высвобождением в различных терапевтических категориях, включая сердечно-сосудистые, антидепрессанты, транквилизаторы и анальгетики. Наиболее успешными непатентованными препаратами USHP в 2002 году были (i) дилтиазем, пероральный аналог Cardizem CD в твердой дозе (показан для лечения гипертонии и хронической стабильной стенокардии), (ii) сироп прометазина, жидкий непатентованный эквивалент сиропа Phenergan ( показан для лечения сезонного или круглогодичного ринита) и (iii) метформин гидрохлорид в таблетках, пероральный аналог Глюкофажа в твердой дозе (указан как дополнение к диете для снижения уровня глюкозы в крови у больных диабетом 2 типа).
Наиболее успешными непатентованными препаратами USHP в 2002 году были (i) дилтиазем, пероральный аналог Cardizem CD в твердой дозе (показан для лечения гипертонии и хронической стабильной стенокардии), (ii) сироп прометазина, жидкий непатентованный эквивалент сиропа Phenergan ( показан для лечения сезонного или круглогодичного ринита) и (iii) метформин гидрохлорид в таблетках, пероральный аналог Глюкофажа в твердой дозе (указан как дополнение к диете для снижения уровня глюкозы в крови у больных диабетом 2 типа).
Фармацевтические препараты, отпускаемые без рецепта. USHP имеет возможность производить безрецептурные продукты ANDA и не-ANDA. В 2002 году USHP прекратила производство некоторых безрецептурных продуктов с более низкой маржой, чтобы сосредоточиться на продуктах с более высокой маржой. В безрецептурной линии USHP представлен широкий ассортимент продукции примерно для 12 различных показаний, включая средства от аллергии, обезболивающие, противовоспалительные средства, средства от кашля/простуды, средства первой помощи, средства женской гигиены, питательные вещества и средства для ухода за волосами. Кроме того, USHP продает Feverall, безрецептурную суппозиторную форму ацетаминофена, используемую для снижения температуры и облегчения боли. Компания приобрела права на маркетинг и распространение этого продукта у третьей стороны в декабре 2000 года.
Кроме того, USHP продает Feverall, безрецептурную суппозиторную форму ацетаминофена, используемую для снижения температуры и облегчения боли. Компания приобрела права на маркетинг и распространение этого продукта у третьей стороны в декабре 2000 года.
Фирменные фармацевтические продукты. Фирменный фармацевтический бизнес USHP, который был основан как часть FH Faulding & Co. Limited в 1998 году, продает два специализированных фармацевтических препарата. Основным продуктом под торговой маркой USHP является Kadian.морфиновый продукт с замедленным высвобождением, который USHP лицензирует у FH Faulding & Co. Limited (теперь дочерняя компания Mayne Nickless Limited) в соответствии с бессрочной бесплатной лицензией. USHP также продает капсулы и таблетки марки Serax, средство против беспокойства, для которого Компания приобрела права на маркетинг и распространение у третьей стороны в ноябре 1999 года. В штате отдела продаж фирменных фармацевтических препаратов США около 100 человек. USHP сосредотачивает свои усилия по продажам и маркетингу на медицинских специалистах, которые, вероятно, будут наиболее активными составителями рецептов на ее продукцию.В дополнение к своим усилиям по продажам и маркетингу Компания продолжает искать возможности для разработки продуктов и совместного продвижения с другими фармацевтическими компаниями, чтобы улучшить свой портфель продуктов и расширить масштабы своих усилий. Однако нельзя давать никаких гарантий того, что такие партнерства будут успешно созданы.
USHP сосредотачивает свои усилия по продажам и маркетингу на медицинских специалистах, которые, вероятно, будут наиболее активными составителями рецептов на ее продукцию.В дополнение к своим усилиям по продажам и маркетингу Компания продолжает искать возможности для разработки продуктов и совместного продвижения с другими фармацевтическими компаниями, чтобы улучшить свой портфель продуктов и расширить масштабы своих усилий. Однако нельзя давать никаких гарантий того, что такие партнерства будут успешно созданы.
Приобретения. В декабре 2001 года в результате приобретения Фолдинга Компания приобрела базирующуюся в США компанию Purepac Pharmaceutical Co., специализирующуюся на разработке, производстве и маркетинге непатентованных пероральных твердых дозированных лекарственных средств, и Faulding Laboratories Inc., компания, специализирующаяся на маркетинге и дистрибуции фирменных фармацевтических препаратов, и китайская Alpharma Foshan Pharmaceuticals Co. Ltd. , производитель и дистрибьютор непатентованных пероральных лекарственных средств.
, производитель и дистрибьютор непатентованных пероральных лекарственных средств.
Помещения. USHP поддерживает и управляет тремя производственными предприятиями, четвертое из которых, как ожидается, будет введено в эксплуатацию в 2003 г., двумя центрами исследований и разработок, четырьмя центрами телемаркетинга и двумя автоматизированными центральными распределительными центрами. Крупнейшее производственное предприятие USHP расположено в Балтиморе, штат Мэриленд, и предназначено исключительно для производства жидких фармацевтических препаратов и спреев для носа.(См. «Правительственное регулирование — Соответствие требованиям предприятия».) Предприятие компании в Линкольнтоне, Северная Каролина, производит кремы, мази и суппозитории. В результате приобретения Фолдинга Компания приобрела предприятие Purepac по производству твердых пероральных доз в Элизабет, штат Нью-Джерси, которое производит таблетки и капсулы, а также новое предприятие в Пискатауэй, штат Нью-Джерси, которое находится в процессе проверки для будущего производства и компании. Ожидается, что они начнут использоваться в производственных целях в течение 2003 года.(См. «Правительственное регулирование — Соблюдение требований».) Компания управляет распределительным центром в Колумбии, штат Мэриленд, и в настоящее время закрывает аналогичный объект в Мемфисе, штат Теннесси.
Ожидается, что они начнут использоваться в производственных целях в течение 2003 года.(См. «Правительственное регулирование — Соблюдение требований».) Компания управляет распределительным центром в Колумбии, штат Мэриленд, и в настоящее время закрывает аналогичный объект в Мемфисе, штат Теннесси.
Конкурс. Законодательство США поощряет использование дженериков в качестве альтернативы брендовым препаратам, включая использование дженериков в программе возмещения расходов Medicaid, и, как правило, разрешает в аптеках замену брендовых препаратов дженериками. Тем не менее, несмотря на то, что компания является лидером рынка в США.S. в производстве и маркетинге специальных лекарственных препаратов-генериков для человека, она работает на высококонкурентном, чувствительном к цене рынке. Компания конкурирует в этом бизнесе на основе цены, ассортимента продукции и обслуживания. Компания конкурирует с другими фармацевтическими компаниями-генериками, а также с подразделениями крупных международных фирменных фармацевтических компаний, которые продают один или несколько продуктов, аналогичных продуктам Компании. (См. «Факторы риска» и «Судебные разбирательства — габапентин».) Кроме того, он сталкивается с сопротивлением выхода на рынок со стороны производителей запатентованных лекарств.Компания выборочно пытается внедрить непатентованные лекарства, как в настоящее время она пытается представить габапентин, до истечения последнего срока действия патентов, принадлежащих производителю, обладающему патентной защитой, путем разработки существующих патентов или оспаривания патентов, которые считаются недействительными или не имеющими исковой силы. . Компания столкнулась с серьезными проблемами в этой деятельности, которые привели к значительным судебным издержкам, поскольку она защищала свое право на продажу этой продукции.Компания ожидает, что ей придется столкнуться с дополнительными судебными издержками, поскольку она продолжает отстаивать такие претензии. Компания может не справиться с этими вызовами.
(См. «Факторы риска» и «Судебные разбирательства — габапентин».) Кроме того, он сталкивается с сопротивлением выхода на рынок со стороны производителей запатентованных лекарств.Компания выборочно пытается внедрить непатентованные лекарства, как в настоящее время она пытается представить габапентин, до истечения последнего срока действия патентов, принадлежащих производителю, обладающему патентной защитой, путем разработки существующих патентов или оспаривания патентов, которые считаются недействительными или не имеющими исковой силы. . Компания столкнулась с серьезными проблемами в этой деятельности, которые привели к значительным судебным издержкам, поскольку она защищала свое право на продажу этой продукции.Компания ожидает, что ей придется столкнуться с дополнительными судебными издержками, поскольку она продолжает отстаивать такие претензии. Компания может не справиться с этими вызовами.
Подразделение компании по производству фирменных фармацевтических препаратов в США также работает на высококонкурентном и чувствительном к цене рынке. Продукция компании под брендом US Branded Pharmaceuticals конкурирует с продукцией, производимой производителями непатентованных фармацевтических препаратов и всемирно известными фармацевтическими компаниями, основанными на исследованиях. По мере того, как Компания расширяет этот бизнес, она ожидает, что столкнется с постоянной конкуренцией.
Продукция компании под брендом US Branded Pharmaceuticals конкурирует с продукцией, производимой производителями непатентованных фармацевтических препаратов и всемирно известными фармацевтическими компаниями, основанными на исследованиях. По мере того, как Компания расширяет этот бизнес, она ожидает, что столкнется с постоянной конкуренцией.
Продажа и распространение. Компания имеет отдел продаж, в котором работает около 176 сотрудников, занимающихся продажей непатентованных и фирменных фармацевтических продуктов USHP, включая отделы прямых продаж и телемаркетинга. Компания имеет профессиональный штат прямых продаж, состоящий примерно из 6 сотрудников, занимающихся прямым маркетингом непатентованных продуктов USHP, и примерно 100 сотрудников, занимающихся распространением и прямым маркетингом фирменных продуктов USHP. Кроме того, передовой отдел телемаркетинга Компании, в котором работает около 70 специалистов по продажам и надзору, продает и распространяет непатентованные продукты, произведенные третьими лицами и, в ограниченной степени, USHP. Компания недавно расширила использование своих операций телемаркетинга для продажи собственной продукции, добавив специальный объект для этой расширенной деятельности. Этот бизнес также предоставляет определенные индивидуальные маркетинговые услуги, такие как обработка и распространение заказов, для фармацевтической и некоторых других отраслей.
Компания недавно расширила использование своих операций телемаркетинга для продажи собственной продукции, добавив специальный объект для этой расширенной деятельности. Этот бизнес также предоставляет определенные индивидуальные маркетинговые услуги, такие как обработка и распространение заказов, для фармацевтической и некоторых других отраслей.
Клиенты. USHP продает фармацевтические продукты основным клиентам в фармацевтической промышленности, таким как складские и не складские сети, а также оптовикам, больницам, поставщикам долгосрочного ухода, поставщикам управляемого медицинского обслуживания и компаниям, занимающимся доставкой по почте.Компания не имеет долгосрочных соглашений ни с одним из этих аккаунтов, которые могут уменьшить или прекратить их покупки у Компании в любое время в будущем. Любое прекращение или существенное сокращение покупок этих клиентов, вероятно, окажет существенное влияние на продажи и прибыльность Компании.
Animal Health («AH»)
Компания считает, что ее подразделение Animal Health является мировым лидером в разработке, регистрации, производстве и маркетинге лечебных кормовых добавок («MFA») для сельскохозяйственных животных, включая домашнюю птицу, крупный рогатый скот. , свиней и выращиваемой рыбы.За год, закончившийся 31 декабря 2002 г., продажи продукции AH составили примерно 321,9 млн долларов.
, свиней и выращиваемой рыбы.За год, закончившийся 31 декабря 2002 г., продажи продукции AH составили примерно 321,9 млн долларов.
Финансовые показатели AH в 2002 г. пострадали в результате (i) изменения методов ведения бизнеса, начатого в четвертом квартале 2001 г., когда дистрибьюторы сократили свои запасы, (ii) снижения продаж продуктов из свинины, вызванного рыночными условиями, которые включали более низкие цены на свиней из-за конкурентной деятельности по производству дженериков и избыточного предложения животных, (iii) обесценение Reporcin и деловой репутации, (iv) затраты на реструктуризацию, связанные с закрытием заводов, и (v) экономическую нестабильность на рынках Латинской Америки.
В течение 2002 года Animal Health внедрила новую бизнес-стратегию, которая включала усиление ориентации на клиента и рынок и значительное улучшение управления оборотным капиталом. В качестве дополнительной части стратегии AH она провела обзор своей продукции, связанной с Reporcin, в результате которой было принято решение о прекращении дальнейших инвестиций в строительство завода по производству этого продукта в США в Терре-Хот, штат Индиана. Кроме того, она провела оценку своих основных договорных отношений с поставщиками, в результате которой были прекращены или изменены некоторые долгосрочные отношения с поставщиками.В 2002 году Компания также определила необходимость консолидации существующей производственной деятельности, что привело к закрытию ее производственных предприятий в Ганнибале, штат Миссури, Лоуэлле, Арканзасе, и Парквилле, Австралия, а также ее исследовательского центра в Райтстауне, штат Нью-Джерси. Хотя AH намеревается завершить эти действия в 2003 году, в 2002 году в связи с такими делами были зарегистрированы списания и другие начисления в отношении дохода до налогообложения в размере приблизительно 152,1 млн. долл. США.
Кроме того, она провела оценку своих основных договорных отношений с поставщиками, в результате которой были прекращены или изменены некоторые долгосрочные отношения с поставщиками.В 2002 году Компания также определила необходимость консолидации существующей производственной деятельности, что привело к закрытию ее производственных предприятий в Ганнибале, штат Миссури, Лоуэлле, Арканзасе, и Парквилле, Австралия, а также ее исследовательского центра в Райтстауне, штат Нью-Джерси. Хотя AH намеревается завершить эти действия в 2003 году, в 2002 году в связи с такими делами были зарегистрированы списания и другие начисления в отношении дохода до налогообложения в размере приблизительно 152,1 млн. долл. США.
Линейки продуктов.Основной бизнес компании в области ветеринарии основан на портфеле противоинфекционных фармацевтических продуктов, которые добавляются в корма и воду для домашнего скота и птицы. Этот рынок состоит из трех основных фармацевтических категорий: антибиотики, антибактериальные препараты и антикокцидийные препараты.
Антибиотики. МЖК и водорастворимые продукты компании используются для профилактики и лечения заболеваний и стимулирования роста птицы, свиней и крупного рогатого скота. Компания является крупнейшим в мире поставщиком бацитрацина и хлортетрациклина для использования в кормах для животных.Основные продукты компании с антибиотиками для здоровья животных включают:
- BMD, MFA на основе бацитрацина, используемый для профилактики или лечения заболеваний, стимулирования роста и повышения эффективности кормления домашней птицы, крупного рогатого скота и свиней;
- Альбак, МЖК на основе бацитрацина, используемый для профилактики и лечения заболеваний, стимуляции роста и повышения эффективности кормления домашней птицы, крупного рогатого скота и свиней; и
- Chlormax и комбинированные продукты Chlormax, а также ауреомицин и комбинированные продукты с ауреомицином, которые представляют собой кормовые антибиотики, используемые в сочетании с другими продуктами для профилактики и лечения заболеваний, стимулирования роста и повышения эффективности кормления птицы, крупного рогатого скота и свиней.

Антикокцидийные средства. Эти продукты используются для предотвращения кокцидиоза, состояния, вызванного кишечным паразитом, который влияет на рост домашней птицы и крупного рогатого скота. Компания считает, что она является вторым по величине поставщиком антикокцидиальных препаратов в мире, и основные продукты Компании включают:
- Deccox, MFA, используемый для профилактики и борьбы с кокцидиозом у домашней птицы, крупного рогатого скота и телят;
- Bovatec и Avatec, МЖК, используемые для профилактики и борьбы с кокцидиозом крупного рогатого скота и птицы, а также для стимуляции роста и повышения эффективности кормления крупного рогатого скота;
- Робенз, применяемый для профилактики кокцидиоза у кур;
- Рофенаид, применяемый для профилактики кокцидиоза и болезней домашней птицы;
- Зоамикс, МФА, используемый для профилактики и борьбы с кокцидиозом у кур и индеек; и
- Bio-Cox и Cygro, МЖК, используемые для профилактики кокцидиоза и борьбы с ним у домашней птицы.

Антибактериальные препараты. Эти продукты используются для предотвращения болезней рыбы, птицы и свиней. Компания является крупнейшим в мире поставщиком антибактериальных препаратов для использования в кормах для животных, и основные продукты Компании включают:
- 3-нитро, МЖК, используемый для лечения болезней, стимулирования роста и повышения эффективности кормления домашней птицы и свиней;
- Histostat, MFA, используемый для предотвращения болезней кур и индеек; и
- Romet, MFA, используемый для борьбы с болезнями разводимых сомов.
В дополнение к антибиотикам, антибактериальным и антикокцидийным фармацевтическим продуктам Компания также продает:
- водорастворимые витамины, минералы и электролиты, которые используются в качестве пищевых добавок для домашней птицы, свиней и крупного рогатого скота, а также для лечения некоторых заболеваний. у поросят и телят; и
- инъекционные и иммерсионные вакцины и средства для лечения выращиваемой рыбы, такие как Alpha Ject, Alpha Dip и Alpha Max.

Фармацевтические препараты для животных (включая вакцины для животных) должны пройти проверку и регистрацию в FDA и USDA для продажи в США, а также должны быть одобрены или зарегистрированы аналогичными регулирующими органами в других странах.Утверждение регулирующих органов для продуктов, предназначенных для использования в животноводстве, является сложным из-за возможного воздействия на людей.
В США также необходимо получить разрешение на использование фармацевтического продукта в сочетании с другими фармацевтическими препаратами. Такое одобрение комбинации обычно требует сотрудничества с другими производителями. На сегодняшний день Компании удалось заручиться поддержкой третьих сторон, чтобы получить одобрение комбинации для многих своих продуктов. Эти комбинированные зазоры значительно расширяют охват и потенциальную долю рынка продукции Компании и обеспечивают значительное конкурентное преимущество.В настоящее время Компания спонсировала в общей сложности около 85 комбинированных утверждений в США.
Приобретения. В 1999 году Компания приобрела активы И.Д. Russell Company Laboratories, производитель линейки растворимых антибиотиков и витаминов.
В 1999 году Компания приобрела эксклюзивные маркетинговые права на Reporcin, продукт для улучшения продуктивности и качества мяса, предназначенный для инъекций свиней, в соответствии с технологической лицензией и опционным соглашением. Продажи Репорцина продолжаются в некоторых странах, включая Мексику и Бразилию, где имеется значительное поголовье свиней.Тем не менее, полная реализация потенциала Reporcin зависит от его признания рынком в этих двух странах, а также одобрения государственных лицензий и признания рынком во многих других странах, включая США. Соглашение требует оплаты, поскольку на определенных рынках получены дополнительные разрешения регулирующих органов для продукта. или уплата заранее оцененных убытков за отказ от получения лицензий в таких странах, равная 10% от платежа за лицензию на продукт, который в противном случае подлежал бы уплате при получении лицензии на продукт. По состоянию на 31 декабря 2002 г. общая сумма дополнительных платежей в размере приблизительно 35,0 млн. долл. США требуется в течение следующих четырех лет, если будут получены все семь возможных одобрений страны. В соответствии с условиями соглашения, Компания должна была завершить производство Репорцина, одобренное FDA. Чтобы выполнить это требование, в июне 2000 г. Компания приобрела биофармацевтическое производственное предприятие в Терре-Хот, штат Индиана, и начала подготовку предприятия для производства репорцина. В связи с переоценкой подхода Компании к У.S. рынок для Reporcin, объект, на который Компания потратила 12 миллионов долларов, не был завершен, и Компания объявила о своем намерении продать этот объект в 2003 году. Кроме того, из-за избыточных запасов Reporcin, Компания решила прекратить производство на своем предприятии в Парквилле, Австралия. В третьем квартале 2002 года Компания определила, что некоторые материальные и нематериальные активы, связанные с Reporcin, были обесценены, и отразила расходы до налогообложения в размере 37,1 млн.
По состоянию на 31 декабря 2002 г. общая сумма дополнительных платежей в размере приблизительно 35,0 млн. долл. США требуется в течение следующих четырех лет, если будут получены все семь возможных одобрений страны. В соответствии с условиями соглашения, Компания должна была завершить производство Репорцина, одобренное FDA. Чтобы выполнить это требование, в июне 2000 г. Компания приобрела биофармацевтическое производственное предприятие в Терре-Хот, штат Индиана, и начала подготовку предприятия для производства репорцина. В связи с переоценкой подхода Компании к У.S. рынок для Reporcin, объект, на который Компания потратила 12 миллионов долларов, не был завершен, и Компания объявила о своем намерении продать этот объект в 2003 году. Кроме того, из-за избыточных запасов Reporcin, Компания решила прекратить производство на своем предприятии в Парквилле, Австралия. В третьем квартале 2002 года Компания определила, что некоторые материальные и нематериальные активы, связанные с Reporcin, были обесценены, и отразила расходы до налогообложения в размере 37,1 млн. долларов США. В рамках своей переоценки Компания намерена изучить возможности платного производства в США.S. и продолжить получение одобрения регулирующих органов для Reporcin в США
долларов США. В рамках своей переоценки Компания намерена изучить возможности платного производства в США.S. и продолжить получение одобрения регулирующих органов для Reporcin в США
В мае 2000 года Компания приобрела бизнес Roche MFA примерно за 288,0 миллионов долларов США. Бизнес Roche MFA состоял из таких продуктов, как Aureomycin, Bovatec, Avatec, Bio-Cox и Cygro. Эти фармацевтические препараты используются для профилактики и лечения заболеваний скота и птицы.
Помещения. Компания производит свою продукцию для здоровья животных на нескольких производственных предприятиях. BMD производится и смешивается на заводе компании в Чикаго-Хайтс, штат Иллинойс, который включает в себя современный завод по ферментации и восстановлению.Albac производится на заводе в Осло, который используется совместно с HPI. Растворимые антибиотики и витамины производятся на предприятии AH в Лонгмонте, штат Колорадо, а кормовой хлортетрациклин производится на предприятии AH в Уиллоу-Айленд, Западная Вирджиния, в дополнение к закупкам у иностранных поставщиков. Затем его смешивают на независимых предприятиях по смешиванию. Bio-Cox смешивается на предприятии AH в Ван Бурене, штат Арканзас, а Avatec и Bovatec смешиваются на предприятии в Солсбери, штат Мэриленд. Линейка продуктов 3-Nitro производится по технологии Компании на стороннем предприятии.В 2002 году компания начала производство тестовых партий ласалоцида на своем предприятии в Уиллоу-Айленд. Декохинат, активный ингредиент, используемый в Deccox, производится в соответствии с соглашением, срок действия которого истекает в 2012 году, с использованием технологии Компании на предприятии, которым владеет и управляет третье лицо. Смешивание Deccox производится на предприятии компании в Лоуэлле, штат Арканзас (до июня 2003 г.), а также на предприятии третьей стороны. Исследования и разработки продуктов проводятся на предприятиях AH в Чикаго-Хайтс, Уиллоу-Айленд и Осло.Компания производит рыбные вакцины на своем предприятии в Оверхалле, Норвегия, и на сторонних предприятиях, а также использует контрактное производство для обеспечения определенным сырьем для производства вакцин.
Затем его смешивают на независимых предприятиях по смешиванию. Bio-Cox смешивается на предприятии AH в Ван Бурене, штат Арканзас, а Avatec и Bovatec смешиваются на предприятии в Солсбери, штат Мэриленд. Линейка продуктов 3-Nitro производится по технологии Компании на стороннем предприятии.В 2002 году компания начала производство тестовых партий ласалоцида на своем предприятии в Уиллоу-Айленд. Декохинат, активный ингредиент, используемый в Deccox, производится в соответствии с соглашением, срок действия которого истекает в 2012 году, с использованием технологии Компании на предприятии, которым владеет и управляет третье лицо. Смешивание Deccox производится на предприятии компании в Лоуэлле, штат Арканзас (до июня 2003 г.), а также на предприятии третьей стороны. Исследования и разработки продуктов проводятся на предприятиях AH в Чикаго-Хайтс, Уиллоу-Айленд и Осло.Компания производит рыбные вакцины на своем предприятии в Оверхалле, Норвегия, и на сторонних предприятиях, а также использует контрактное производство для обеспечения определенным сырьем для производства вакцин. Компания объявила, что закроет свои предприятия в Ганнибале, Миссури, Лоуэлле, Арканзасе, Парквилле, Австралия, и Райтстауне, Нью-Джерси. Продукция, производимая в настоящее время на этих предприятиях, будет поставляться другими предприятиями Компании или третьими сторонами, если это необходимо.
Компания объявила, что закроет свои предприятия в Ганнибале, Миссури, Лоуэлле, Арканзасе, Парквилле, Австралия, и Райтстауне, Нью-Джерси. Продукция, производимая в настоящее время на этих предприятиях, будет поставляться другими предприятиями Компании или третьими сторонами, если это необходимо.
Конкурс.Компания конкурирует в этом высококонкурентном, чувствительном к цене бизнесе на основе цены, торговой марки и обслуживания клиентов. Некоторые из конкурентов Компании в индустрии здоровья животных предлагают широкий спектр продуктов с различными терапевтическими и производственными качествами. Благодаря сильной позиции Компании на рынке кормовых добавок и ее опыту в получении необходимых разрешений FDA на комбинированную терапию, Компания считает, что она обладает конкурентным преимуществом в коммерциализации одобренных FDA комбинированных лечебных кормовых добавок для животных.Тем не менее, нет никаких гарантий того, что третьи стороны будут продолжать сотрудничество в поисках одобрения комбинаций продуктов Компании, и Компания ожидает появления новых участников на рынке непатентованных лекарственных кормовых добавок в 2003 году.
Географические рынки. Компания продает большую часть своей продукции для здоровья животных в США. С добавлением бизнеса Roche MFA AH расширила свое международное присутствие. Компания продает свои продукты для здоровья водных животных в Норвегии, Великобритании, Ю.С., Чили и другие международные рынки.
Продажа и распространение. Товары компании для здоровья животных в США, Европе, Канаде, Мексике, Бразилии, Австралии и на других отдельных рынках продаются через штат из 141 технически подготовленного сотрудника по продажам и обслуживанию, многие из которых являются ветеринарами и диетологами. Компания имеет офисы продаж в США, Канаде, Мексике, Чили, Аргентине, Таиланде, Китае, Бразилии, Франции, Бельгии, Великобритании и Австралии. В остальном мире продукция AH продается в основном через дистрибьюторов и торговые компании.В январе 1999 года Компания объединила свою полностью принадлежащую ей дистрибьюторскую компанию в США с двумя аналогичными сторонними дистрибьюторскими компаниями, чтобы сформировать совместное предприятие, на 50% принадлежащее Компании.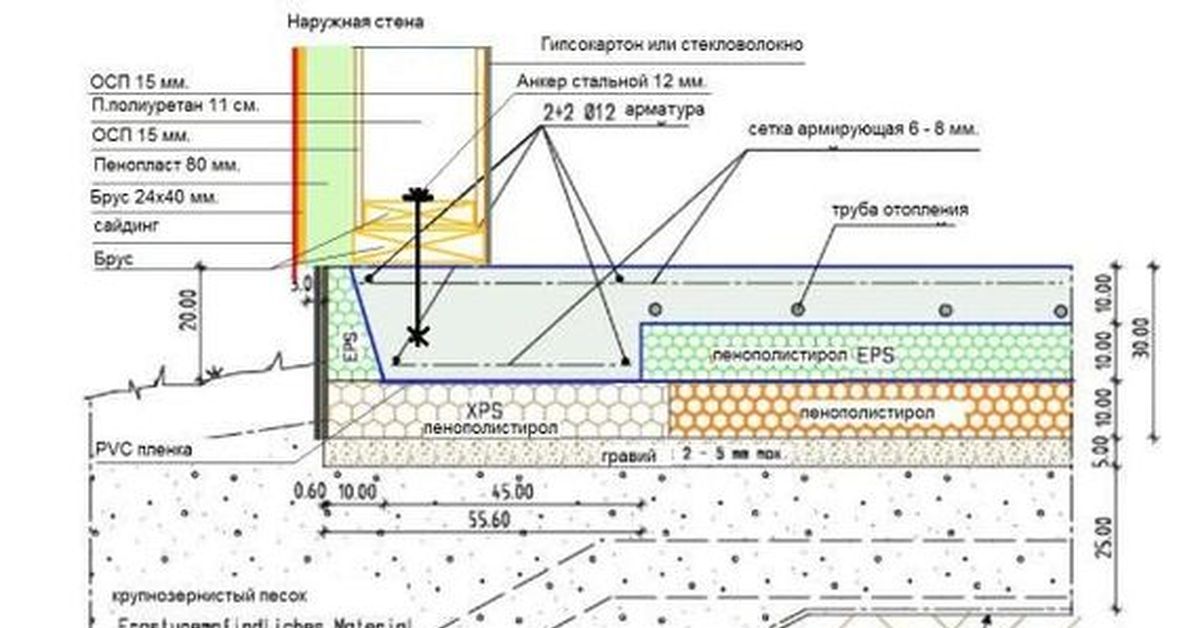 Совместное предприятие является региональным дистрибьютором товаров для здоровья животных в Центральном, Юго-Западном и Восточном регионах США. Компания продает свои товары для здоровья водных животных через собственный технически подготовленный торговый персонал в Норвегии, Великобритании и Чили, а также через дистрибьюторов в других странах. рынки.
Совместное предприятие является региональным дистрибьютором товаров для здоровья животных в Центральном, Юго-Западном и Восточном регионах США. Компания продает свои товары для здоровья водных животных через собственный технически подготовленный торговый персонал в Норвегии, Великобритании и Чили, а также через дистрибьюторов в других странах. рынки.
Клиенты.Продажи осуществляются в основном коммерческим производителям кормов для животных, оптовым торговцам и интегрированным производителям крупного рогатого скота, свиней и птицы. Хотя AH не зависит ни от одного клиента, клиентская база продуктов AH находится в стадии консолидации. Таким образом, по мере продолжения консолидации Компания может стать более зависимой от отдельных клиентов, поскольку эти клиенты увеличивают свой размер и долю рынка. Компания продает свои продукты для здоровья водных животных рыбным хозяйствам, как правило, по контракту, который продлевается как минимум на один вегетационный период. Относительно мало покупателей продукции Компании для здоровья водных животных и относительно мало поставщиков продукции, которую Компания продает на этом рынке.
Относительно мало покупателей продукции Компании для здоровья водных животных и относительно мало поставщиков продукции, которую Компания продает на этом рынке.
Информация, применимая ко всем бизнес-сегментам
Исследования, разработка продуктов и техническая деятельность
Научные разработки важны для каждого из бизнес-сегментов Компании. Исследования, разработка продуктов и техническая деятельность компании в сфере генерических фармацевтических препаратов для человека, которая в основном осуществляется в США.S., сосредоточьтесь на разработке непатентованных эквивалентов известных запатентованных продуктов, а также на открытии новых способов лечения существующих лекарств. Такие исследования, разработка продуктов и техническая деятельность также сосредоточены на разработке запатентованных систем доставки лекарств, обходе патентов в США и улучшении существующих систем доставки, упаковки и технологий производства. Подразделение API компании занимается исследованиями и разработками в области технологий химического синтеза, ферментации и очистки в Норвегии и Дании.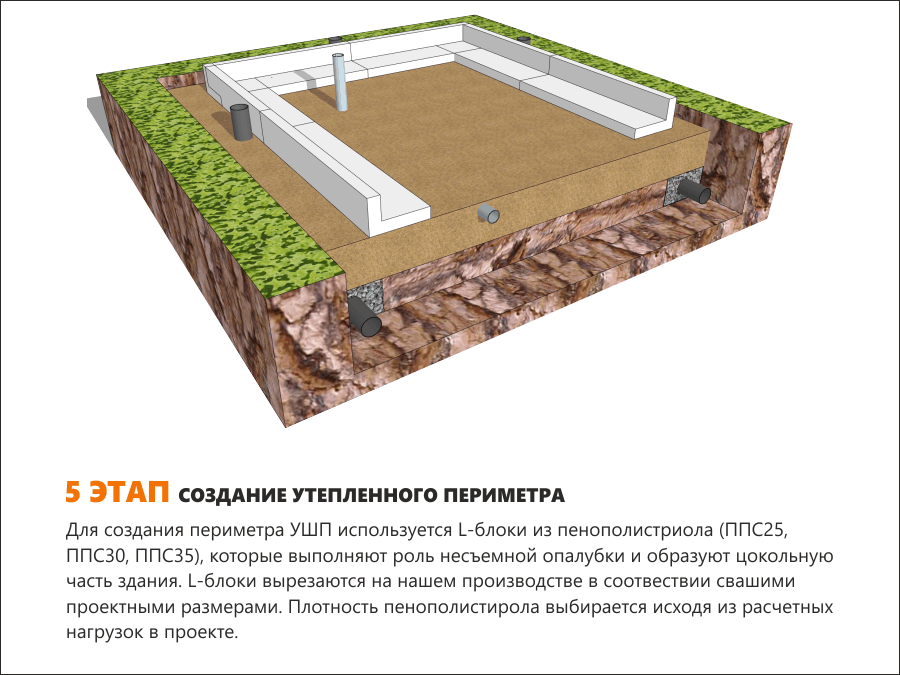
Возможности компании в области исследований и разработок были усилены и расширены в результате приобретения Фолдинга, что укрепило ее возможности по внедрению новых продуктов и ее опыт в области продуктов с пролонгированным высвобождением, а также разработки и производства пероральных твердых дозированных продуктов. Принимая во внимание значительные средства, которые обычно требуются для разработки новых химических препаратов, Компания не планирует предпринимать значительных действий в этой области.
Деятельность Компании по технической разработке фармацевтических препаратов для животных ранее включала обширную разработку и тестирование продуктов с основной целью обеспечения клинической поддержки новых продуктов и дополнительных применений для вариантов существующих продуктов и получения соответствующих разрешений FDA и других государственных органов.В 2003 г. Компания сосредоточила свои расходы на разработку продуктов AH на таких мероприятиях, как лицензирование и совместная разработка технологий в рамках договоренностей с третьими сторонами.
Учитывая глобальное присутствие Компании и ее внимание к исследованиям и разработкам, Компания стремится:
- сократить циклы разработки продуктов для внедрения и утверждения аналогичных продуктов на географических рынках посредством обмена знаниями в рамках своих глобальных исследований и разработок. ; и
- извлекают выгоду из глобальной функции исследований и разработок в области фармацевтики человека, чтобы быть более эффективными в масштабах исследовательской деятельности, включая распределение затрат на исследования и разработки, производство и закупки на глобальной платформе.
Как правило, исследования и разработки проводятся на основе бизнес-сегментов. Соответственно, после объединения трех бизнес-сегментов Компании в два сегмента исследования и разработки будут проводиться на основе двух сегментов. Компания осуществляет свою деятельность по разработке технических продуктов на своих объектах в Осло, Норвегия; Балтимор, Мэриленд; Остров Уиллоу, Западная Вирджиния; Чикаго-Хайтс, Иллинойс и Элизабет, Нью-Джерси, а также через независимые исследовательские центры в США. С. и Европе. Завод в Копенгагене используется для исследований и разработок API. В 2001 году компания закрыла свои исследования и разработки готовой продукции в Копенгагене, Дания. Компания находится в процессе закрытия своего предприятия в Райтстауне, штат Нью-Джерси.
С. и Европе. Завод в Копенгагене используется для исследований и разработок API. В 2001 году компания закрыла свои исследования и разработки готовой продукции в Копенгагене, Дания. Компания находится в процессе закрытия своего предприятия в Райтстауне, штат Нью-Джерси.
Расходы на исследования и разработки (без учета судебных издержек) составили примерно 67,1 млн долларов, 86,7 млн долларов и 43,3 млн долларов в 2002, 2001 и 2000 годах соответственно. Расходы 2001 года включают расходы на приобретение незавершенных исследований и разработок в размере 37 долл. США.7 миллионов, связанных с приобретением Faulding.
Исследования и разработки по своей сути носят спекулятивный характер. Деньги, потраченные на исследования и разработки, не всегда приводят к успешной разработке продукта. Например, Компания иногда отзывает или отказывается от своих находящихся на рассмотрении ANDA, особенно если Компания определяет, что она не была первой компанией, подавшей заявку в параграфе IV на связанный препарат. Соответственно, не следует полагать, что потенциальные продукты, находящиеся в разработке Компании, будут успешно коммерциализированы.
Соответственно, не следует полагать, что потенциальные продукты, находящиеся в разработке Компании, будут успешно коммерциализированы.
Новая линейка продуктов
Компания считает, что у нее есть привлекательный портфель новых продуктов, которые она планирует представить в течение следующих нескольких лет. Одним из наиболее потенциально значимых из этих продуктов является генерическая форма габапентина USHP. Габапентин — это генерическая версия нейронтина, препарата, предназначенного для лечения эпилепсии, продажи которого в 2002 году превысили 2,0 миллиарда долларов. В январе 2003 года Компания получила подтверждение от FDA, что Purepac был первым производителем дженериков, подавшим заявку на сертификацию по параграфу IV, оспаривающую патенты, защищающие капсулы Neurontin.Будучи первой организацией, подавшей сертификацию по параграфу IV в отношении основных действующих патентов на габапентин, Компания имеет возможность пользоваться эксклюзивными правами на рынке дженериков на срок до шести месяцев. Эксклюзивность предоставляется при условии получения всех необходимых разрешений FDA и удовлетворительного разрешения судебного разбирательства со стороны компании-бренда в начале периода эксклюзивности. Компания может не при всех обстоятельствах быть в состоянии контролировать начало периода эксклюзивности и, следовательно, не может гарантировать, что она получит выгоду от того, что она первой подаст сертификат параграфа IV.Если Компания получит это исключительное право на основе результатов запуска аналогичных непатентованных продуктов в прошлом, Компания полагает, что она может разумно ожидать значительную первоначальную долю рынка (до 25-50% рынка брендов в натуральном выражении) и такие первоначальные продажи также должны помочь Компании сохранить меньшую, но ведущую долю рынка после периода эксклюзивности. Однако Компания не может гарантировать, что она достигнет этих результатов. (См. «Факторы риска» и «Судебные разбирательства — Габапентин».)
Эксклюзивность предоставляется при условии получения всех необходимых разрешений FDA и удовлетворительного разрешения судебного разбирательства со стороны компании-бренда в начале периода эксклюзивности. Компания может не при всех обстоятельствах быть в состоянии контролировать начало периода эксклюзивности и, следовательно, не может гарантировать, что она получит выгоду от того, что она первой подаст сертификат параграфа IV.Если Компания получит это исключительное право на основе результатов запуска аналогичных непатентованных продуктов в прошлом, Компания полагает, что она может разумно ожидать значительную первоначальную долю рынка (до 25-50% рынка брендов в натуральном выражении) и такие первоначальные продажи также должны помочь Компании сохранить меньшую, но ведущую долю рынка после периода эксклюзивности. Однако Компания не может гарантировать, что она достигнет этих результатов. (См. «Факторы риска» и «Судебные разбирательства — Габапентин».)
Постановление правительства
Общие. Исследования, разработка, производство и маркетинг лекарственных препаратов компании для человека и продуктов для здоровья животных подлежат широкому государственному регулированию со стороны FDA или Министерства сельского хозяйства США, а также Управления по борьбе с наркотиками, Федеральной торговой комиссии, Управления безопасности потребительских товаров. Комиссией и другими государственными учреждениями, а также сопоставимыми органами в ЕС, Норвегии, Индонезии и других странах.Хотя Норвегия не является членом ЕС, она является членом Европейской экономической зоны и, как таковая, приняла все правила ЕС в отношении фармацевтических препаратов, за исключением кормовых антибиотиков. Государственное регулирование включает в себя детальную проверку и контроль за тестированием, производством, безопасностью, эффективностью, маркировкой, хранением, ведением учета, отчетностью, одобрением, рекламой, продвижением, продажей и распространением фармацевтической продукции. Несоблюдение применимых требований может привести к письмам-предупреждениям, гражданским или уголовным штрафам, действиям, включая судебное преследование, отзыв или конфискацию продуктов, судебные запреты, полную или частичную приостановку производства и распространения, приостановку или отзыв разрешений на продукцию, отстранение Компании или запрет на получение новых разрешений на лекарства или оказание услуг фармацевтическим компаниям в любом качестве, отказ правительства одобрять новые продукты или покупать продукты Компании и уголовное преследование.
Исследования, разработка, производство и маркетинг лекарственных препаратов компании для человека и продуктов для здоровья животных подлежат широкому государственному регулированию со стороны FDA или Министерства сельского хозяйства США, а также Управления по борьбе с наркотиками, Федеральной торговой комиссии, Управления безопасности потребительских товаров. Комиссией и другими государственными учреждениями, а также сопоставимыми органами в ЕС, Норвегии, Индонезии и других странах.Хотя Норвегия не является членом ЕС, она является членом Европейской экономической зоны и, как таковая, приняла все правила ЕС в отношении фармацевтических препаратов, за исключением кормовых антибиотиков. Государственное регулирование включает в себя детальную проверку и контроль за тестированием, производством, безопасностью, эффективностью, маркировкой, хранением, ведением учета, отчетностью, одобрением, рекламой, продвижением, продажей и распространением фармацевтической продукции. Несоблюдение применимых требований может привести к письмам-предупреждениям, гражданским или уголовным штрафам, действиям, включая судебное преследование, отзыв или конфискацию продуктов, судебные запреты, полную или частичную приостановку производства и распространения, приостановку или отзыв разрешений на продукцию, отстранение Компании или запрет на получение новых разрешений на лекарства или оказание услуг фармацевтическим компаниям в любом качестве, отказ правительства одобрять новые продукты или покупать продукты Компании и уголовное преследование. Стоимость соблюдения государственных постановлений существенно увеличивает стоимость производства продукции Компании.
Стоимость соблюдения государственных постановлений существенно увеличивает стоимость производства продукции Компании.
Меняющийся и сложный характер нормативных требований (включая возможность будущих изменений в законах или правилах), широкие полномочия и свобода действий FDA и аналогичных государственных и иностранных агентств, а также в целом высокий уровень регулирующего надзора приводят к постоянному вероятность того, что время от времени Компания будет подвергаться негативному влиянию со стороны регулирующих органов, несмотря на усилия Компании по достижению и поддержанию полного соблюдения всех нормативных требований.В результате действий, предпринятых Компанией в ответ на все более строгую нормативную среду, в которой работает Компания, Компания потратила и будет продолжать тратить значительные средства и время руководства на соблюдение нормативных требований.
Управление по маркетингу продукции. В США процедура регулирования FDA, обычно применимая к непатентованным фармацевтическим продуктам для человека, зависит от того, является ли фирменное лекарство, эквивалентным или сопоставимым с которым является непатентованная версия:
- предметом утвержденной заявки на новое лекарственное средство или NDA, которая имеет были проверены как на безопасность, так и на эффективность;
- , продаваемый в соответствии с NDA до 1962 г.
 , проверенным только на предмет безопасности;
, проверенным только на предмет безопасности; - продается без NDA; или
- , продаваемый в соответствии с программой безрецептурных монографий.
Если предлагаемый препарат представляет собой непатентованную вариацию фирменного продукта, являющегося предметом NDA, утвержденного как с точки зрения безопасности, так и с точки зрения эффективности, непатентованный продукт должен быть предметом сокращенной заявки на новый лекарственный препарат, или ANDA, и быть одобрены FDA до выхода на рынок. Лекарственные препараты, являющиеся непатентованными копиями других типов фирменных продуктов, как правило, могут продаваться в соответствии либо с политикой соблюдения требований FDA, либо с программой фармацевтики, отпускаемой без рецепта, в которой описаны активные ингредиенты и маркированные способы применения, признанные FDA безопасными и эффективными. не требуют одобрения NDA и, как правило, не подлежат регистрации и утверждению ANDA до выхода на рынок в настоящее время. Хотя Компания считает, что текущие фармацевтические продукты Компании должным образом продаются в соответствии с применимой процедурой FDA или действующей политикой правоприменения, основа для сбыта продуктов, не подпадающих под действие утвержденных ANDA, может быть изменена или отозвана FDA. Статус всех продуктов также может быть изменен, если опыт выявляет существенную новую неблагоприятную информацию.
Хотя Компания считает, что текущие фармацевтические продукты Компании должным образом продаются в соответствии с применимой процедурой FDA или действующей политикой правоприменения, основа для сбыта продуктов, не подпадающих под действие утвержденных ANDA, может быть изменена или отозвана FDA. Статус всех продуктов также может быть изменен, если опыт выявляет существенную новую неблагоприятную информацию.
Все заявки на одобрение регулирующими органами непатентованных лекарственных препаратов, на которые распространяются требования ANDA, должны содержать данные, касающиеся состава продукта, поставщиков сырья, стабильности, производства, упаковки, маркировки и контроля качества, а также другую информацию.ANDA также должны содержать данные, демонстрирующие биоэквивалентность непатентованного лекарственного средства фирменному лекарственному средству. Каждое одобрение продукта ограничивает производство определенным сайтом или сайтами. Дополнительные заявки, разрешающие производство продукции на новых площадках, также обычно требуют рассмотрения и утверждения. Кроме того, определенные изменения в нашем производственном процессе, ингредиентах лекарств и маркировке также могут потребовать рассмотрения и одобрения регулирующими органами. Утверждения новых продуктов или разрешения на изменение продуктов могут быть получены несвоевременно, если вообще будут получены.Неполучение этих разрешений или их получение в срок может оказать существенное негативное влияние на деятельность, финансовое положение и результаты деятельности Компании.
Кроме того, определенные изменения в нашем производственном процессе, ингредиентах лекарств и маркировке также могут потребовать рассмотрения и одобрения регулирующими органами. Утверждения новых продуктов или разрешения на изменение продуктов могут быть получены несвоевременно, если вообще будут получены.Неполучение этих разрешений или их получение в срок может оказать существенное негативное влияние на деятельность, финансовое положение и результаты деятельности Компании.
Некоторые фармацевтические препараты для животных компании регулируются FDA, как и лекарственные препараты для людей, в то время как другие фармацевтические препараты для животных регулируются Министерством сельского хозяйства США. Хотя Компания продает некоторые непатентованные лекарственные препараты для животных, на которые распространяются аналогичные требования FDA, применимые к ее непатентованным фармацевтическим продуктам для человека, многие из ее фармацевтических препаратов для животных считаются фирменными или новаторскими лекарственными препаратами для животных. Как и их аналоги для людей, для препаратов для животных, а также для любых изменений в заявлениях на этикетке, спецификациях или производственных площадках, которые происходят после утверждения, требуется предварительное одобрение FDA в соответствии со строгими правилами FDA для их тестирования, разработки и производства. Огромное количество заявок, ожидающих рассмотрения в Центре ветеринарной медицины FDA, затрудняет прогнозирование сроков таких разрешений. Несмотря на трудности и задержки, вызванные этой ситуацией, Компании удалось получить такие разрешения.Как и в случае с фармацевтическими препаратами для людей, к продуктам компании для здоровья животных применяются требования FDA по проверке и ведению учета, а также положения о запрещении производства.
Как и их аналоги для людей, для препаратов для животных, а также для любых изменений в заявлениях на этикетке, спецификациях или производственных площадках, которые происходят после утверждения, требуется предварительное одобрение FDA в соответствии со строгими правилами FDA для их тестирования, разработки и производства. Огромное количество заявок, ожидающих рассмотрения в Центре ветеринарной медицины FDA, затрудняет прогнозирование сроков таких разрешений. Несмотря на трудности и задержки, вызванные этой ситуацией, Компании удалось получить такие разрешения.Как и в случае с фармацевтическими препаратами для людей, к продуктам компании для здоровья животных применяются требования FDA по проверке и ведению учета, а также положения о запрещении производства.
Время от времени в Конгресс США вносятся законодательные законопроекты, некоторые из которых в случае принятия могут оказать неблагоприятное влияние на бизнес AH. Однако в прошлом такие законопроекты, которые могли иметь существенные негативные последствия, не имели достаточной поддержки, чтобы стать законом. Фармацевтическая отрасль для животных активно участвует в законодательном процессе.Чтобы справиться с ранее упомянутым отставанием в рассмотрении, отрасль поддерживает законодательство, согласно которому будут приняты сборы с пользователей и стандарты эффективности, аналогичные тем, которые действуют для новых лекарств для людей и медицинских устройств.
Фармацевтическая отрасль для животных активно участвует в законодательном процессе.Чтобы справиться с ранее упомянутым отставанием в рассмотрении, отрасль поддерживает законодательство, согласно которому будут приняты сборы с пользователей и стандарты эффективности, аналогичные тем, которые действуют для новых лекарств для людей и медицинских устройств.
Законодательство ЕС требует, чтобы медицинские продукты для человека должны были получить разрешение на продажу, прежде чем они будут размещены на рынке в ЕС. Критериями, по которым оценивается выдача разрешения, являются качество, безопасность и эффективность. Демонстрация безопасности и эффективности, в частности, требует проведения клинических испытаний на людях, которые подпадают под действие стандартов, кодифицированных в руководстве ЕС по надлежащей клинической практике.Кроме того, законодательство ЕС требует, чтобы таким испытаниям предшествовали адекватные фармакологические и токсикологические испытания на животных, чтобы проводились испытания на стабильность, чтобы в клинических испытаниях использовались контроли и чтобы клинические испытания проводились двойным слепым методом и допускали статистический анализ. по возможности используя конкретные критерии, а не полагаясь на большой размер выборки. Рабочая группа Комитета по патентованным лекарственным средствам также дала различные рекомендации в этой области.Аналогичные разрешения правительства и ведомств также требуются в других странах, где Компания ведет бизнес. Не может быть никакой гарантии, что одобрение нового продукта будет получено своевременно, если вообще когда-либо. Неполучение этих разрешений или их получение в срок может оказать существенное негативное влияние на деятельность, финансовое положение и результаты деятельности Компании.
по возможности используя конкретные критерии, а не полагаясь на большой размер выборки. Рабочая группа Комитета по патентованным лекарственным средствам также дала различные рекомендации в этой области.Аналогичные разрешения правительства и ведомств также требуются в других странах, где Компания ведет бизнес. Не может быть никакой гарантии, что одобрение нового продукта будет получено своевременно, если вообще когда-либо. Неполучение этих разрешений или их получение в срок может оказать существенное негативное влияние на деятельность, финансовое положение и результаты деятельности Компании.
Аналогичные требования применяются к выдаче регистрационных удостоверений на лекарственные средства для ветеринарного применения в странах ЕС.
Непатентованные лекарственные препараты для людей и ветеринарии могут быть разрешены в ЕС посредством сокращенных заявок на получение разрешений. Например, заявки на регистрацию в ЕС не должны содержать результаты токсикологических и фармакологических тестов и результаты клинических испытаний при соблюдении определенных условий, в частности, если «оригинальное» лекарственное средство было разрешено в ЕС в течение как минимум шесть лет (а в некоторых случаях десять лет) и находится на рынке в государстве-члене, в котором была подана заявка на регистрационное удостоверение. Сокращенные заявки должны относиться к информации, содержащейся в досье «оригинального» продукта, для которого разрешение на продажу было предоставлено на основе полного досье. Исходное полное досье должно быть досье, находящимся в распоряжении соответствующего компетентного органа. Это означает, что сокращенные заявки должны подаваться в органы, которые фактически владеют досье на «оригинальный» продукт. Упомянутый «оригинальный» продукт должен быть разрешен на момент подачи сокращенной заявки.Для включения в сокращенные досье продукт должен рассматриваться как «по существу аналогичный» оригинальному лекарственному средству. В ЕС нет определения этого «по существу аналогичного» состояния. Согласно толкованию Европейского Суда, лекарственное средство считается «по существу подобным» оригинальному лекарственному средству, если оно имеет такой же качественный и количественный состав с точки зрения активных начал/веществ, ту же лекарственную форму и является биоэквивалентным, если только оно не В свете научных знаний очевидно, что он значительно отличается от оригинального продукта в отношении безопасности или эффективности.
Сокращенные заявки должны относиться к информации, содержащейся в досье «оригинального» продукта, для которого разрешение на продажу было предоставлено на основе полного досье. Исходное полное досье должно быть досье, находящимся в распоряжении соответствующего компетентного органа. Это означает, что сокращенные заявки должны подаваться в органы, которые фактически владеют досье на «оригинальный» продукт. Упомянутый «оригинальный» продукт должен быть разрешен на момент подачи сокращенной заявки.Для включения в сокращенные досье продукт должен рассматриваться как «по существу аналогичный» оригинальному лекарственному средству. В ЕС нет определения этого «по существу аналогичного» состояния. Согласно толкованию Европейского Суда, лекарственное средство считается «по существу подобным» оригинальному лекарственному средству, если оно имеет такой же качественный и количественный состав с точки зрения активных начал/веществ, ту же лекарственную форму и является биоэквивалентным, если только оно не В свете научных знаний очевидно, что он значительно отличается от оригинального продукта в отношении безопасности или эффективности.
Многочисленные предложения по пересмотру законодательства ЕС находятся на рассмотрении. Эти предложения повлияют на регулирование лекарственных препаратов как для людей, так и для животных. На данный момент изменений в законодательство не вносилось. Компания не может предсказать, какие изменения будут реализованы, если таковые будут.
Европейский союз и пять стран, не входящих в ЕС, запретили использование четырех антибиотиков для стимулирования роста сельскохозяйственных животных с 1 июля 1999 г., и к 2006 г. этот запрет будет распространен на оставшиеся утвержденные антибиотики, стимулирующие рост.Хотя три из этих продуктов не производились и не продавались нами, под запрет подпадает бацитрацин цинк, стимулятор роста кормового антибиотика для скота и птицы, производимый нами. Попытка Компании отменить или ограничить запрет ЕС, который затрагивает продукт Albac Компании, не увенчалась успехом и не была обжалована. Аналогичные действия по запрету или строгому ограничению использования антибиотиков у животных были предприняты или рассматриваются торговыми партнерами ЕС. (См. «Факторы риска».)
(См. «Факторы риска».)
Требования аналогичны требованиям США.S. и ЕС применяются к выдаче разрешений на производство и продажу фармацевтических продуктов в Азии и Африке.
Соответствие объекта. Производственные операции Компании в США и три предприятия Компании в Европе, производящие продукцию для экспорта в США, должны соответствовать действующим правилам надлежащей производственной практики FDA («cGMP»). cGMP охватывает все аспекты производственного процесса, включая проверку и ведение документации, в дополнение к стандартам для помещений, оборудования и персонала, и включает в себя изменение и развитие стандартов.Следовательно, постоянное соблюдение cGMP может быть особенно сложной и дорогостоящей частью соблюдения нормативных требований. Подобные правила cGMP действуют и в других странах, где Компания имеет производственные операции. ЕС требует, чтобы перед производством и сборкой лекарственного средства каждая компания, выполняющая такую операцию, имела лицензию производителя, лицензия на продукт должна быть у лица, ответственного за состав продукта, а производство и сборка должны соответствовать лицензии на продукт и надлежащей производственной практике.
Компания находится под постоянным контролем и периодическими проверками FDA. В течение 2001 и 2002 гг. Компания получила существенные уведомления об инспекционных наблюдениях («Отчеты 483») от FDA для своего объекта USHP в Балтиморе. Что касается объекта USHP в Элизабет, Компания получила письмо с предупреждением от FDA в 2001 г. и отчет 483 от FDA в 2003 г. Компания считает, что вопросы, поднятые в письме с предупреждением, были должным образом решены, поскольку никаких дополнительных комментариев получено не было. от FDA в ходе последующей проверки.В отчете 483 перечислены предполагаемые отклонения от требований cGMP. По оценкам Компании, стоимость устранения отклонений, перечисленных в этих отчетах 483, составит приблизительно 38 миллионов долларов США. (См. «Факторы риска» и «Судебные разбирательства».) В прошлом Компания время от времени получала 483 отчета по другим заводам, все из которых, по мнению Компании, она рассмотрела должным образом.
Далее, что касается cGMP, в августе 2002 года FDA объявило о новой крупной инициативе по регулированию качества лекарственных препаратов под названием «CGMP для фармацевтических препаратов для 21 st века».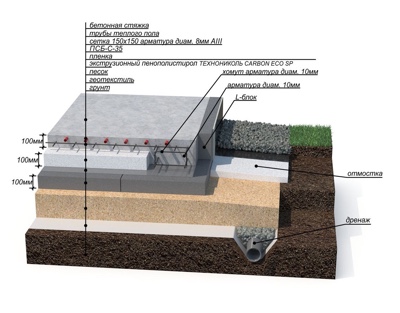 Двухлетняя программа предназначена, среди прочего, для обеспечения того, чтобы политика нормативного контроля и инспекции основывалась на передовых достижениях фармацевтической науки, а также для поощрения внедрения новых технологических достижений в фармацевтической промышленности. Будут реализованы подходы, которые сосредоточат внимание как промышленности, так и FDA на критических областях
Двухлетняя программа предназначена, среди прочего, для обеспечения того, чтобы политика нормативного контроля и инспекции основывалась на передовых достижениях фармацевтической науки, а также для поощрения внедрения новых технологических достижений в фармацевтической промышленности. Будут реализованы подходы, которые сосредоточат внимание как промышленности, так и FDA на критических областях
Потенциальная ответственность за текущую продукцию. промышленности, государственных органов и др.Эти исследования, в которых все чаще используются сложные методы и приемы, могут поставить под сомнение использование, безопасность и эффективность ранее продаваемых продуктов и в некоторых случаях привели и могут привести в будущем к прекращению их продажи, а в некоторых странах дать подавать иски о возмещении ущерба от лиц, которые считают, что им причинен вред в результате их использования.
Расширенная защита для определенных продуктов. В 1984 году Закон Ваксмана-Хэтча внес поправки как в Патентный кодекс, так и в Федеральный закон о пищевых продуктах, лекарствах и косметике, более известный как Закон о FDC.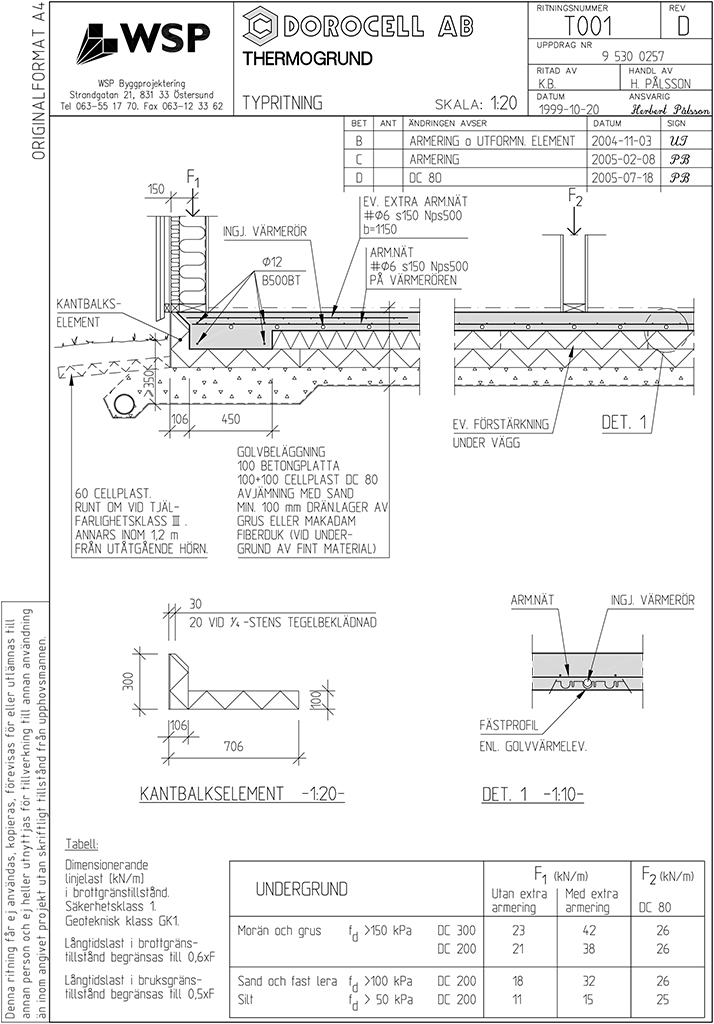 Закон Ваксмана-Хэтча кодифицировал и расширил процедуры подачи заявок на получение одобрения FDA на дженерики патентованных фармацевтических препаратов, которые не запатентованы или срок действия рыночных эксклюзивных прав которых истек. Закон Ваксмана-Хэтча также предусматривает положения о продлении срока действия патента и рыночных эксклюзивных правах для производителей инновационных лекарств, которые исключают представление или задерживают утверждение конкурирующего ANDA при определенных условиях. Одно из таких положений предусматривает пятилетний период исключительного права на рынке для NDA, включающих новые химические вещества, и трехлетний период исключительного права на рынке для NDA или дополнений к NDA, содержащих новые клинические исследования, необходимые для утверждения такой заявки.Положения об исключительности рынка в равной степени применяются к запатентованным и непатентованным лекарственным препаратам. Другое положение разрешает продление срока действия патента на срок до пяти лет в качестве компенсации за некоторое сокращение фактического срока действия патента в результате времени, затраченного на тестирование и рассмотрение FDA заявки на одобрение лекарственного средства.
Закон Ваксмана-Хэтча кодифицировал и расширил процедуры подачи заявок на получение одобрения FDA на дженерики патентованных фармацевтических препаратов, которые не запатентованы или срок действия рыночных эксклюзивных прав которых истек. Закон Ваксмана-Хэтча также предусматривает положения о продлении срока действия патента и рыночных эксклюзивных правах для производителей инновационных лекарств, которые исключают представление или задерживают утверждение конкурирующего ANDA при определенных условиях. Одно из таких положений предусматривает пятилетний период исключительного права на рынке для NDA, включающих новые химические вещества, и трехлетний период исключительного права на рынке для NDA или дополнений к NDA, содержащих новые клинические исследования, необходимые для утверждения такой заявки.Положения об исключительности рынка в равной степени применяются к запатентованным и непатентованным лекарственным препаратам. Другое положение разрешает продление срока действия патента на срок до пяти лет в качестве компенсации за некоторое сокращение фактического срока действия патента в результате времени, затраченного на тестирование и рассмотрение FDA заявки на одобрение лекарственного средства. Срок действия патента также может быть продлен в соответствии с положениями Закона о соглашениях Уругвайского раунда или URAA. Кроме того, Закон о модернизации FDA от 1997 г. («FDAMA») позволяет производителям фирменных фармацевтических препаратов при определенных обстоятельствах добиваться шестимесячного дополнительного эксклюзивного права, если они провели педиатрические исследования препарата в соответствии с требованиями закона.Хотя положения об исключительности педиатрии в FDAMA предусматривали дату истечения срока действия 1 января 2002 г., они были повторно разрешены Законом о лучших лекарственных препаратах для детей, который был принят в январе 2002 г. оспаривание патента, указанного производителем фирменного наименования (т. е. ANDA, содержащего сертификат параграфа IV, в котором говорится, что непатентованный препарат не будет нарушать какой-либо из перечисленных патентов на эталонный препарат или что такой патент (патенты) является (являются) недействительными или не имеющими исковой силы ) может получить эксклюзивный период в 180 дней при определенных обстоятельствах, в течение которых другие общие заявки на продукт, содержащие сертификаты параграфа IV, не могут быть одобрены.
Срок действия патента также может быть продлен в соответствии с положениями Закона о соглашениях Уругвайского раунда или URAA. Кроме того, Закон о модернизации FDA от 1997 г. («FDAMA») позволяет производителям фирменных фармацевтических препаратов при определенных обстоятельствах добиваться шестимесячного дополнительного эксклюзивного права, если они провели педиатрические исследования препарата в соответствии с требованиями закона.Хотя положения об исключительности педиатрии в FDAMA предусматривали дату истечения срока действия 1 января 2002 г., они были повторно разрешены Законом о лучших лекарственных препаратах для детей, который был принят в январе 2002 г. оспаривание патента, указанного производителем фирменного наименования (т. е. ANDA, содержащего сертификат параграфа IV, в котором говорится, что непатентованный препарат не будет нарушать какой-либо из перечисленных патентов на эталонный препарат или что такой патент (патенты) является (являются) недействительными или не имеющими исковой силы ) может получить эксклюзивный период в 180 дней при определенных обстоятельствах, в течение которых другие общие заявки на продукт, содержащие сертификаты параграфа IV, не могут быть одобрены.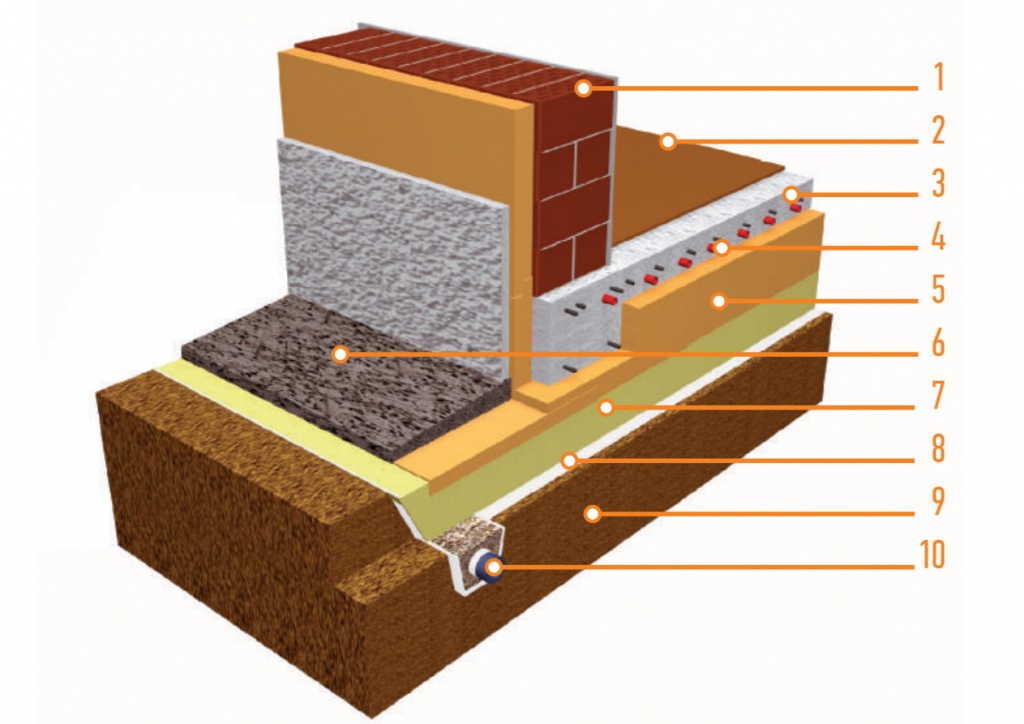 Таким образом, Компания не может предсказать, в какой степени Закон Ваксмана-Хэтча, Закон о лучших лекарственных препаратах для детей, FDAMA или URAA могут отсрочить утверждение некоторых новых продуктов Компании. Кроме того, со временем могут произойти изменения в уставах или правилах. Компания не может предсказать, в какой степени любые такие будущие изменения могут повлиять на ее продукты или разработку продуктов.
Таким образом, Компания не может предсказать, в какой степени Закон Ваксмана-Хэтча, Закон о лучших лекарственных препаратах для детей, FDAMA или URAA могут отсрочить утверждение некоторых новых продуктов Компании. Кроме того, со временем могут произойти изменения в уставах или правилах. Компания не может предсказать, в какой степени любые такие будущие изменения могут повлиять на ее продукты или разработку продуктов.
В Европе некоторые Директивы предоставляют аналогичные исключительные права на рынке в отношении запатентованных лекарственных средств, независимо от какой-либо патентной защиты.Прежде чем производитель дженерика сможет подать сокращенную заявку на получение регистрационного удостоверения (как указано выше), он, как правило, должен подождать, пока оригинальный запатентованный препарат не появится на рынке в течение определенного периода времени, если только у него нет согласия лица, подавшего оригинал. тестовые данные для первого регистрационного удостоверения или могут самостоятельно составить адекватное досье.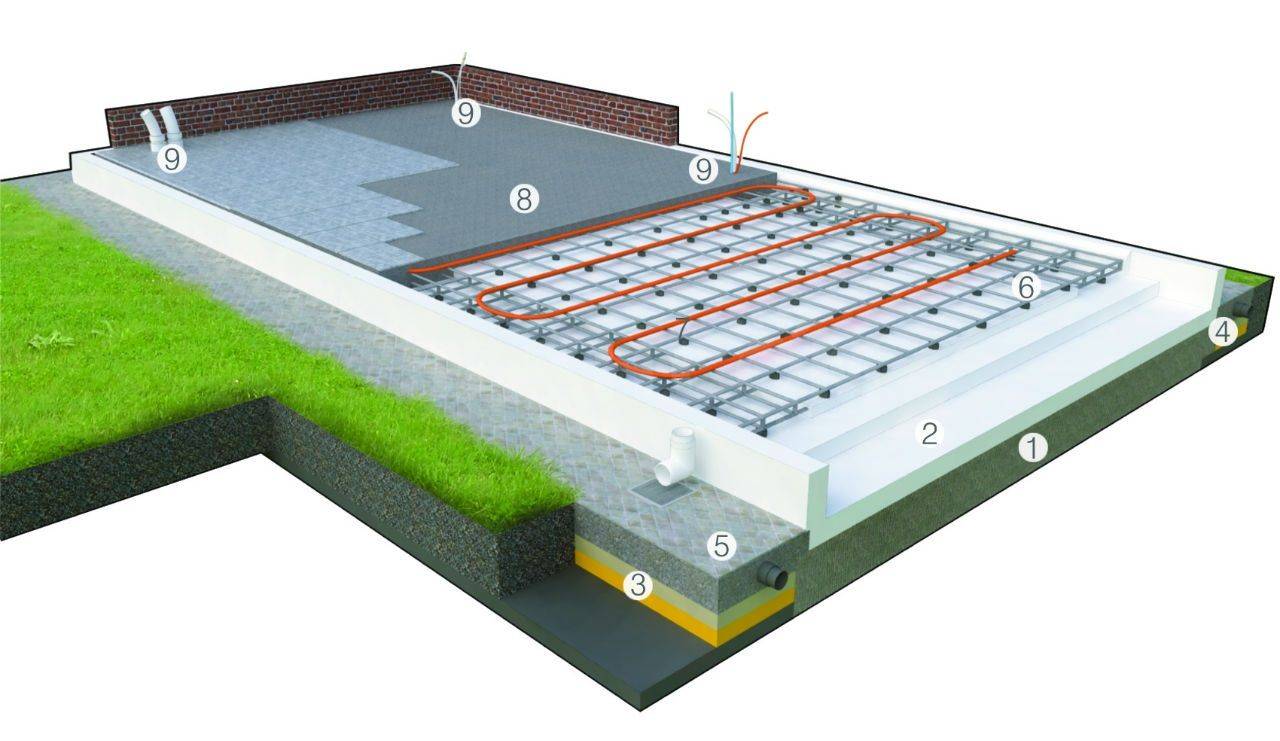 В случае высокотехнологичных продуктов этот период составляет десять лет, а в некоторых штатах для других лекарственных средств — шесть лет, при условии, что государства-члены могут выбрать десятилетний период исключительности в отношении всех продуктов.
В случае высокотехнологичных продуктов этот период составляет десять лет, а в некоторых штатах для других лекарственных средств — шесть лет, при условии, что государства-члены могут выбрать десятилетний период исключительности в отношении всех продуктов.
В дополнение к периоду эксклюзивности в ЕС также возможно продлить срок патентной защиты продукта, имеющего регистрационное удостоверение, посредством сертификата дополнительной охраны или SPC. SPC вступает в силу по истечении срока действия соответствующего патента и действует в течение периода, исчисляемого с учетом задержки между подачей заявки на патент и выдачей первого регистрационного удостоверения на лекарство. Этот период защиты, который составляет не более пяти лет, еще больше задерживает выход на рынок непатентованных лекарственных средств.
Общий закон о борьбе с наркотиками. Общий закон о борьбе с наркотиками от 1992 г., внесший поправки в Закон о FDC, дает FDA шесть способов наказывать компании, совершающие правонарушения в связи с разработкой или утверждением ANDA. FDA может:
FDA может:
- навсегда или временно запретить правонарушителям подавать или помогать в подаче ANDA;
- временно отказать в одобрении или приостановить подачу заявок на продажу определенных непатентованных лекарств;
- приостановить распространение всех лекарств, одобренных или разработанных в соответствии с ANDA такого лица;
- отозвать одобрение ANDA;
- требовать гражданской ответственности против предполагаемого правонарушителя; и
- в соответствии с соответствующими процедурами, значительно задерживают одобрение любого ожидаемого ANDA от такого лица.
Компания никогда не подвергалась принудительным действиям в соответствии с настоящим законом, но нет никаких гарантий, что ограничения или штрафы не будут наложены на Компанию в будущем.
Закон о контролируемых веществах. Компания также производит и продает лекарственные препараты, которые являются «контролируемыми веществами» в соответствии с определением в Законе о контролируемых веществах, который устанавливает определенные требования к персоналу службы безопасности, отчетности, ведению учета и импорту и экспорту, администрируемые Управлением по борьбе с наркотиками или DEA, подразделением Министерство юстиции. Компания зарегистрирована DEA для производства и распространения определенных контролируемых веществ. У DEA двойная миссия: правоохранительная и регулирующая. Первый касается контроля за веществами, вызывающими злоупотребление, а также за оборудованием и сырьем, используемым для их производства. Управление по борьбе с наркотиками разделяет правоприменительные полномочия с Федеральным бюро расследований, еще одним подразделением Министерства юстиции. Регуляторные обязанности DEA связаны с контролем лицензированных лиц, занимающихся контролируемыми веществами, а также с самими веществами, оборудованием и сырьем, используемым при их производстве и упаковке, с целью предотвращения утечки таких предметов в каналы незаконной торговли.На Компанию не наложены какие-либо ограничения за несоблюдение вышеуказанных правил, но нет никаких гарантий, что ограничения или штрафы не будут наложены на Компанию в будущем.
Компания зарегистрирована DEA для производства и распространения определенных контролируемых веществ. У DEA двойная миссия: правоохранительная и регулирующая. Первый касается контроля за веществами, вызывающими злоупотребление, а также за оборудованием и сырьем, используемым для их производства. Управление по борьбе с наркотиками разделяет правоприменительные полномочия с Федеральным бюро расследований, еще одним подразделением Министерства юстиции. Регуляторные обязанности DEA связаны с контролем лицензированных лиц, занимающихся контролируемыми веществами, а также с самими веществами, оборудованием и сырьем, используемым при их производстве и упаковке, с целью предотвращения утечки таких предметов в каналы незаконной торговли.На Компанию не наложены какие-либо ограничения за несоблюдение вышеуказанных правил, но нет никаких гарантий, что ограничения или штрафы не будут наложены на Компанию в будущем.
Возмещение медицинских расходов. Методы и уровень возмещения расходов на фармацевтические продукты в рамках программ Medicare, Medicaid и других внутренних программ возмещения расходов являются предметом постоянного контроля со стороны правительств штатов и федерального правительства, а также частных сторонних плательщиков, таких как страховые компании. Компания считает, что правительственные учреждения США продолжат анализировать и оценивать альтернативные методы оплаты и реформировать меры, направленные на снижение стоимости лекарств для населения. В рамках этих усилий федеральное правительство и несколько штатов возбудили административные или судебные иски, оспаривающие практику ценообразования некоторых названных производителей лекарств. Компания не является стороной ни в одном из этих действий. Поскольку результат этих и других инициатив по реформе здравоохранения неясен, Компания не может предсказать, какое влияние они на нее окажут, если таковое будет.
Компания считает, что правительственные учреждения США продолжат анализировать и оценивать альтернативные методы оплаты и реформировать меры, направленные на снижение стоимости лекарств для населения. В рамках этих усилий федеральное правительство и несколько штатов возбудили административные или судебные иски, оспаривающие практику ценообразования некоторых названных производителей лекарств. Компания не является стороной ни в одном из этих действий. Поскольку результат этих и других инициатив по реформе здравоохранения неясен, Компания не может предсказать, какое влияние они на нее окажут, если таковое будет.
Законодательство Medicaid требует, чтобы все производители фармацевтической продукции уплачивали правительствам штатов определенный процент от средней отпускной цены производителя, основанной на продажах лекарств для амбулаторного лечения, расходы на которые возмещаются в рамках программ штата Medicaid. Требуемая ставка скидки для производителей дженериков в настоящее время составляет 11% от средневзвешенной цены продажи каждого продукта на уровне единицы.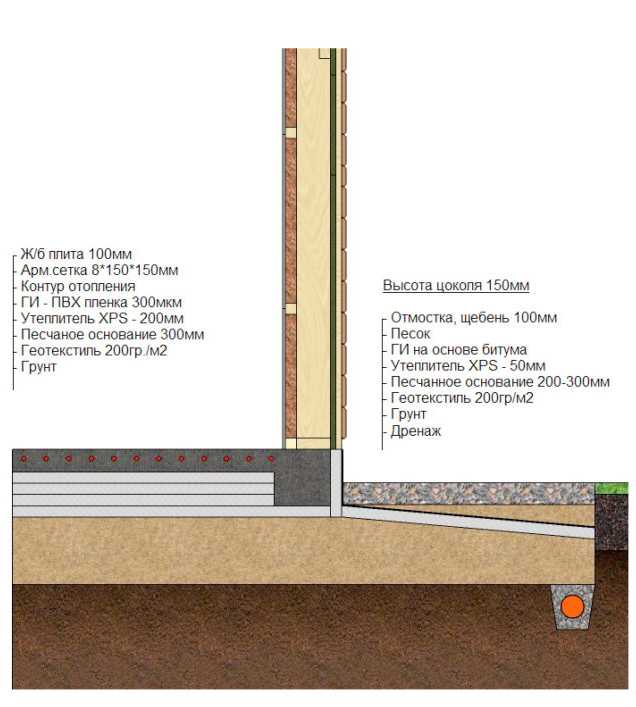
Во многих странах, в которых Компания ведет бизнес, за исключением США, начальные цены на фармацевтические препараты для человека зависят от правительственного одобрения или разрешения в рамках государственных схем возмещения расходов.Эти государственные программы обычно устанавливают цены на основе производственных затрат или цен на сопоставимые продукты. Последующее повышение цен также может регулироваться. В последние годы в рамках общих программ по снижению расходов на здравоохранение некоторые европейские правительства запретили повышение цен и ввели различные системы, предназначенные для снижения цен. В настоящее время проводится обзор предлагаемых законодательных изменений на рынке дженериков в Великобритании, и в рамках обзора временного законодательства о максимальных ценах для продажи дженериков в США.был представлен К. В Германии в январе 2002 г. было принято новое законодательство, которое изменило существующую систему фиксированных цен, требуя снижения цен на некоторые непатентованные фармацевтические препараты для человека, включая большое количество продуктов Компании. Кроме того, несмотря на то, что новый немецкий закон разрешает фармацевтам заменять дженериками некоторые патентованные препараты, существует несколько исключений из этого закона, которые, по мнению Компании, сделают его менее чем полностью эффективным в отношении требования такой замены на широкой основе.Было предложено принять законодательство в 2003 г. в Германии и Франции, которое, если оно будет принято в предлагаемой в настоящее время форме, приведет к устранению возмещения государством расходов на значительную продукцию Компании, что существенно снизит продажи этой продукции. В случае принятия в соответствии с предложением доходы и доходы в этих странах окажутся неблагоприятными. Аналогичное законодательство рассматривается в Швеции. Кроме того, во Франции рассматривается предлагаемый закон, который, в случае его принятия, введет систему референтных цен, которая может оказать понижательное давление на цены на продукцию Компании и привести к исключению значительного числа продуктов Компании из числа государственное возмещение.
Кроме того, несмотря на то, что новый немецкий закон разрешает фармацевтам заменять дженериками некоторые патентованные препараты, существует несколько исключений из этого закона, которые, по мнению Компании, сделают его менее чем полностью эффективным в отношении требования такой замены на широкой основе.Было предложено принять законодательство в 2003 г. в Германии и Франции, которое, если оно будет принято в предлагаемой в настоящее время форме, приведет к устранению возмещения государством расходов на значительную продукцию Компании, что существенно снизит продажи этой продукции. В случае принятия в соответствии с предложением доходы и доходы в этих странах окажутся неблагоприятными. Аналогичное законодательство рассматривается в Швеции. Кроме того, во Франции рассматривается предлагаемый закон, который, в случае его принятия, введет систему референтных цен, которая может оказать понижательное давление на цены на продукцию Компании и привести к исключению значительного числа продуктов Компании из числа государственное возмещение. (См. разделы «Факторы риска» и «Обсуждение и анализ руководством финансового состояния и результатов деятельности».) случаев, ограничить диапазон различных форм лекарств, доступных для рецепта национальными службами здравоохранения. Эти меры контроля могут привести к значительным различиям в ценах между государствами-членами. Существует также Общий внешний тариф, уплачиваемый при ввозе лекарственных средств в ЕС, хотя в отношении некоторых продуктов предусмотрены исключения, разрешающие беспошлинный ввоз.Если в отношении лекарственного средства не действует тарифная приостановка, можно подать заявку на беспошлинный ввоз продукта, но это подлежит рассмотрению на европейском уровне, чтобы установить, сможет ли государство-член производить продукт. вместо этого под вопросом. Кроме того, на некоторые продукты распространяется государственная квота, которая ограничивает количество, которое можно ввозить беспошлинно.
(См. разделы «Факторы риска» и «Обсуждение и анализ руководством финансового состояния и результатов деятельности».) случаев, ограничить диапазон различных форм лекарств, доступных для рецепта национальными службами здравоохранения. Эти меры контроля могут привести к значительным различиям в ценах между государствами-членами. Существует также Общий внешний тариф, уплачиваемый при ввозе лекарственных средств в ЕС, хотя в отношении некоторых продуктов предусмотрены исключения, разрешающие беспошлинный ввоз.Если в отношении лекарственного средства не действует тарифная приостановка, можно подать заявку на беспошлинный ввоз продукта, но это подлежит рассмотрению на европейском уровне, чтобы установить, сможет ли государство-член производить продукт. вместо этого под вопросом. Кроме того, на некоторые продукты распространяется государственная квота, которая ограничивает количество, которое можно ввозить беспошлинно.
Соблюдение экологических норм
Компания считает, что она в значительной степени соблюдает все применимые федеральные, государственные и местные положения, регулирующие сброс материалов в окружающую среду или иным образом относящиеся к защите окружающей среды. В настоящее время Компания ведет административное разбирательство в отношении загрязнения почвы и водоносных горизонтов на своем заводе в Будапеште. Компания подчиняется распоряжениям государственной администрации, касающимся атмосферного воздуха и сброса отходов на заводе в Лоуэлле, штат Арканзас, а также вопросов обработки, транспортировки и сброса отходов на заводе в Лонгмонте, штат Колорадо. Ожидается, что текущие расходы на эти административные распоряжения и разбирательство в Будапеште не будут существенными.
В настоящее время Компания ведет административное разбирательство в отношении загрязнения почвы и водоносных горизонтов на своем заводе в Будапеште. Компания подчиняется распоряжениям государственной администрации, касающимся атмосферного воздуха и сброса отходов на заводе в Лоуэлле, штат Арканзас, а также вопросов обработки, транспортировки и сброса отходов на заводе в Лонгмонте, штат Колорадо. Ожидается, что текущие расходы на эти административные распоряжения и разбирательство в Будапеште не будут существенными.
В сентябре 2001 г. пожар на заводе компании в Лоуэлле, штат Арканзас, привел к выбросу мышьяка в воду, поступающую на местное водоочистное сооружение, в почву, окружающую завод, и в сажу, распространяющуюся внутри завода.В 2002 году были завершены восстановительные работы, проведенные под наблюдением Департамента качества окружающей среды штата Арканзас. Реабилитационные работы были завершены, и практически все расходы были покрыты страховкой.
Несмотря на то, что многие крупные капитальные проекты, включая текущие проекты расширения Компании, как правило, включают компонент контроля за состоянием окружающей среды, в 2003 году не ожидается никаких материальных затрат на контроль за состоянием окружающей среды.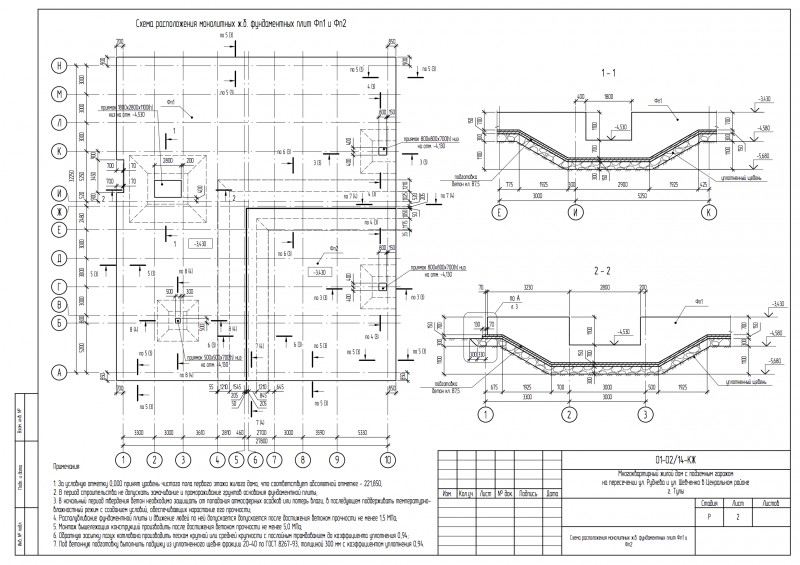 системы управления в большинстве своих операций, и мы можем понести значительные расходы, включая потенциальные штрафы или пени, если обнаружим экологические условия или имевшие место в прошлом несоблюдения на наших объектах.Кроме того, обнаружение ранее неизвестного загрязнения или введение новых требований по очистке на объектах, на которых мы в настоящее время проводим мероприятия по восстановлению окружающей среды, может потребовать от нас дополнительных затрат или стать основанием для новых или повышенных обязательств, которые могут иметь существенные неблагоприятные последствия. о нашем бизнесе, финансовом состоянии или результатах деятельности.
системы управления в большинстве своих операций, и мы можем понести значительные расходы, включая потенциальные штрафы или пени, если обнаружим экологические условия или имевшие место в прошлом несоблюдения на наших объектах.Кроме того, обнаружение ранее неизвестного загрязнения или введение новых требований по очистке на объектах, на которых мы в настоящее время проводим мероприятия по восстановлению окружающей среды, может потребовать от нас дополнительных затрат или стать основанием для новых или повышенных обязательств, которые могут иметь существенные неблагоприятные последствия. о нашем бизнесе, финансовом состоянии или результатах деятельности.
Сырье
Многие виды сырья, включая АФС, необходимые для деятельности Компании, закупаются у отдельных поставщиков.Любой перерыв в доступности этих материалов может привести к задержкам производства и снижению продаж затронутых продуктов. Такое прерывание деятельности может оказать существенное неблагоприятное воздействие на деятельность Компании. В этом случае Компания может попытаться заключить соглашения с третьими сторонами о закупке сырья, что может потребовать дополнительных разрешений регулирующих органов, поскольку разрешения относятся к одному продукту, произведенному указанным производителем.
В этом случае Компания может попытаться заключить соглашения с третьими сторонами о закупке сырья, что может потребовать дополнительных разрешений регулирующих органов, поскольку разрешения относятся к одному продукту, произведенному указанным производителем.
Пересмотры финансовых отчетов
В течение третьего квартала 2000 года Компания пересмотрела свои финансовые отчеты за четыре квартала 1999 года и первые два квартала 2000 года.Изменения произошли в связи со счетами-фактурами в Бразилии, которые либо не подтверждались базовыми транзакциями, либо зарегистрированные продажи по которым не соответствовали базовым транзакциям. В ноябре 2001 г. Компания объявила о завершении пересмотра своей финансовой отчетности за 1998, 1999, 2000 гг. и первые два квартала 2001 г. Этот пересмотр был вызван, главным образом, необходимыми изменениями в признании выручки по конкретным заказам клиентов в бизнесе AH Компании. в 1998, 1999 и 2000 годах с момента, когда заказ был разделен на сторонних складах и выставлен счет, до последующего периода, когда заказ был отправлен покупателю со склада третьей стороны.
Сотрудники
По состоянию на 31 декабря 2002 г. в Компании работало около 4 700 сотрудников, в том числе около 2 050 в США и 2 650 за пределами США. Компания считает свои отношения со своими сотрудниками хорошими. На трех американских предприятиях заключены коллективные договоры, а на четырех крупных европейских предприятиях Компании действуют рабочие советы, и на них распространяются национальные трудовые соглашения. Компания считает свои отношения со всеми этими подразделениями удовлетворительными.Срок действия двух коллективных договоров, касающихся сотрудников AH на объекте Willow Island, истекает в первой половине 2003 года.
Факторы риска
Настоящий отчет содержит определенные прогнозные заявления. Как и любая компания, подверженная конкуренции и меняющейся деловой среде, Компания не может гарантировать результаты, предсказанные в любом из прогнозных заявлений Компании. Важные факторы, которые могут привести к тому, что фактические результаты могут существенно отличаться от тех, что указаны в прогнозных заявлениях, включают (но не ограничиваются ими) следующее:
Важные факторы, которые могут привести к тому, что фактические результаты могут существенно отличаться от тех, что указаны в прогнозных заявлениях, включают (но не ограничиваются ими) следующее:
Объекты в Балтиморе и Элизабет.Неспособность должным образом учесть эти замечания может оказать существенное негативное влияние на деятельность Компании.
В течение 2001 и 2002 гг. Компания получила существенные уведомления об инспекционных наблюдениях («Отчеты 483») от FDA на объекте USHP в Балтиморе. В отчетах 483 перечислены предполагаемые отклонения, в первую очередь, от цГМФ. Инспекция 2001 года в Балтиморе привела к заявлению FDA о том, что Компания не соблюдает Постановление о согласии 1992 года, которое требует общего соблюдения cGMP.В течение 2003 года Компания получила отчет 483 от FDA в результате инспекции FDA на объекте USHP в Элизабет.
В результате инспекции 2002 г. в Балтиморе и инспекции 2003 г. в Элизабет было получено 483 отчета, в ответ на которые Компания представила в FDA всеобъемлющие планы корректирующих действий. Компания приступила к реализации этих планов на обоих объектах. Планы корректирующих действий включали отзыв определенных продуктов, произведенных в Балтиморе, который был проведен в 2002 году, и отзыв определенных продуктов, произведенных в Элизабет, которые были проведены в 2003 году.Затраты на эти отзывы уже были понесены. Балтиморский план корректирующих действий также включает замедление производства, которое началось в 2002 г. и продолжается в 2003 г. В 2002 г. Компания понесла расходы в размере 3,2 млн долл. этих планов корректирующих действий.
Компания приступила к реализации этих планов на обоих объектах. Планы корректирующих действий включали отзыв определенных продуктов, произведенных в Балтиморе, который был проведен в 2002 году, и отзыв определенных продуктов, произведенных в Элизабет, которые были проведены в 2003 году.Затраты на эти отзывы уже были понесены. Балтиморский план корректирующих действий также включает замедление производства, которое началось в 2002 г. и продолжается в 2003 г. В 2002 г. Компания понесла расходы в размере 3,2 млн долл. этих планов корректирующих действий.
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) не ответило Компании относительно адекватности любого из этих планов или отзывов и действий по замедлению, содержащихся в них.Не может быть никаких гарантий того, что текущая реализация планов корректирующих действий или реакция FDA на состояние этих объектов не потребует дальнейших действий со значительными дополнительными затратами, включая дополнительный отзыв продукции или корректирующие действия, которые еще больше ограничивают производство по сравнению с их текущими уровнями. . Кроме того, отзыв продукции в будущем может привести к значительным расходам Компании, возможным перебоям в поставках продукции Компании ее клиентам и негативной рекламе, что может нанести ущерб способности Компании продавать свою продукцию.Аналогичным образом, отзыв одного из продуктов Компании или продукта, произведенного другим производителем, может снизить продажи других аналогичных продуктов, которые продает Компания, из-за путаницы в отношении объема отзыва.
. Кроме того, отзыв продукции в будущем может привести к значительным расходам Компании, возможным перебоям в поставках продукции Компании ее клиентам и негативной рекламе, что может нанести ущерб способности Компании продавать свою продукцию.Аналогичным образом, отзыв одного из продуктов Компании или продукта, произведенного другим производителем, может снизить продажи других аналогичных продуктов, которые продает Компания, из-за путаницы в отношении объема отзыва.
Статус соответствия FDA каждого из предприятий в Балтиморе и Элизабет имел и будет иметь эффект отсрочки утверждения новых продуктов на каждом из этих предприятий до тех пор, пока FDA не убедится, что достигнут достаточный прогресс для достижения соответствия cGMP. в отношении этих объектов.Задержки с утверждением продукции на каком-либо из предприятий Компании не обязательно повлияют на утверждение продукции на других ее предприятиях. Если время, необходимое для достижения соответствия, превышает время, установленное в планах корректирующих действий Компании, задержка может быть существенно неблагоприятной. FDA также имеет право налагать гражданские штрафы и использовать справедливое изъятие в связи с отчетами 483 или указом о согласии в Балтиморе, хотя FDA не предприняло никаких подобных действий в отношении Компании.(См. сразу последующий фактор риска, связанный с государственными постановлениями.) Эти вопросы могут оказать существенное негативное влияние на будущие операции Компании.
FDA также имеет право налагать гражданские штрафы и использовать справедливое изъятие в связи с отчетами 483 или указом о согласии в Балтиморе, хотя FDA не предприняло никаких подобных действий в отношении Компании.(См. сразу последующий фактор риска, связанный с государственными постановлениями.) Эти вопросы могут оказать существенное негативное влияние на будущие операции Компании.
Компания подчиняется правительственным постановлениям и действиям, которые увеличивают расходы Компании и могут помешать маркетингу и продаже некоторых ее продуктов в определенных странах.
Исследования, разработки, производство и маркетинг лекарственных препаратов компании для человека и продуктов для здоровья животных подлежат широкому государственному регулированию.Государственное регулирование включает проверку и контроль за тестированием, производством, безопасностью, эффективностью, маркировкой, ведением учета, ценообразованием, продажей и распространением фармацевтической продукции.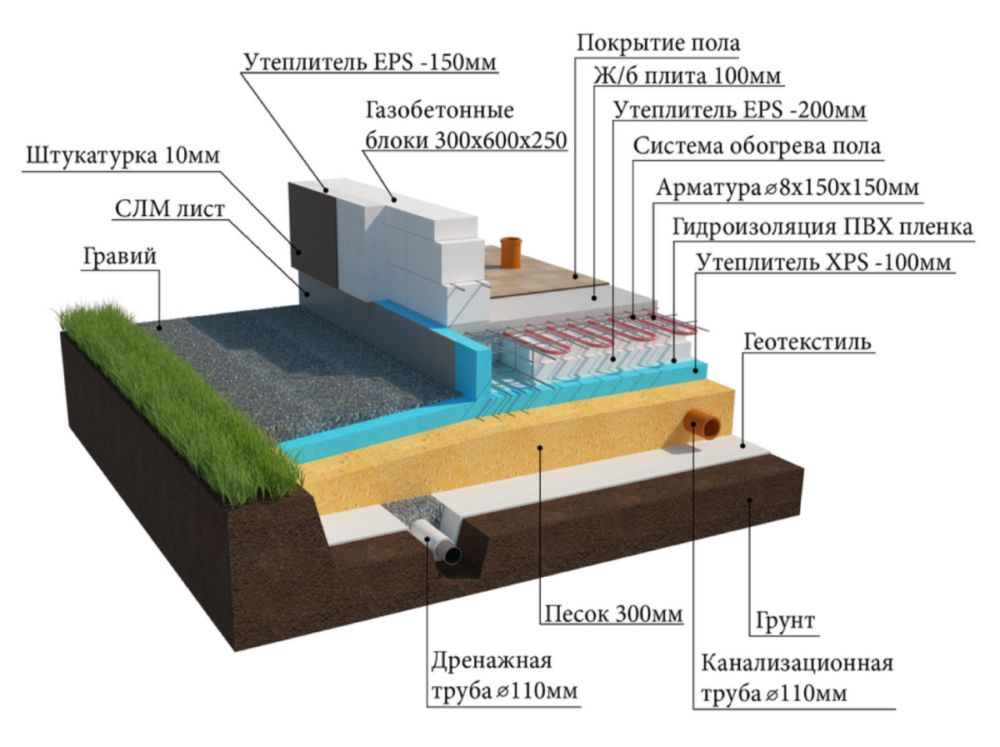 Государственное регулирование существенно увеличивает стоимость производства, разработки и реализации продукции Компании.
Государственное регулирование существенно увеличивает стоимость производства, разработки и реализации продукции Компании.
Правительства США и других стран регулярно проверяют производственные операции. Эти проверки могут привести к проблемам регулирующих органов, требующим ответа со стороны Компании. Неспособность должным образом решить эти проблемы может оказать существенное негативное влияние на Компанию, включая, среди прочего, задержки в утверждении продукции, сокращение производства и производственные перерывы.Несоблюдение применимых требований может привести к штрафам, отзыву или конфискации продуктов, приостановке производства или распространения и лишению отдельных лиц или Компании возможности предоставлять услуги фармацевтическим компаниям в любом качестве или получать новые разрешения на лекарства. В последние годы, помимо усиления соблюдения требований cGMP, федеральное правительство использовало справедливое изъятие как средство обеспечения соблюдения правил cGMP FDA.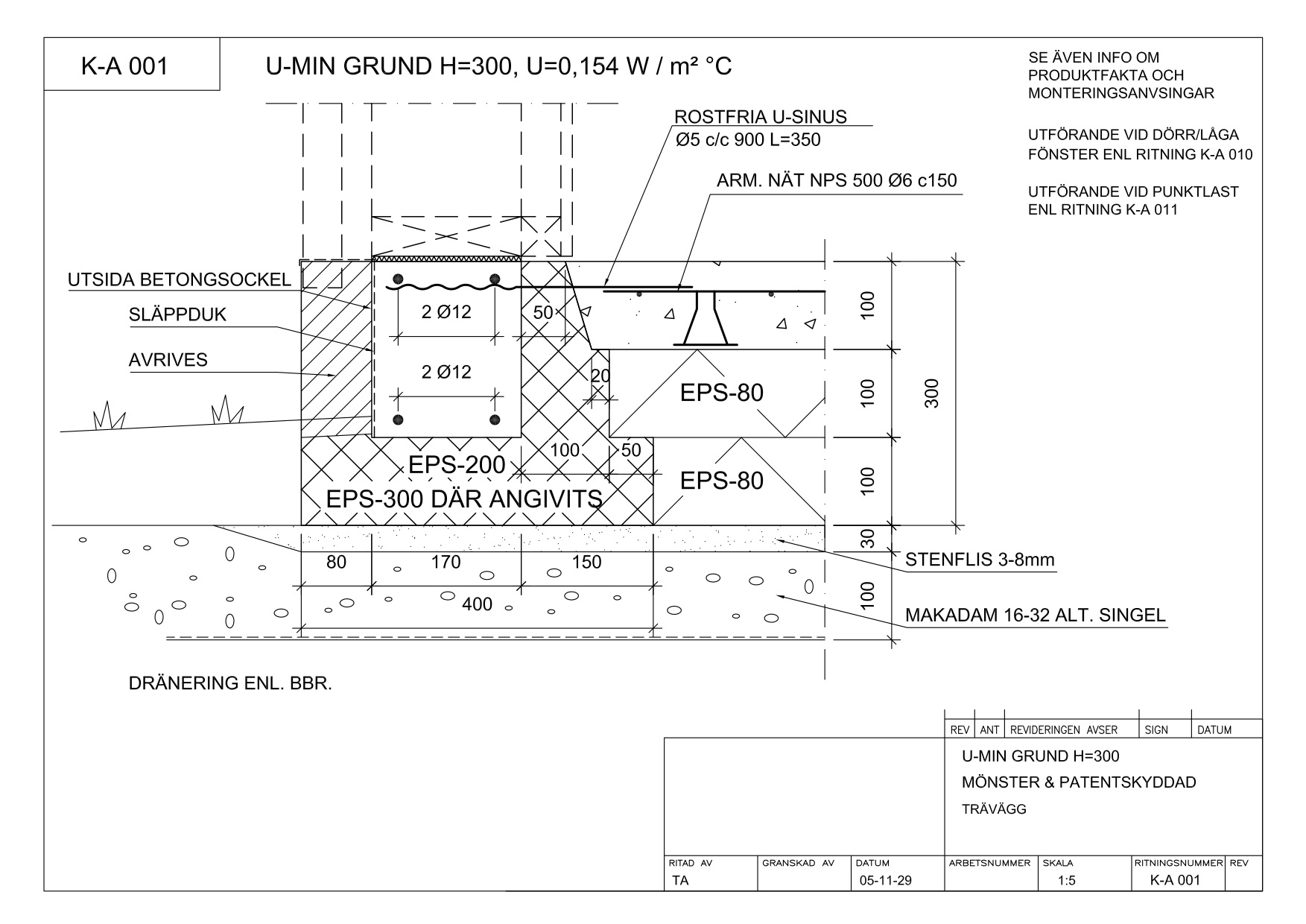 Не может быть никаких гарантий, что FDA не попытается наложить аналогичные санкции на Компанию, и любая такая санкция может оказать существенное неблагоприятное влияние на деятельность и деятельность Компании.(См. непосредственно предшествующий фактор риска, который касается планов корректирующих действий, связанных с cGMP на объектах Компании в Балтиморе и Элизабет.)
Не может быть никаких гарантий, что FDA не попытается наложить аналогичные санкции на Компанию, и любая такая санкция может оказать существенное неблагоприятное влияние на деятельность и деятельность Компании.(См. непосредственно предшествующий фактор риска, который касается планов корректирующих действий, связанных с cGMP на объектах Компании в Балтиморе и Элизабет.)
Компания также имеет аффилированные лица, лицензионные соглашения и другие договоренности с третьими сторонами, которые зависят от разрешений регулирующих органов, запрашиваемых такими третьими лицами. стороны. Поставщики Компании и сторонние контрактные производители должны соблюдать нормативные требования. Если будет обнаружено, что какая-либо из этих третьих сторон допустила нарушения, имеющие нормативное значение, это повлечет за собой существенное негативное воздействие на Компанию, поскольку ее поставка API и/или продукта окажется под угрозой.Несмотря на то, что Компания принимает меры, где это уместно и доступно, для обеспечения резервных поставщиков, нет никаких гарантий, что такие планы на случай непредвиденных обстоятельств смогут предоставить адекватный и своевременный продукт для устранения любой угрозы прерывания поставок продуктов Компании ее клиентам или что эти проблемы не окажут существенного влияния на деятельность Компании. (См. непосредственно предыдущий фактор риска, который касается планов корректирующих действий в Балтиморе и Элизабет.)
(См. непосредственно предыдущий фактор риска, который касается планов корректирующих действий в Балтиморе и Элизабет.)
Компания подала и продолжает подавать заявки на продажу своей продукции в FDA и другие регулирующие органы как в США.С. и на международном уровне. Сроки получения одобрения этих заявок могут существенно повлиять на будущие доходы и доходы Компании. Это особенно важно в отношении фармацевтических препаратов для людей, где Компания в некоторых случаях использует процедуры, известные как «сертификация по параграфу IV», для получения маркетинговых разрешений до последней даты, когда третья сторона может претендовать на патентную защиту, в том числе , среди прочего, в отношении габапентина. Использование этой стратегии может повлечь за собой длительные судебные разбирательства, часто со значительно более крупными и лучше финансируемыми фармацевтическими компаниями.Не может быть никаких гарантий, что Компания получит одобрение нового продукта своевременно, если вообще когда-либо, путем судебного разбирательства или иным образом. Неполучение разрешений в ожидаемые сроки или вообще не может оказать существенного неблагоприятного воздействия на деятельность Компании. (См. непосредственно предшествующий фактор риска, который касается планов корректирующих действий для объектов Компании в Балтиморе и Элизабет.) Компания также имеет аффилированные лица, лицензионные соглашения и другие договоренности с компаниями, которые зависят от разрешений регулирующих органов, запрашиваемых этими компаниями.
Неполучение разрешений в ожидаемые сроки или вообще не может оказать существенного неблагоприятного воздействия на деятельность Компании. (См. непосредственно предшествующий фактор риска, который касается планов корректирующих действий для объектов Компании в Балтиморе и Элизабет.) Компания также имеет аффилированные лица, лицензионные соглашения и другие договоренности с компаниями, которые зависят от разрешений регулирующих органов, запрашиваемых этими компаниями.
Вопрос о потенциальной повышенной устойчивости бактерий к некоторым антибиотикам, используемым у некоторых сельскохозяйственных животных, является предметом дискуссий во всем мире и, в некоторых случаях, привел к правительственным ограничениям на использование антибиотиков в этих пищевых продуктах. производство животных. В то время как большая часть деятельности правительства в этой области связана с продуктами, отличными от тех, которые Компания предлагает для продажи, Европейский союз и пять стран, не входящих в ЕС, запретили использование бацитрацина цинка, кормового антибиотика и стимулятора роста, производимого Компанией и другими. который использовался в кормах для скота более 40 лет, начиная с 1 июля 1999 года.Компания не продавала этот продукт в этих странах с момента вступления в силу запрета. Запрет ЕС основан на «Принципе предосторожности», в котором говорится, что продукт может быть отозван с рынка на основании обнаружения потенциальной угрозы серьезного или необратимого ущерба, даже если такой вывод не подтверждается научной достоверностью. Попытка Компании отменить этот иск в суде первой инстанции Европейского суда не увенчалась успехом, и Компания решила не обжаловать это решение.Хотя действия ЕС негативно повлияли на бизнес Компании, они не были существенными для финансового положения Компании или результатов ее деятельности.
который использовался в кормах для скота более 40 лет, начиная с 1 июля 1999 года.Компания не продавала этот продукт в этих странах с момента вступления в силу запрета. Запрет ЕС основан на «Принципе предосторожности», в котором говорится, что продукт может быть отозван с рынка на основании обнаружения потенциальной угрозы серьезного или необратимого ущерба, даже если такой вывод не подтверждается научной достоверностью. Попытка Компании отменить этот иск в суде первой инстанции Европейского суда не увенчалась успехом, и Компания решила не обжаловать это решение.Хотя действия ЕС негативно повлияли на бизнес Компании, они не были существенными для финансового положения Компании или результатов ее деятельности.
Компания не может предсказать, будет ли расширен действующий запрет на бацитрацин цинк. Если либо (а) ЕС или страны или потребители в ЕС принимают меры по предотвращению импорта мясных продуктов из стран, в которых разрешено использование продуктов на основе бацитрацина, либо (б) распространяется запрет на другие страны, такие как У.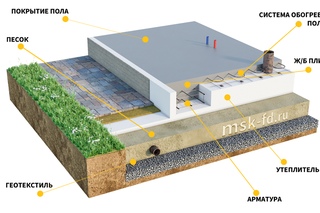 S., если у Компании есть существенные продажи продуктов на основе бацитрацина или (c) есть усиление общественного давления с целью прекращения использования кормовых добавок с антибиотиками, результирующая потеря продаж может быть существенной для финансового состояния Компании, движения денежных средств. и результаты операций. Компания также не может предсказать, приведет ли эта озабоченность по поводу устойчивости к антибиотикам к расширению правил, неблагоприятно влияющих на другие продукты для здоровья животных на основе антибиотиков, производимые Компанией, которые она продает в значительных объемах.
S., если у Компании есть существенные продажи продуктов на основе бацитрацина или (c) есть усиление общественного давления с целью прекращения использования кормовых добавок с антибиотиками, результирующая потеря продаж может быть существенной для финансового состояния Компании, движения денежных средств. и результаты операций. Компания также не может предсказать, приведет ли эта озабоченность по поводу устойчивости к антибиотикам к расширению правил, неблагоприятно влияющих на другие продукты для здоровья животных на основе антибиотиков, производимые Компанией, которые она продает в значительных объемах.
В последнее время в США активизировались дискуссии относительно устойчивости к антибиотикам, используемым у некоторых сельскохозяйственных животных. Различные источники опубликовали отчеты о возможных побочных эффектах использования антибиотиков у сельскохозяйственных животных. В некоторых из этих отчетов утверждается, что крупные производители животных, некоторые из которых являются клиентами Компании или конечными потребителями ее продукции, сокращают использование антибиотиков. Неясно, какие действия FDA может предпринять в отношении устойчивых к лекарственным препаратам бактерий в продуктах для здоровья животных.Тем не менее, FDA предложило использовать рейтинговую систему для сравнения рисков, связанных с использованием животных определенных антибиотиков, в том числе продаваемых Компанией. Хотя Компания не считает, что предлагаемая в настоящее время система оценки рисков будет существенно неблагоприятной для ее бизнеса, она может быть изменена до принятия или более поздних поправок. Потеря рынка США для продуктов Компании на основе антибиотиков или негативная огласка в отношении продуктов Компании на основе антибиотиков нанесут существенный ущерб Компании.
Неясно, какие действия FDA может предпринять в отношении устойчивых к лекарственным препаратам бактерий в продуктах для здоровья животных.Тем не менее, FDA предложило использовать рейтинговую систему для сравнения рисков, связанных с использованием животных определенных антибиотиков, в том числе продаваемых Компанией. Хотя Компания не считает, что предлагаемая в настоящее время система оценки рисков будет существенно неблагоприятной для ее бизнеса, она может быть изменена до принятия или более поздних поправок. Потеря рынка США для продуктов Компании на основе антибиотиков или негативная огласка в отношении продуктов Компании на основе антибиотиков нанесут существенный ущерб Компании.
Зарубежная деятельность Компании связана с дополнительными экономическими и политическими рисками.
Зарубежные операции Компании подвержены колебаниям валютных курсов и ограничениям, политической нестабильности в некоторых странах и неопределенности в отношении обеспечения соблюдения коммерческих прав и государственного контроля над ними. Неопределенность, связанная с конфликтом с Ираком, и сохраняющиеся террористические угрозы могут негативно сказаться на деятельности Компании.
Неопределенность, связанная с конфликтом с Ираком, и сохраняющиеся террористические угрозы могут негативно сказаться на деятельности Компании.
Компания продает продукцию во многих странах, подверженных значительным колебаниям валютных курсов.API-продукты Компании обычно продаются за доллары США, что устраняет прямую подверженность колебаниям валютных курсов, но увеличивает кредитный риск, если местная валюта значительно обесценивается и клиентам становится труднее покупать доллары США, необходимые для оплаты Компании.
Некоторые регионы, включая Аргентину, Бразилию и Индонезию, страдают от резких колебаний валютных курсов и снижения экономической активности в этих регионах, а в некоторых ограниченных районах — от социальных и политических волнений.
Перебои в поставках сырья или продукции Компании или неблагоприятное событие на одном из производственных объектов Компании могут негативно сказаться на ее деятельности.
В настоящее время Компания закупает большую часть своего сырья, включая АФС и другие продукты, у одних поставщиков, и многие из ее продуктов производятся на одном предприятии. Любой перебой в поставке этих материалов или неблагоприятное событие на предприятиях, которые производят и смешивают продукты Компании, может привести к снижению продаж затронутых продуктов.В этом случае Компания может попытаться заключить соглашения с третьими сторонами о покупке сырья или продукции, а также об аренде или покупке новых производственных мощностей. Компания может быть не в состоянии найти третью сторону, желающую или способную предоставить необходимые продукты или оборудование, подходящие для производства фармацевтических препаратов на условиях, приемлемых для Компании. Если бы Компании пришлось получить замещающие материалы или продукты, Компании потребовались бы дополнительные разрешения регулирующих органов, поскольку разрешения относятся к одному продукту, произведенному указанным производителем. Точно так же использование новых объектов потребует одобрения регулирующих органов. Любое существенное прекращение поставок от поставщиков Компании или неблагоприятное событие на любом из ее производственных объектов может оказать существенное негативное влияние на деятельность Компании.
Точно так же использование новых объектов потребует одобрения регулирующих органов. Любое существенное прекращение поставок от поставщиков Компании или неблагоприятное событие на любом из ее производственных объектов может оказать существенное негативное влияние на деятельность Компании.
На деятельность Компании оказывали и будут воздействовать факторы конкуренции, включая ценовую конкуренцию и ограничения, включая государственное регулирование, на определенных рынках.
Бизнес компании по производству непатентованных фармацевтических препаратов исторически был предметом жесткой конкуренции, особенно из-за цены.По мере истечения срока действия патентов и других оснований для эксклюзивности на рынке цены обычно снижаются, поскольку на рынок выходят конкуренты-дженерики, такие как Компания. Обычно происходит дальнейшее снижение цены за единицу по мере увеличения числа конкурентов-дженериков. Сроки такого снижения цен непредсказуемы и могут привести к значительному сокращению периода прибыльности непатентованного препарата. Кроме того, производители фирменных и запатентованных фармацевтических препаратов часто принимают меры, чтобы предотвратить или воспрепятствовать использованию непатентованных эквивалентов.Эти действия могут включать:
Кроме того, производители фирменных и запатентованных фармацевтических препаратов часто принимают меры, чтобы предотвратить или воспрепятствовать использованию непатентованных эквивалентов.Эти действия могут включать:
- подачу новых патентов на лекарства, срок действия первоначальной патентной защиты которых истекает;
- разработка запатентованных продуктов с контролируемым высвобождением или других усовершенствований продукта; и
- увеличение маркетинговых инициатив и подача дополнительных судебных исков.
В последние годы на конъюнктуру рынка дженериков, в частности в США, еще больше повлияло фундаментальное изменение отраслевых моделей распределения, закупок и складирования в результате возросшей важности продаж крупным оптовикам и одновременного сокращения продаж частным распространители универсальных этикеток.Программы оптовых торговцев обычно требуют более низких цен на продаваемые товары, более низкие уровни запасов, хранящихся у оптовых продавцов, и меньшее количество производителей, выбранных для предоставления продуктов для собственных маркетинговых программ оптовых продавцов.
Факторы, которые негативно повлияли на фармацевтическую промышленность США по производству дженериков, могут также повлиять на некоторые или все рынки, на которых Компания работает на международном уровне. Кроме того, в Европе Компания сталкивается с ценовым давлением из-за параллельного импорта идентичных товаров с более дешевых рынков в соответствии с законами ЕС о свободном перемещении товаров.Параллельный импорт может привести к снижению выручки и операционной прибыли Компании. На международный фармацевтический бизнес Компании также влияют общие правительственные инициативы по снижению цен на лекарства, включая контроль над ценами или другие ограничения в отрасли Компании. Параллельный импорт, сдерживание государственных расходов и другие меры регулирования могут привести к снижению цен на определенных рынках, включая Великобританию, Германию и страны Северной Европы, где Компания имеет значительные объемы продаж.
Министерство здравоохранения Соединенного Королевства в настоящее время рассматривает предлагаемые законодательные изменения на рынке непатентованных лекарственных средств Соединенного Королевства и в рамках этого пересмотра в августе 2000 г. приняло временное законодательство о максимальных ценах для продажи непатентованных лекарственных средств в Соединенном Королевстве. Ожидается, что этот контроль над ценами останется в силе, по крайней мере, в течение 2003 года. Компания столкнулась с тенденцией к снижению цен на непатентованные фармацевтические препараты для человека в Соединенном Королевстве, которая в настоящее время является следствием конкурентного давления. с потенциалом дальнейшего снижения цен в результате будущих действий регулирующих органов.Компания не может предсказать долгосрочное влияние этих обстоятельств на деятельность Компании в Соединенном Королевстве, а также на ценообразование и продажи дженериков в Соединенном Королевстве. В Германии в январе 2002 г. было принято новое законодательство, которое скорректировало существующую систему фиксированных цен, требуя снижения цен на большое количество непатентованных фармацевтических препаратов для человека в Германии, включая ряд продуктов Компании. Несмотря на то, что этот новый немецкий закон разрешает фармацевтам заменять дженериками некоторые патентованные препараты, существует несколько исключений из этого закона, которые, по мнению Компании, сделают его менее чем полностью эффективным в отношении требования такой замены на широкой основе.
приняло временное законодательство о максимальных ценах для продажи непатентованных лекарственных средств в Соединенном Королевстве. Ожидается, что этот контроль над ценами останется в силе, по крайней мере, в течение 2003 года. Компания столкнулась с тенденцией к снижению цен на непатентованные фармацевтические препараты для человека в Соединенном Королевстве, которая в настоящее время является следствием конкурентного давления. с потенциалом дальнейшего снижения цен в результате будущих действий регулирующих органов.Компания не может предсказать долгосрочное влияние этих обстоятельств на деятельность Компании в Соединенном Королевстве, а также на ценообразование и продажи дженериков в Соединенном Королевстве. В Германии в январе 2002 г. было принято новое законодательство, которое скорректировало существующую систему фиксированных цен, требуя снижения цен на большое количество непатентованных фармацевтических препаратов для человека в Германии, включая ряд продуктов Компании. Несмотря на то, что этот новый немецкий закон разрешает фармацевтам заменять дженериками некоторые патентованные препараты, существует несколько исключений из этого закона, которые, по мнению Компании, сделают его менее чем полностью эффективным в отношении требования такой замены на широкой основе.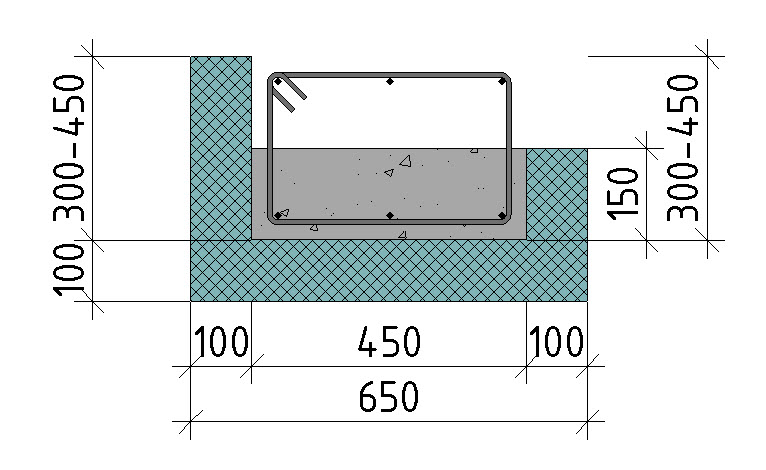 В целом, Компания ожидает, что этот закон приведет к снижению цен на непатентованные лекарственные препараты для человека в Германии, что, как ожидается, приведет к снижению прибыльности для всех участников отрасли, включая Компанию. Кроме того, правила, предложенные для введения в действие в 2003 г., лишат некоторых продуктов права на государственную компенсацию расходов на пациентов, в том числе по крайней мере один продукт, важный для операций компании в Германии, Pentalong. Компания не может предсказать, какое влияние эти обстоятельства окажут на деятельность Компании в Германии, а также на ценообразование и продажи непатентованных фармацевтических препаратов в Германии.Аналогичное законодательство о замене рассматривается в Швеции. Во Франции было предложено законодательство, которое прекратит возмещение государством расходов на большую группу непатентованных препаратов, включая значительное количество продуктов, продаваемых Компанией. Эта потеря государственного возмещения будет иметь существенные негативные последствия для операций Компании во Франции, но Компания не может предсказать, будет ли принят этот закон или, если он будет принят, его окончательная форма.
В целом, Компания ожидает, что этот закон приведет к снижению цен на непатентованные лекарственные препараты для человека в Германии, что, как ожидается, приведет к снижению прибыльности для всех участников отрасли, включая Компанию. Кроме того, правила, предложенные для введения в действие в 2003 г., лишат некоторых продуктов права на государственную компенсацию расходов на пациентов, в том числе по крайней мере один продукт, важный для операций компании в Германии, Pentalong. Компания не может предсказать, какое влияние эти обстоятельства окажут на деятельность Компании в Германии, а также на ценообразование и продажи непатентованных фармацевтических препаратов в Германии.Аналогичное законодательство о замене рассматривается в Швеции. Во Франции было предложено законодательство, которое прекратит возмещение государством расходов на большую группу непатентованных препаратов, включая значительное количество продуктов, продаваемых Компанией. Эта потеря государственного возмещения будет иметь существенные негативные последствия для операций Компании во Франции, но Компания не может предсказать, будет ли принят этот закон или, если он будет принят, его окончательная форма.
Во всех сферах бизнеса Компании может стать труднее реагировать на вызовы конкуренции, поскольку у нее мало крупных клиентов, таких как крупные оптовики, животноводы и сетевые магазины, быстро меняющийся рынок и неопределенность сроков появления нового продукта одобрения.
В Европе международная промышленность по производству непатентованных препаратов для человека и животных отличается высокой конкуренцией, и многие из конкурентов Компании в этих областях значительно крупнее и располагают большими финансовыми, техническими и маркетинговыми ресурсами, чем Компания. Повышенное внимание к ценам на фармацевтические препараты в Европе может привести к усилению конкуренции и ценового давления на поставщиков всех видов фармацевтических препаратов, включая дженерики. Кроме того, в некоторых странах, таких как Франция, из-за размера Компании и ассортимента продукции Компания может быть не в состоянии извлечь выгоду из таких изменений в конкуренции и ценообразовании так же полно, как конкуренты Компании. Кроме того, Компания ожидает, что в 2003 г. появятся новые участники рынка непатентованных лекарственных кормовых добавок для животных. Бизнес фирменных лекарственных препаратов Компании также может столкнуться с конкурентными проблемами, связанными с непатентованными аналогами. Компания имеет два патента на Кадиан, которые подлежат оспариванию в соответствии с пунктом IV, хотя до настоящего времени таких оспариваний не было. При выходе на рынок генерического аналога брендовые препараты Компании могут существенно потерять продажи.
Кроме того, Компания ожидает, что в 2003 г. появятся новые участники рынка непатентованных лекарственных кормовых добавок для животных. Бизнес фирменных лекарственных препаратов Компании также может столкнуться с конкурентными проблемами, связанными с непатентованными аналогами. Компания имеет два патента на Кадиан, которые подлежат оспариванию в соответствии с пунктом IV, хотя до настоящего времени таких оспариваний не было. При выходе на рынок генерического аналога брендовые препараты Компании могут существенно потерять продажи.
На бизнес компании Human Pharmaceutical влияет политика возмещения расходов сторонних плательщиков, таких как страховые компании и организации управляемого медицинского обслуживания.
Коммерческий успех Компании в отношении непатентованных продуктов частично зависит от наличия адекватного возмещения расходов для клиентов Компании от сторонних плательщиков медицинских услуг, таких как государственные и частные медицинские страховые компании и организации управляемого медицинского обслуживания. Сторонние плательщики все чаще оспаривают ценообразование на медицинские продукты и услуги, и их практика возмещения расходов может помешать Компании поддерживать текущий уровень цен на продукцию Компании. Кроме того, рынок для продуктов Компании может быть ограничен сторонними плательщиками, которые составляют списки разрешенных продуктов и не предоставляют возмещения за продукты, не включенные в список.Законодательство Medicaid требует, чтобы все производители фармацевтической продукции возвращали правительствам штатов процент от средней отпускной цены производителя при продаже определенных рецептурных препаратов, стоимость которых возмещается в рамках программ штата Medicaid. Некоторые штаты, такие как Мичиган и Флорида, приняли меры для дальнейшего сдерживания расходов на лекарства, отпускаемые по рецепту, в рамках их программ Medicaid. Эти меры включают в себя включение определенных рецептурных препаратов в ограниченный список и переговоры о дополнительных скидках в ценах, уплачиваемых за рецептурные препараты.
Сторонние плательщики все чаще оспаривают ценообразование на медицинские продукты и услуги, и их практика возмещения расходов может помешать Компании поддерживать текущий уровень цен на продукцию Компании. Кроме того, рынок для продуктов Компании может быть ограничен сторонними плательщиками, которые составляют списки разрешенных продуктов и не предоставляют возмещения за продукты, не включенные в список.Законодательство Medicaid требует, чтобы все производители фармацевтической продукции возвращали правительствам штатов процент от средней отпускной цены производителя при продаже определенных рецептурных препаратов, стоимость которых возмещается в рамках программ штата Medicaid. Некоторые штаты, такие как Мичиган и Флорида, приняли меры для дальнейшего сдерживания расходов на лекарства, отпускаемые по рецепту, в рамках их программ Medicaid. Эти меры включают в себя включение определенных рецептурных препаратов в ограниченный список и переговоры о дополнительных скидках в ценах, уплачиваемых за рецептурные препараты.
Ответственность Компании за несчастные случаи, ответственность за качество продукции или другие претензии могут превышать страховое покрытие Компании.
Компания стремится застраховать свою ответственность и прямой ущерб, чтобы защитить себя от ответственности в результате несчастных случаев, ответственности за качество продукции и других претензий, возникающих в ходе ведения бизнеса. Страхование, которое Компания стремится получить, чтобы защитить себя от этих потенциальных обязательств, может быть неадекватным, недостижимым или чрезмерно дорогим.Компания подлежит продлению большинства своих страховых полисов каждый год, и изменения ожидаются при каждом продлении. В последние месяцы Компания столкнулась со значительным увеличением расходов на страхование и сокращением покрытия, включая исключения из покрытия, относящиеся к определенным продуктам, которые она производит сейчас или может производить в будущем. Неспособность Компании получить и поддерживать достаточное страховое покрытие на разумных условиях может оказать существенное неблагоприятное воздействие на деятельность, финансовое положение и результаты деятельности Компании.
Компании не известны окончательные последствия исков о нарушении прав, предъявленных Pfizer в отношении габапентина, и она не знает с какой-либо уверенностью, придется ли ей списывать запасы, относящиеся к габапентину.
Компания подала заявку на сертификацию по параграфу IV, оспаривающую патенты, защищающие таблетки и капсулы Pfizer Neurontin (габапентин) — лекарство, используемое для лечения эпилепсии. Хотя это и не гарантируется, эта заявка может предоставить Компании исключительные права на рынке на срок до шести месяцев.Учитывая размер рынка габапентина (более 2,0 млрд долларов в 2002 г.), а также рыночную цену и долю, обычно ожидаемые в период действия эксклюзивных прав на дженерики, потенциал прибыли Компании (которую она изначально обязана делить поровну со своим поставщиком активного ингредиента препарата). в течение ограниченного периода) может быть значительным, если Компания получит эксклюзивные права на рынке. Компания Torpharm, конкурент, подала заявку ANDA на капсулы габапентина, недавно подала иск против FDA, добиваясь окончательного одобрения своих капсул ANDA габапентина. Если Торфарм добьется успеха, Компания может потерять право на эксклюзивность.
Если Торфарм добьется успеха, Компания может потерять право на эксклюзивность.
Тем не менее, Pfizer подала несколько исков, оспаривающих позицию компании о том, что она может представить продукт до истечения срока действия последнего из патентов Pfizer. Срок действия 30-месячного автоматического запрета на запуск Компании в соответствии с Законом Ваксмана-Хэтча истек, и, при условии благоприятного исхода в отношении вопросов эксклюзивности, Компания может иметь юридическое право начать продажу продукта до принятия окончательного решения в Pfizer. судебные разбирательства.Однако возможно, что Pfizer могут быть выданы дополнительные патенты на габапентин, что может привести к дополнительной задержке начала периода эксклюзивности на срок до 30 месяцев. Компания также может отложить начало продаж до получения решения суда или апелляции. Запуск в любое время до принятия окончательного решения по претензиям Pfizer подвергнет Компанию потенциальному материальному ущербу в связи с нарушением прав, если Pfizer в конечном итоге выиграет судебный процесс. Кроме того, чтобы быть готовым воспользоваться любым применимым шестимесячным периодом эксклюзивности, Компания должна будет производить значительные объемы запасов до любого запланированного запуска продукта и, возможно, до того, как станет известно, была ли Компания окончательно присуждено исключительное право или получение окончательного судебного решения по делу Pfizer.В случае, если Pfizer выиграет судебный процесс, Компания не получит исключительных прав или результат любого из этих событий приведет к значительной задержке запуска, этот инвентарь может больше не продаваться в коммерческих целях, что приведет к списанию и оплате. против дохода Общества в соответствующем периоде. (См. «Судебные разбирательства».)
Кроме того, чтобы быть готовым воспользоваться любым применимым шестимесячным периодом эксклюзивности, Компания должна будет производить значительные объемы запасов до любого запланированного запуска продукта и, возможно, до того, как станет известно, была ли Компания окончательно присуждено исключительное право или получение окончательного судебного решения по делу Pfizer.В случае, если Pfizer выиграет судебный процесс, Компания не получит исключительных прав или результат любого из этих событий приведет к значительной задержке запуска, этот инвентарь может больше не продаваться в коммерческих целях, что приведет к списанию и оплате. против дохода Общества в соответствующем периоде. (См. «Судебные разбирательства».)
Компания может столкнуться с трудностями при разработке и интеграции стратегических союзов, возможностей совместного развития и других отношений.
Компания намерена добиваться лицензирования конкретных продуктов, маркетинговых соглашений, возможностей совместной разработки и других партнерских соглашений в своих подразделениях по производству лекарственных средств для человека и ветеринарии. Компания также может проводить выборочные приобретения. Компания не может быть уверена, что сможет найти подходящих партнеров для этих сделок. Кроме того, если Компания найдет подходящих партнеров, процесс эффективного заключения этих договоренностей сопряжен с риском того, что внимание руководства Компании может быть отвлечено от других деловых вопросов, и что у Компании могут возникнуть трудности с интеграцией новых договоренностей в свой существующий бизнес.
Компания также может проводить выборочные приобретения. Компания не может быть уверена, что сможет найти подходящих партнеров для этих сделок. Кроме того, если Компания найдет подходящих партнеров, процесс эффективного заключения этих договоренностей сопряжен с риском того, что внимание руководства Компании может быть отвлечено от других деловых вопросов, и что у Компании могут возникнуть трудности с интеграцией новых договоренностей в свой существующий бизнес.
Компания остается с высокой долей заемных средств. Существенная задолженность Компании может поставить Компанию в невыгодное положение с точки зрения конкурентоспособности или негативно сказаться на ее способности получить дополнительное финансирование в случае необходимости.
По состоянию на 31 декабря 2002 г. общая задолженность Компании составляла 895,9 млн долларов США, а общий консолидированный акционерный капитал составлял 1 005,2 млн долларов США. Операционная прибыль Компании и EBITDA (согласно определению Кредитной линии 2001 г. ) по отношению к уровню ее задолженности могут ограничивать ее деятельность.Среди прочего, задолженность Компании и ограничительные условия, содержащиеся в соглашениях, регулирующих ее задолженность:
) по отношению к уровню ее задолженности могут ограничивать ее деятельность.Среди прочего, задолженность Компании и ограничительные условия, содержащиеся в соглашениях, регулирующих ее задолженность:
- требуют значительной части денежных потоков Компании от операций для выплаты процентов по долгу Компании;
- ограничивают способность Компании использовать свой денежный поток или получать дополнительное финансирование для финансирования приобретений и других общих корпоративных целей;
- ограничивают гибкость Компании в планировании и реагировании на изменения, а также в использовании возможностей в своем бизнесе и отрасли;
- повысить уязвимость Компании к неблагоприятным экономическим и отраслевым условиям; и
- ставят Компанию в невыгодное положение по сравнению с конкурентами с меньшим объемом заемных средств.
Кроме того, у Компании может возникнуть дополнительная задолженность. Соглашения Компании позволяют Компании и ее дочерним поручителям брать на себя существенную дополнительную задолженность.
Обслуживание долга Компании требует значительной суммы денежных средств, и способность Компании генерировать достаточное количество денежных средств зависит от многих факторов, некоторые из которых находятся вне контроля Компании.
Способность Компании производить платежи и рефинансировать свой долг зависит от способности Компании генерировать денежный поток.Это в значительной степени зависит от общеэкономических, финансовых, конкурентных, законодательных, нормативных и других факторов, не зависящих от Компании. Кроме того, способность Компании заимствовать средства в будущем для погашения своего долга будет зависеть от выполнения ею финансовых условий Кредитной линии 2001 года и других долговых соглашений. Бизнес Компании может не генерировать достаточный денежный поток от операций, и будущие займы могут быть недоступны для Компании в рамках Кредитной линии 2001 года или иным образом в сумме, достаточной для того, чтобы Компания могла погасить свой долг или финансировать другие потребности в ликвидности. Если Компания не может генерировать достаточно денежных средств, ей может потребоваться рефинансировать весь или часть своего долга в момент или до наступления срока погашения. Компания может оказаться не в состоянии рефинансировать какой-либо из своих долгов на выгодных условиях или вообще не иметь возможности. Любая неспособность генерировать достаточный денежный поток или рефинансировать задолженность Компании на выгодных условиях может оказать существенное неблагоприятное воздействие на ее финансовое положение.
Если Компания не может генерировать достаточно денежных средств, ей может потребоваться рефинансировать весь или часть своего долга в момент или до наступления срока погашения. Компания может оказаться не в состоянии рефинансировать какой-либо из своих долгов на выгодных условиях или вообще не иметь возможности. Любая неспособность генерировать достаточный денежный поток или рефинансировать задолженность Компании на выгодных условиях может оказать существенное неблагоприятное воздействие на ее финансовое положение.
Ковенантные ограничения по непогашенным долговым обязательствам Компании могут ограничивать способность Компании вести свою деятельность.
Непогашенные долговые инструменты Компании содержат ковенанты, которые ограничивают способность Компании и поручителей финансировать будущие операции и потребности в капитале, а также участвовать в некоторых других видах коммерческой деятельности. Например, Кредитная линия 2001 года требует, чтобы Компания поддерживала определенные финансовые коэффициенты и удовлетворяла критериям финансового состояния, состоящим из теста максимального общего коэффициента заемных средств, теста максимального коэффициента старшего долга, теста минимального коэффициента покрытия фиксированных платежей, теста минимального коэффициента покрытия процентов. и тест на минимальный собственный капитал.
и тест на минимальный собственный капитал.
В дополнение к финансовым ковенантам Кредитная линия 2001 г. имеет ряд нефинансовых положений, в том числе требование о том, чтобы Промышленник сохранял контроль над достаточным количеством обыкновенных акций Компании класса B, чтобы позволить Промышленнику избирать большинство членов Совета директоров Компании. Режиссеры. Сохранение этого контроля над Компанией зависит от односторонних действий Промышленника и поддержания Промышленником определенной залоговой стоимости по договору банковского кредита Промышленника, срок действия которого истекает 30 июня 2003 г. (который включает расчеты, частично основанные на предполагаемых стоимость обыкновенных акций Компании класса B, принадлежащих Industrier, которая, в свою очередь, основана на рыночной стоимости обыкновенных акций Компании класса A, устанавливаемой время от времени на Нью-Йоркской фондовой бирже).Если залоговая стоимость Industrier упадет ниже определенного уровня (что, при условии постоянной стоимости других обеспеченных активов Industrier, произойдет, если цена обыкновенных акций компании класса A составит 3,50 доллара США или ниже), кредиторы могут объявить дефолт по соглашению о банковской ссуде Industrier. В случае дефолта или если Industrier не полностью выплатит или не рефинансирует свое соглашение о банковском кредите на дату погашения 30 июня 2003 г., банки Industrier могут действовать для защиты своих прав, вызывая изменение бенефициарного владения обыкновенными акциями Компании класса B. принадлежит Industrier.Любое такое изменение в бенефициарном владении обыкновенными акциями Компании класса B, принадлежащими Industrier, будет означать смену контроля над Компанией и дефолт по Кредитной линии 2001 года. Кредитная линия 2001 года также содержит требование о том, чтобы Компания предоставляла неквалифицированные аудиторские заключения от своих независимых бухгалтеров.
В случае дефолта или если Industrier не полностью выплатит или не рефинансирует свое соглашение о банковском кредите на дату погашения 30 июня 2003 г., банки Industrier могут действовать для защиты своих прав, вызывая изменение бенефициарного владения обыкновенными акциями Компании класса B. принадлежит Industrier.Любое такое изменение в бенефициарном владении обыкновенными акциями Компании класса B, принадлежащими Industrier, будет означать смену контроля над Компанией и дефолт по Кредитной линии 2001 года. Кредитная линия 2001 года также содержит требование о том, чтобы Компания предоставляла неквалифицированные аудиторские заключения от своих независимых бухгалтеров.
Кредитная линия 2001 г. также требует, чтобы Компания уменьшила непогашенную основную сумму (i) своих 5,75%-ных Облигаций до 10,0 миллионов долларов США или меньше к 1 октября 2004 г. и (ii) своих 3-процентных Облигаций до 10 долларов США.0 миллионов или меньше к 1 декабря 2005 г. Для выполнения этих обязательств Компании может потребоваться выпустить дополнительные обыкновенные акции класса А для держателей Облигаций, что размывает интересы нынешних акционеров Компании.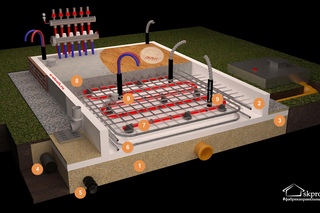
События, не зависящие от Компании, в том числе изменения общих экономических и деловых условий, могут повлиять на ее способность выполнить финансовые обязательства по Кредитной Линии 2001 года. Компания может не выполнять эти условия, и кредиторы могут не отказываться от невыполнения этих условий.Нарушение любого из этих условий, если оно не будет устранено или отменено, может привести к дефолту по Кредитной линии 2001 года и другим долговым соглашениям. В случае неисполнения обязательств по Кредитной линии 2001 г. кредиторы по этим линиям могут принять решение объявить все непогашенные суммы вместе с начисленными процентами подлежащими немедленной оплате. Кредитная линия 2001 года также подлежит прекращению в определенных случаях.
Интересы держателя контрольного пакета акций Общества могут противоречить интересам Общества.
Industrier является бенефициарным владельцем 11 872 897 обыкновенных акций Компании класса B по состоянию на 31 декабря 2002 г. , что составляет 100% находящихся в обращении обыкновенных акций Компании класса B на эту дату. По состоянию на 31 декабря 2002 г. Industrier владел 54,6% голосующих акций наших обыкновенных акций. Таким образом, Industrier имеет значительное влияние и контроль над бизнесом Компании и в настоящее время имеет право избирать две трети членов ее совета директоров. Эйнар Сиссенер, председатель совета директоров компании, контролирует большинство выпущенных в обращение акций Industrier и является председателем Industrier.Кроме того, г-н Сиссенер фактически владеет 373 667 обыкновенными акциями Компании класса А.
, что составляет 100% находящихся в обращении обыкновенных акций Компании класса B на эту дату. По состоянию на 31 декабря 2002 г. Industrier владел 54,6% голосующих акций наших обыкновенных акций. Таким образом, Industrier имеет значительное влияние и контроль над бизнесом Компании и в настоящее время имеет право избирать две трети членов ее совета директоров. Эйнар Сиссенер, председатель совета директоров компании, контролирует большинство выпущенных в обращение акций Industrier и является председателем Industrier.Кроме того, г-н Сиссенер фактически владеет 373 667 обыкновенными акциями Компании класса А.
Промышленник имеет возможность принимать решения, влияющие на бизнес Компании и структуру капитала, включая, в некоторых случаях, выпуск дополнительных долговых обязательств. Industrier может проводить будущие сделки, которые могли бы повысить его инвестиции в акционерный капитал, в то же время сопряженные с риском для интересов Компании. Все договорные отношения между Компанией и Industrier подлежат рассмотрению или утверждению комитетом по аудиту совета директоров Компании на предмет справедливости условий таких договоренностей по отношению к Компании. Комитет по аудиту состоит исключительно из одного или нескольких директоров, не связанных с Industrier.
Комитет по аудиту состоит исключительно из одного или нескольких директоров, не связанных с Industrier.
Компания также время от времени участвует в различных сделках с Industrier, и в отношении условий таких сделок существуют конфликты интересов.
Пункт 1А. Руководители регистранта
Ниже приводится список имен и возрастов всех корпоративных исполнительных должностных лиц Компании с указанием всех должностей и должностей у регистранта, занимаемых каждым таким лицом, а также основной род занятий или место работы каждого такого лица в прошлом. пять лет.
Предусилитель leslie Vibratone по существу был эквивалентом Leslie 16. Кабель с косичками соединял … Краткий обзор Универсальная педаль комбинированного предусилителя для колонок Leslie 110/120 В Если ваша колонка Leslie рассчитана на 220/240 В: используйте 220/240V UC-1A Изображения продукта Описание продукта UC-1A позволяет использовать большинство динамиков Leslie с портативным органом, гитарой, синтезатором или любым другим аудиоисточником, который можно подключить к стандартному разъему 1/4 дюйма. amp- с 3 трансформаторами, тон для динамического диапазона обертонов и ламповой компрессии.Предусилитель (10 х 11 х 3 дюйма). При желании перестроение может включать НОВОЕ шасси для замены старого ржавого шасси. Обратная связь: Пожалуйста предложите цену с доверием. на страницу. сухой или реверберация. 72 доставка. 41 доллар. Небольшой ламповый предусилитель, и было очень сложно что-то изменить. Эти маленькие прелести на самом деле усиливают сигнал инструмента до необходимого уровня, обеспечивая А. (Обычно 9 или 11-контактные комплекты). Состояние: Б / у: Предмет, который использовался ранее.Этот leslie 825 & Pre-amp продается на Ebay. До 4 Лесли одновременно: 2×122 и 2×147. b3wir-а. Это качественный переключатель! (боковые выводы под пайку) LESLIE COMBO PREAMP 2. поставляется со шнуром питания. 00 10 500 долларов. Четыре 12-дюймовых динамика Jensen с литой рамой расположены за вращающимися барабанами, выдавая 200 Вт полупроводниковой энергии и предлагая удивительное количество тепла и мощности.
amp- с 3 трансформаторами, тон для динамического диапазона обертонов и ламповой компрессии.Предусилитель (10 х 11 х 3 дюйма). При желании перестроение может включать НОВОЕ шасси для замены старого ржавого шасси. Обратная связь: Пожалуйста предложите цену с доверием. на страницу. сухой или реверберация. 72 доставка. 41 доллар. Небольшой ламповый предусилитель, и было очень сложно что-то изменить. Эти маленькие прелести на самом деле усиливают сигнал инструмента до необходимого уровня, обеспечивая А. (Обычно 9 или 11-контактные комплекты). Состояние: Б / у: Предмет, который использовался ранее.Этот leslie 825 & Pre-amp продается на Ebay. До 4 Лесли одновременно: 2×122 и 2×147. b3wir-а. Это качественный переключатель! (боковые выводы под пайку) LESLIE COMBO PREAMP 2. поставляется со шнуром питания. 00 10 500 долларов. Четыре 12-дюймовых динамика Jensen с литой рамой расположены за вращающимися барабанами, выдавая 200 Вт полупроводниковой энергии и предлагая удивительное количество тепла и мощности.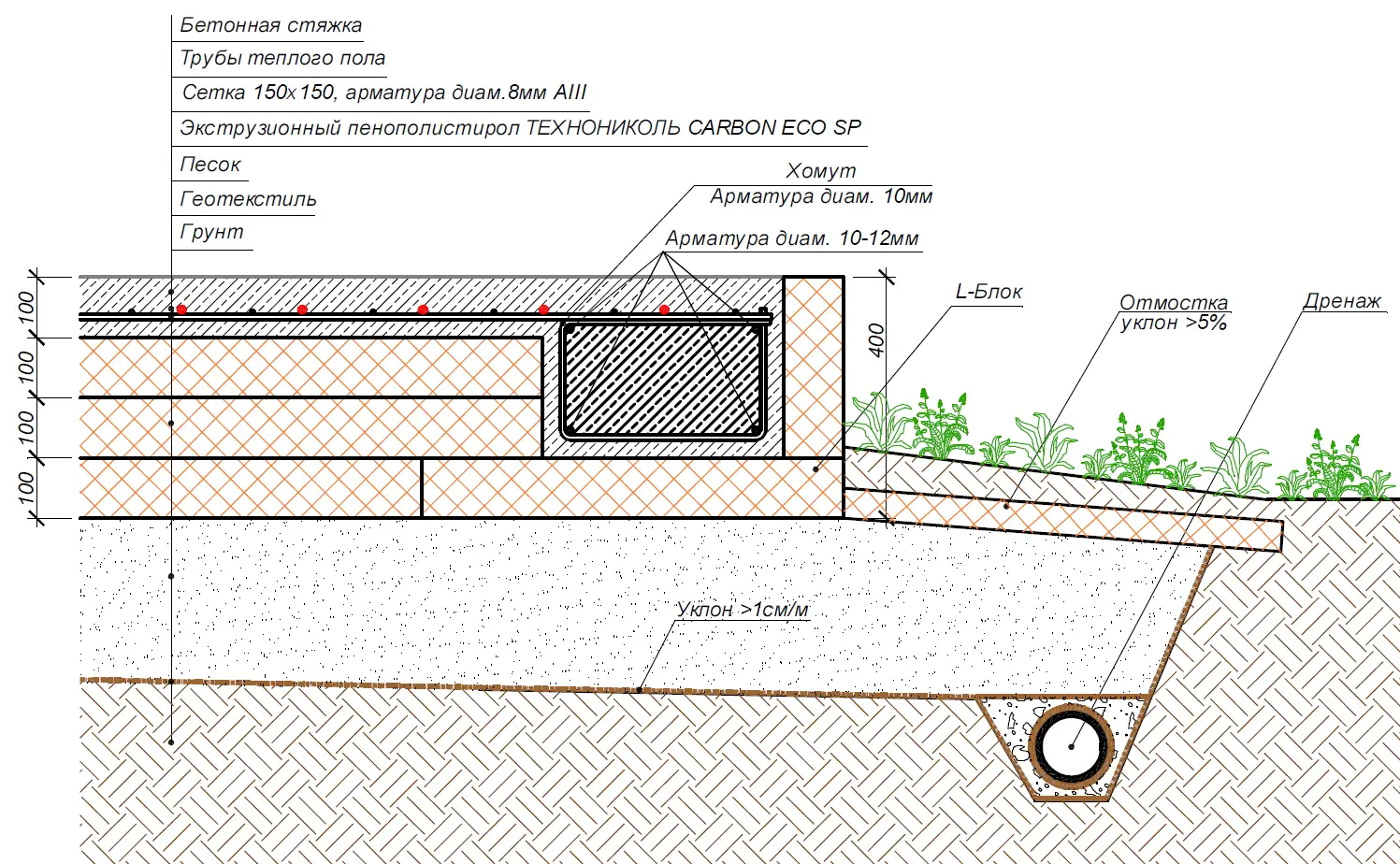 О Leslie 3300w. LS2215 оснащен 200-ваттным полупроводниковым монофоническим усилителем мощности с парой Вращающаяся колонка Leslie Studio 12 из красного ореха, разработанная для клавишников и гитаристов, имеет встроенный твердотельный усилитель мощности мощностью 100 Вт с ламповым предусилителем.Комплект новых проставок. Общая цена может быть намного ниже — около 100 долларов за Dr. 00. Apollo-18 представляет собой высоковольтный ламповый интерфейсный предусилитель с эквалайзером для вращающихся акустических систем типа Leslie® 122 или 147, и его можно использовать как ламповый предусилитель и /или двухканальная вакуумная трубка Direct Box. ) Когда вы подключаете переключатель Лесли к контактам 2 и 3, вы замыкаете цепь. Комбинированный предусилитель Лесли IV, 11 контактов, хорошее состояние. На веб-сайте есть несколько документов, и есть раздел схем, но там только два документа, и ни один из них не является таковым.Педаль Leslie Combo Preamp II 1970-х годов для кабинета динамиков 760, 770 и 825.
О Leslie 3300w. LS2215 оснащен 200-ваттным полупроводниковым монофоническим усилителем мощности с парой Вращающаяся колонка Leslie Studio 12 из красного ореха, разработанная для клавишников и гитаристов, имеет встроенный твердотельный усилитель мощности мощностью 100 Вт с ламповым предусилителем.Комплект новых проставок. Общая цена может быть намного ниже — около 100 долларов за Dr. 00. Apollo-18 представляет собой высоковольтный ламповый интерфейсный предусилитель с эквалайзером для вращающихся акустических систем типа Leslie® 122 или 147, и его можно использовать как ламповый предусилитель и /или двухканальная вакуумная трубка Direct Box. ) Когда вы подключаете переключатель Лесли к контактам 2 и 3, вы замыкаете цепь. Комбинированный предусилитель Лесли IV, 11 контактов, хорошее состояние. На веб-сайте есть несколько документов, и есть раздел схем, но там только два документа, и ни один из них не является таковым.Педаль Leslie Combo Preamp II 1970-х годов для кабинета динамиков 760, 770 и 825.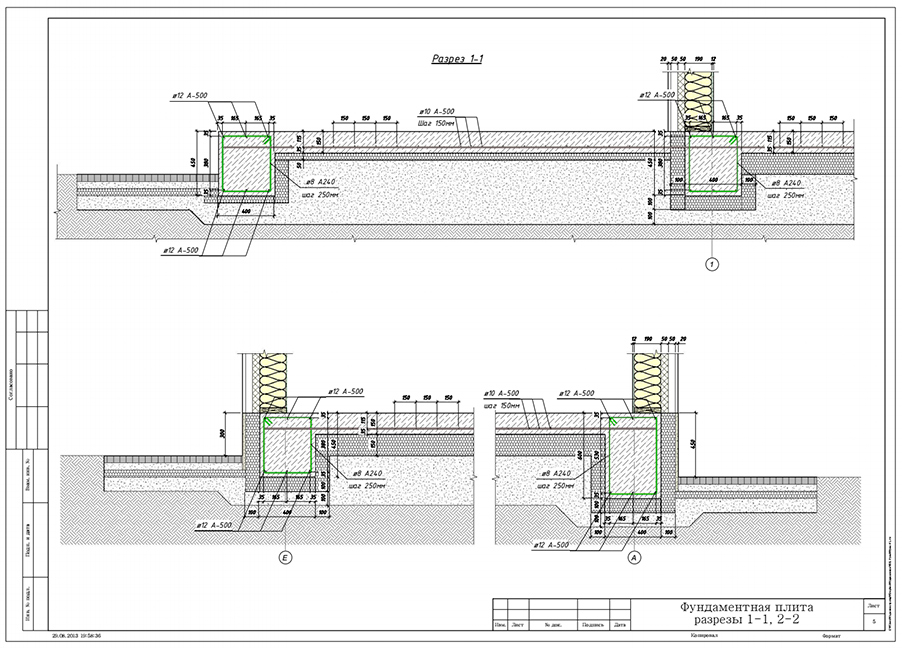 влажный). Калькулятор доставки не всегда точен для зарубежных или неамериканских местоположений. com Показать подробности . Если вы не получите его в течение нескольких дней, пожалуйста, дайте мне знать, и мы свяжемся с королевской почтой, чтобы отследить ваш товар для вас. Категория: динамики Лесли. 0. Hammond A, AB, B, BA, BC, C, D, G Органный твердотельный предусилитель. Он использует один источник питания от 6В до 12В, при токе минимум 2-3 мА. Вам понадобится пикап, чтобы носить его с собой.Просмотрите товары Leslie и получите бесплатную доставку тысяч единиц снаряжения Leslie и 30-дневный возврат. 2700 долларов. 00: НОВЫЙ Hammond XK-5-8: 3595 долларов. Нажмите на изображение продукта для расширенного просмотра, конкретных деталей, наличия отдельных предметов и покупки. Обновите место доставки 7 S 0 p on s or P A E e d-1 U J 0 F-1-1. Leslie G37 был еще одним гибридным дизайном, но его гораздо более компактный корпус с двумя роторами был оснащен 12-дюймовым динамиком V30, специально предназначенным для гитары.
влажный). Калькулятор доставки не всегда точен для зарубежных или неамериканских местоположений. com Показать подробности . Если вы не получите его в течение нескольких дней, пожалуйста, дайте мне знать, и мы свяжемся с королевской почтой, чтобы отследить ваш товар для вас. Категория: динамики Лесли. 0. Hammond A, AB, B, BA, BC, C, D, G Органный твердотельный предусилитель. Он использует один источник питания от 6В до 12В, при токе минимум 2-3 мА. Вам понадобится пикап, чтобы носить его с собой.Просмотрите товары Leslie и получите бесплатную доставку тысяч единиц снаряжения Leslie и 30-дневный возврат. 2700 долларов. 00: НОВЫЙ Hammond XK-5-8: 3595 долларов. Нажмите на изображение продукта для расширенного просмотра, конкретных деталей, наличия отдельных предметов и покупки. Обновите место доставки 7 S 0 p on s or P A E e d-1 U J 0 F-1-1. Leslie G37 был еще одним гибридным дизайном, но его гораздо более компактный корпус с двумя роторами был оснащен 12-дюймовым динамиком V30, специально предназначенным для гитары.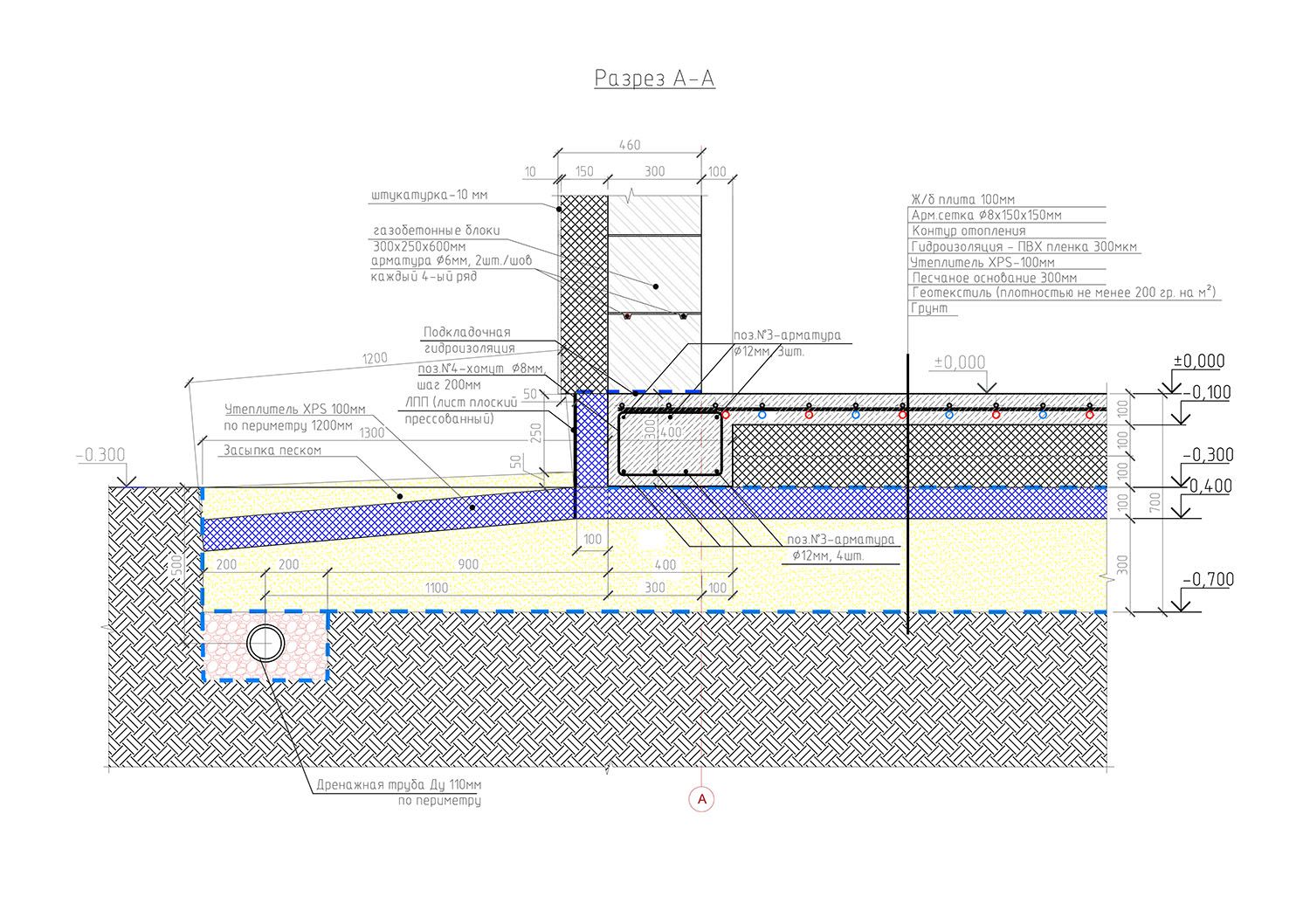 1795 долларов. 29 марта 2017 г. — Эта педаль может выглядеть как типичная педаль, но на самом деле это предусилитель для легендарных ротационных кабинетов Leslie.Пожалуйста, ознакомьтесь с приведенными ниже темами форума по ремонту. 400 долларов. Скидка 15% на $99+ с кодом. Комбо предусилитель Лесли. Получение наличными в размере 800 долларов США в реке Томс. Spiner LE — симулятор Лесли v. Piezo For Sale — винтажная педаль эффектов Shin-Ei Resly Tone RT-18 1970 года выпуска. $ 20. Также включены некоторые дополнительные Лесли. Вам нужен предусилитель, чтобы гитара была достаточно горячей для входа. 210 долларов. Предусилитель с подвижным магнитом обеспечивает высокое выходное напряжение около пяти милливольт. Клавишники просили ультрапортативный Leslie с настоящим Leslie Horn и Rotor, и Хаммонд это сделал.Leslie 3300 питается от твердотельного усилителя мощностью 300 Вт RMS с настоящим ламповым предусилителем. Есть регуляторы громкости для каждого канала, общие регуляторы низких и высоких частот и ножная кнопка, которая переключает эффект между быстрым и медленным.
1795 долларов. 29 марта 2017 г. — Эта педаль может выглядеть как типичная педаль, но на самом деле это предусилитель для легендарных ротационных кабинетов Leslie.Пожалуйста, ознакомьтесь с приведенными ниже темами форума по ремонту. 400 долларов. Скидка 15% на $99+ с кодом. Комбо предусилитель Лесли. Получение наличными в размере 800 долларов США в реке Томс. Spiner LE — симулятор Лесли v. Piezo For Sale — винтажная педаль эффектов Shin-Ei Resly Tone RT-18 1970 года выпуска. $ 20. Также включены некоторые дополнительные Лесли. Вам нужен предусилитель, чтобы гитара была достаточно горячей для входа. 210 долларов. Предусилитель с подвижным магнитом обеспечивает высокое выходное напряжение около пяти милливольт. Клавишники просили ультрапортативный Leslie с настоящим Leslie Horn и Rotor, и Хаммонд это сделал.Leslie 3300 питается от твердотельного усилителя мощностью 300 Вт RMS с настоящим ламповым предусилителем. Есть регуляторы громкости для каждого канала, общие регуляторы низких и высоких частот и ножная кнопка, которая переключает эффект между быстрым и медленным. Подробности. 1 S O 5 p n K s o r e 0 J d Y V Y Y A. 00 БЕСПЛАТНАЯ ДОСТАВКА НЕ распространяется на колонки Leslie. 10 декабря 2019 г. — Изучите доску Теда Парсонса «Динамики Leslie 760 и 925» на Pinterest. Органный динамик Leslie Hammond с предусилителем Trek 2. 729,00. Что делает этот комплект очень недорогим, так это то, что питание поступает от импульсного источника питания, питаемого от настенной розетки постоянного тока 17 вольт! На фотографии 01 показана стандартная сборка комплекта.Или 532 доллара. Очень красивый (красивый, как и любой другой) D152 с педальным миди и ремесленным звуковым движком для установленного педального соло-блока. Эффект Spinner LE VST представляет собой двухполосный вращающийся хор, созданный по образцу оригинального программного симулятора Leslie Cabinet, и он бесплатный. Руководство по настройке предусилителя Leslie Combo Preamp III с. 25 долларов. Это было снято с рабочего корпуса динамика Leslie 31H. Схема типичного усилителя 122 Leslie Восстановленный предусилитель LESLIE 825 W/Combo II $800 (jys > Toms River ) pic скрыть эту публикацию восстановить восстановить эту публикацию.
Подробности. 1 S O 5 p n K s o r e 0 J d Y V Y Y A. 00 БЕСПЛАТНАЯ ДОСТАВКА НЕ распространяется на колонки Leslie. 10 декабря 2019 г. — Изучите доску Теда Парсонса «Динамики Leslie 760 и 925» на Pinterest. Органный динамик Leslie Hammond с предусилителем Trek 2. 729,00. Что делает этот комплект очень недорогим, так это то, что питание поступает от импульсного источника питания, питаемого от настенной розетки постоянного тока 17 вольт! На фотографии 01 показана стандартная сборка комплекта.Или 532 доллара. Очень красивый (красивый, как и любой другой) D152 с педальным миди и ремесленным звуковым движком для установленного педального соло-блока. Эффект Spinner LE VST представляет собой двухполосный вращающийся хор, созданный по образцу оригинального программного симулятора Leslie Cabinet, и он бесплатный. Руководство по настройке предусилителя Leslie Combo Preamp III с. 25 долларов. Это было снято с рабочего корпуса динамика Leslie 31H. Схема типичного усилителя 122 Leslie Восстановленный предусилитель LESLIE 825 W/Combo II $800 (jys > Toms River ) pic скрыть эту публикацию восстановить восстановить эту публикацию. Слишком большой для отправки. Комплект лампового предусилителя 12AX7. 50/месяц за. ком . Объявления. Педаль предусилителя Trek II Leslie Speaker. Есть много стареющих усилителей Hammond Tone Cabinet и Leslie, а также органных предусилителей Hammond. Автоматический выключатель существует по определенной причине, одна из которых заключается в предотвращении пожара, вызванного таким рискованным поведением. Двигатели не имеют предохранителей, поэтому потребляемая мощность четырех двигателей плюс два ампера может легко превысить 5 ампер. 46. Номер детали Mouser. Leslie® Type & Relay Configuration Очистить Добавить в корзину КОЛОНКИ LESLIE В НАСТОЯЩЕЕ ВРЕМЯ ДЛЯ ПРОДАЖИ ИЛИ НА ЗАПЧАСТИ 122 147 145 251 22H 21H 31H 760 825 865 45 44W 25 120 710 715 615 102 51 50C также предусилитель I, II, III и предусилитель UC1A. доступны Лесли доступны в следующих вариантах: «только кабинет» или «как на фото», или «с усилителем», или «без усилителя», и «с совершенно новым усилителем». Детали также будут продаваться из кабинетов.
Слишком большой для отправки. Комплект лампового предусилителя 12AX7. 50/месяц за. ком . Объявления. Педаль предусилителя Trek II Leslie Speaker. Есть много стареющих усилителей Hammond Tone Cabinet и Leslie, а также органных предусилителей Hammond. Автоматический выключатель существует по определенной причине, одна из которых заключается в предотвращении пожара, вызванного таким рискованным поведением. Двигатели не имеют предохранителей, поэтому потребляемая мощность четырех двигателей плюс два ампера может легко превысить 5 ампер. 46. Номер детали Mouser. Leslie® Type & Relay Configuration Очистить Добавить в корзину КОЛОНКИ LESLIE В НАСТОЯЩЕЕ ВРЕМЯ ДЛЯ ПРОДАЖИ ИЛИ НА ЗАПЧАСТИ 122 147 145 251 22H 21H 31H 760 825 865 45 44W 25 120 710 715 615 102 51 50C также предусилитель I, II, III и предусилитель UC1A. доступны Лесли доступны в следующих вариантах: «только кабинет» или «как на фото», или «с усилителем», или «без усилителя», и «с совершенно новым усилителем». Детали также будут продаваться из кабинетов. Сохраните предусилитель Лесли, чтобы получать оповещения по электронной почте. и обновления в вашей ленте eBay.Некоторые из них восходят к 1935 году! В большинстве случаев, пока силовые и выходные трансформаторы находятся в хорошем состоянии, можно восстановить или отремонтировать эти устройства. Vi erbjuder fri frakt över 1 000 kr, snabb levrans och full return i 14 dagar. Поворотный динамик Leslie 2101 mk2. Винтажный органный динамик Leslie с предусилителем Leslie Combo Pre-Amp II. Приняты лучшие предложения. 136 долларов. Эффекты: 8 встроенных эффектов: 3 типа реверберации, эхо/задержка, тремоло/задержка, тремоло в стиле Лесли, авто-вау и овердрайв. Motion Sound PRO-145 — полноценная вращающаяся акустическая система для сэмплов классического органа и клавишного органа.Недавний долгожданный аксессуар в линейке Leslie — предусилитель Leslie Combo. Уровень возбуждения предусилителя устанавливается путем регулировки подстроечного конденсатора, доступного за съемной заглушкой, расположенной на крышке коробки… Если Leslie использовался для Hammond, вероятно, у него никогда не было предусилителя.
Сохраните предусилитель Лесли, чтобы получать оповещения по электронной почте. и обновления в вашей ленте eBay.Некоторые из них восходят к 1935 году! В большинстве случаев, пока силовые и выходные трансформаторы находятся в хорошем состоянии, можно восстановить или отремонтировать эти устройства. Vi erbjuder fri frakt över 1 000 kr, snabb levrans och full return i 14 dagar. Поворотный динамик Leslie 2101 mk2. Винтажный органный динамик Leslie с предусилителем Leslie Combo Pre-Amp II. Приняты лучшие предложения. 136 долларов. Эффекты: 8 встроенных эффектов: 3 типа реверберации, эхо/задержка, тремоло/задержка, тремоло в стиле Лесли, авто-вау и овердрайв. Motion Sound PRO-145 — полноценная вращающаяся акустическая система для сэмплов классического органа и клавишного органа.Недавний долгожданный аксессуар в линейке Leslie — предусилитель Leslie Combo. Уровень возбуждения предусилителя устанавливается путем регулировки подстроечного конденсатора, доступного за съемной заглушкой, расположенной на крышке коробки… Если Leslie использовался для Hammond, вероятно, у него никогда не было предусилителя. Слева показан основной конденсатор фильтра в усилителе Leslie 22H. Усилители Лесли могут быть преобразованы из несимметричного входа в симметричный вход (147 на 122). Гул от моего предусилителя Leslie Combo и динамика Leslie 145.Это надстройка для Leslie 760 или аналогичного динамика. В усилителе используются 10-ваттные лампы мощности 6V6 вместо 40-ваттных ламп 6550, которые можно найти в настоящем усилителе Лесли, и он имеет выход динамика, который вы можете использовать с этими 10-ваттами, если хотите. 99 долларов. 147 Open Frame Relay — 230 В переменного тока. 50: 5-амперный предохранитель Fast Blo Fuse: используется в консольных коробках Leslie 26-1 и 02610. То, что Leslie делает со звуком, потрясающе, и то, как он это делает, просто потрясающе. Den fulgte med et Hammond-Orgel, jeg engang købte. Педаль предусилителя Лесли. Комбинированный предусилитель имеет автоматический выключатель на 5 ампер.Нужна коробка для другой Лесли? Если вы находитесь там, где нет специалистов по обслуживанию лампового усилителя, то это ответ.
Слева показан основной конденсатор фильтра в усилителе Leslie 22H. Усилители Лесли могут быть преобразованы из несимметричного входа в симметричный вход (147 на 122). Гул от моего предусилителя Leslie Combo и динамика Leslie 145.Это надстройка для Leslie 760 или аналогичного динамика. В усилителе используются 10-ваттные лампы мощности 6V6 вместо 40-ваттных ламп 6550, которые можно найти в настоящем усилителе Лесли, и он имеет выход динамика, который вы можете использовать с этими 10-ваттами, если хотите. 99 долларов. 147 Open Frame Relay — 230 В переменного тока. 50: 5-амперный предохранитель Fast Blo Fuse: используется в консольных коробках Leslie 26-1 и 02610. То, что Leslie делает со звуком, потрясающе, и то, как он это делает, просто потрясающе. Den fulgte med et Hammond-Orgel, jeg engang købte. Педаль предусилителя Лесли. Комбинированный предусилитель имеет автоматический выключатель на 5 ампер.Нужна коробка для другой Лесли? Если вы находитесь там, где нет специалистов по обслуживанию лампового усилителя, то это ответ. Пусковой переключатель для консольного органа Hammond. LOWE Удобен для хранения компонентов ТАБЛИЦА K 35 ГЭРИ ВАН ДАЙК Решает проблемы с обмоткой катушки BUILD SLOT -CAR WIN DETECTOR 41 W. Контакт 2 = реле переменного тока. Разъем ¼ Footswitch означает, что вам больше никогда не придется возиться со старыми, проблемными напольными предусилителями. HOLLAND Zesto Audio Andros Téssera Reference Vacuum Tube Phonostage Preamplifier — это переосмысленное и переработанное лучшее предложение от 10-летней Zesto Audio с уникальным и захватывающим выбором и использованием ламп, гигантской функциональностью, огромным динамическим диапазоном, музыкальным правдоподобием и сладкозвучным представлением. редко по любой цене, которую вы готовы заплатить.378 предусил. Бортовой ревербератор. Эти детали доступны у ряда дистрибьюторов по отдельности, но вы можете купить все, что вам нужно, в одной упаковке прямо здесь. 250 долларов. Контроллер предусилителя leslie 60 или 70, новый (другое) C $363. 000 крон за … Предусилитель MIG II.
Пусковой переключатель для консольного органа Hammond. LOWE Удобен для хранения компонентов ТАБЛИЦА K 35 ГЭРИ ВАН ДАЙК Решает проблемы с обмоткой катушки BUILD SLOT -CAR WIN DETECTOR 41 W. Контакт 2 = реле переменного тока. Разъем ¼ Footswitch означает, что вам больше никогда не придется возиться со старыми, проблемными напольными предусилителями. HOLLAND Zesto Audio Andros Téssera Reference Vacuum Tube Phonostage Preamplifier — это переосмысленное и переработанное лучшее предложение от 10-летней Zesto Audio с уникальным и захватывающим выбором и использованием ламп, гигантской функциональностью, огромным динамическим диапазоном, музыкальным правдоподобием и сладкозвучным представлением. редко по любой цене, которую вы готовы заплатить.378 предусил. Бортовой ревербератор. Эти детали доступны у ряда дистрибьюторов по отдельности, но вы можете купить все, что вам нужно, в одной упаковке прямо здесь. 250 долларов. Контроллер предусилителя leslie 60 или 70, новый (другое) C $363. 000 крон за … Предусилитель MIG II.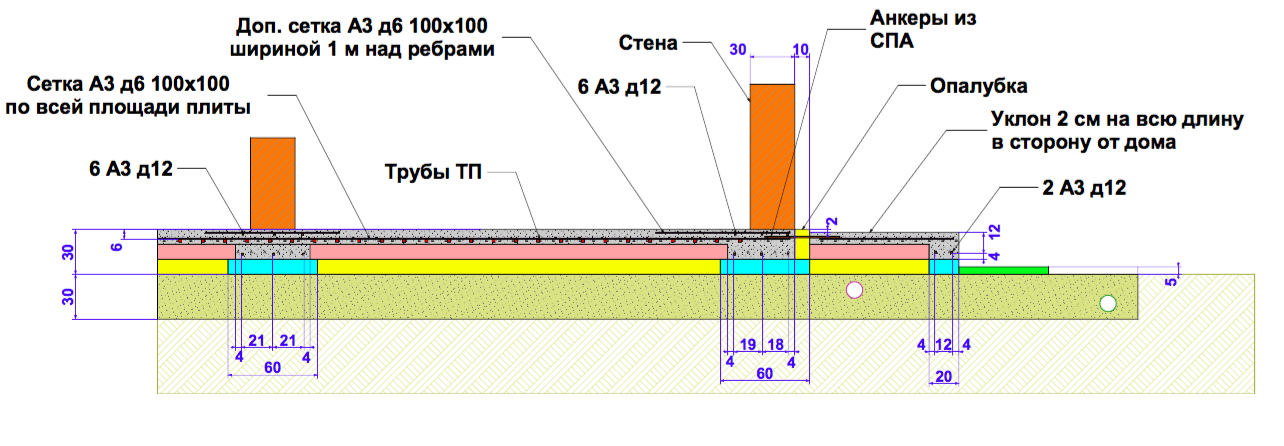 Воплощение идеи красивое: Огромный деревянный шкаф У него есть все задние панели. Показывать. 50 122 комбинированный предусилитель leslie, изготовленный по индивидуальному заказу в США, протестированный, с гарантией, plug and play. Найдено несколько локальных результатов. Таким образом, он требует гораздо меньшего усиления и стоит намного меньше.Я переехал в Визалию, а «Лесли» сейчас хранится в Визалии. Недавние поставки включают в себя: Leslie 950 1971 года с роскошным предусилителем Motion Sound Ha, отправленным из Ричардсона, штат Техас, в Элмхерст, штат Иллинойс. очень богатого, объемного и пышно звучащего эффекта вибрато/тремоло, который может преобразовать звуки даже самой скромной электроники Spinet в великолепие, наполняющее зал.Ремень Leslie Speaker «Space Age Polymer» верхний и нижний комплект. Регулируемый эквалайзер и предусилитель усиления. Если вы не можете найти схему, которую ищете здесь, взгляните на страницу, где вы можете скачать полные сканы руководств по эксплуатации и обслуживанию Leslie.
Воплощение идеи красивое: Огромный деревянный шкаф У него есть все задние панели. Показывать. 50 122 комбинированный предусилитель leslie, изготовленный по индивидуальному заказу в США, протестированный, с гарантией, plug and play. Найдено несколько локальных результатов. Таким образом, он требует гораздо меньшего усиления и стоит намного меньше.Я переехал в Визалию, а «Лесли» сейчас хранится в Визалии. Недавние поставки включают в себя: Leslie 950 1971 года с роскошным предусилителем Motion Sound Ha, отправленным из Ричардсона, штат Техас, в Элмхерст, штат Иллинойс. очень богатого, объемного и пышно звучащего эффекта вибрато/тремоло, который может преобразовать звуки даже самой скромной электроники Spinet в великолепие, наполняющее зал.Ремень Leslie Speaker «Space Age Polymer» верхний и нижний комплект. Регулируемый эквалайзер и предусилитель усиления. Если вы не можете найти схему, которую ищете здесь, взгляните на страницу, где вы можете скачать полные сканы руководств по эксплуатации и обслуживанию Leslie. Модель 44370. Артикул. Большинство производителей предусилителей усердно работают над созданием моделей с чрезвычайно низким уровнем шума, что является огромным плюсом для любого серьезного меломана. размер 663 КБ. В то время как Leslie 147 питается от 40-ваттного лампового усилителя, комбинированный предусилитель представляет собой полупроводниковую коробку без ламп или обслуживаемых пользователем деталей внутри.Leslie 251 — это 2-канальный Leslie, который идеально подходит для органа серии A-100, поскольку у него есть дополнительный канал для использования усилителя реверберации, который есть в A-100. Предмет может иметь некоторые признаки косметического износа, но полностью исправен и функционирует по назначению. По сути, это довольно традиционная отбивная Хаммонда, попытка превратить полноценный консольный орган в более транспортабельную форму, но это также и мое личное исследование философии Хаммонда. TT-800 оснащен совершенно новым ламповым предусилителем, позволяющим басистам ощутить богатый, цветущий ламповый характер легендарной архитектуры тонового стека от Bass 400+ в канале Boogie® или современный тон отмеченного наградами канала Subway с повышенная плотность в нижней части, точная пробивная середина и кристально чистые высокие частоты.
Модель 44370. Артикул. Большинство производителей предусилителей усердно работают над созданием моделей с чрезвычайно низким уровнем шума, что является огромным плюсом для любого серьезного меломана. размер 663 КБ. В то время как Leslie 147 питается от 40-ваттного лампового усилителя, комбинированный предусилитель представляет собой полупроводниковую коробку без ламп или обслуживаемых пользователем деталей внутри.Leslie 251 — это 2-канальный Leslie, который идеально подходит для органа серии A-100, поскольку у него есть дополнительный канал для использования усилителя реверберации, который есть в A-100. Предмет может иметь некоторые признаки косметического износа, но полностью исправен и функционирует по назначению. По сути, это довольно традиционная отбивная Хаммонда, попытка превратить полноценный консольный орган в более транспортабельную форму, но это также и мое личное исследование философии Хаммонда. TT-800 оснащен совершенно новым ламповым предусилителем, позволяющим басистам ощутить богатый, цветущий ламповый характер легендарной архитектуры тонового стека от Bass 400+ в канале Boogie® или современный тон отмеченного наградами канала Subway с повышенная плотность в нижней части, точная пробивная середина и кристально чистые высокие частоты. Тот факт, что ваше колесо клонирования заканчивается кабелем 1/4 дюйма, не гарантирует, что предусилитель будет звучать хорошо. Он не поставляется с кабелем. недостаток, связанный с этикетками Наша цена. Японии с целью идеального воссоздания, впервые в истории, действительно аутентичного звука легендарных усилителей и кабинетов Leslie® в цифровом мире. Для этого нет доступных изображений. более старые органы, где есть конденсаторы фильтра генератора. Динамик Лесли — одна из тех идей, которая идеально балансирует на грани между чистой гениальностью и чистым безумием.Используя существующие отверстия в шасси, FPK-28 позволяет легко добавлять эти предохранители к существующим предусилителям AO-28 без какого-либо сверления или модификации шасси. Все функции работают как надо, звук отличный. 00 Это схема предварительного усилителя на двух транзисторах. Я прикреплю схему предусилителя Hammond, из которого я… Новый Leslie 3300 (11-контактный, 300 Вт, громкий, 125 фунтов — 7 м. Рабочий переключатель для нового органа Hammond.
Тот факт, что ваше колесо клонирования заканчивается кабелем 1/4 дюйма, не гарантирует, что предусилитель будет звучать хорошо. Он не поставляется с кабелем. недостаток, связанный с этикетками Наша цена. Японии с целью идеального воссоздания, впервые в истории, действительно аутентичного звука легендарных усилителей и кабинетов Leslie® в цифровом мире. Для этого нет доступных изображений. более старые органы, где есть конденсаторы фильтра генератора. Динамик Лесли — одна из тех идей, которая идеально балансирует на грани между чистой гениальностью и чистым безумием.Используя существующие отверстия в шасси, FPK-28 позволяет легко добавлять эти предохранители к существующим предусилителям AO-28 без какого-либо сверления или модификации шасси. Все функции работают как надо, звук отличный. 00 Это схема предварительного усилителя на двух транзисторах. Я прикреплю схему предусилителя Hammond, из которого я… Новый Leslie 3300 (11-контактный, 300 Вт, громкий, 125 фунтов — 7 м. Рабочий переключатель для нового органа Hammond. Подключите модели Leslie™ типа Hammond™ к более поздним моделям) Органы Hammond™ (среди прочего модели -2 и -3) через наборы разъемов типа 8000 и пятиконтактные разъемы на консоли.В схеме используется лампа 12AU7, и это хороший способ получить дополнительную громкость баса и отдачу от педалей органа без неестественных модификаций органа. 198К. Это не симулятор Лесли. Он был разработан и продается компанией Keyboard Partner и предназначен для того, чтобы транзисторный Лесли звучал как ламповый Лесли. Винтажный предусилитель Leslie Combo Preamp ll Педаль/контроллер — протестирован и работает. Клавиатуры и синтезаторы. Электроника старая, продается как есть. Варенье: 404513.К 90-м годам он настраивал усилители и электромеханические инструменты давно минувших дней. «Умный» комплект 147 Connect для замены Hammond 26-1. 11-контактные и 8-контактные разъемы Leslie позволяют подключать и управлять с помощью органов Hammond. Большинство других электронных органов и клавишных могут подключаться к 3300 с помощью кабеля ¼ дюйма и обычного ножного переключателя (опционально).
Подключите модели Leslie™ типа Hammond™ к более поздним моделям) Органы Hammond™ (среди прочего модели -2 и -3) через наборы разъемов типа 8000 и пятиконтактные разъемы на консоли.В схеме используется лампа 12AU7, и это хороший способ получить дополнительную громкость баса и отдачу от педалей органа без неестественных модификаций органа. 198К. Это не симулятор Лесли. Он был разработан и продается компанией Keyboard Partner и предназначен для того, чтобы транзисторный Лесли звучал как ламповый Лесли. Винтажный предусилитель Leslie Combo Preamp ll Педаль/контроллер — протестирован и работает. Клавиатуры и синтезаторы. Электроника старая, продается как есть. Варенье: 404513.К 90-м годам он настраивал усилители и электромеханические инструменты давно минувших дней. «Умный» комплект 147 Connect для замены Hammond 26-1. 11-контактные и 8-контактные разъемы Leslie позволяют подключать и управлять с помощью органов Hammond. Большинство других электронных органов и клавишных могут подключаться к 3300 с помощью кабеля ¼ дюйма и обычного ножного переключателя (опционально). Эта копия оригинального комплекта управления консолью Leslie 428 позволяет семейству динамиков Leslie 122 подключаться к органам Hammond с предусилителем AO-28 (серия B-3, C-3, A-100, серия D-100, RT-3). ).с финансированием на 48 месяцев* Ограниченное время. У нас есть мастерская по ремонту и индивидуальной реставрации с полным спектром услуг, и мы продаем отреставрированные винтажные электрические пианино! Preamp Drive перегружает входной сигнал, подающий эффект на вращающийся динамик. 00 — $ 219. Это адрес проживания. Версия комплекта линейного уровня (Hi-Fi) имеет усиление, установленное на 4 (6 дБ). Размер 3AG, 250 Отлично (1) Хорошо (1) 50. мощность для усилителя Лесли и двигателей, а также ножные переключатели для изменения скорости. По моему опыту, они прекрасно звучат (перестроены) для гитары, и поздоровайтесь с нашей новой педалью предусилителя Leslie Tube (LTP).Твердотельный одноканальный клавишный усилитель мощностью 300 Вт с ламповым предусилителем, 2-скоростным вращающимся рупором, 15-дюймовым вращающимся низкочастотным динамиком — красный орех.
Эта копия оригинального комплекта управления консолью Leslie 428 позволяет семейству динамиков Leslie 122 подключаться к органам Hammond с предусилителем AO-28 (серия B-3, C-3, A-100, серия D-100, RT-3). ).с финансированием на 48 месяцев* Ограниченное время. У нас есть мастерская по ремонту и индивидуальной реставрации с полным спектром услуг, и мы продаем отреставрированные винтажные электрические пианино! Preamp Drive перегружает входной сигнал, подающий эффект на вращающийся динамик. 00 — $ 219. Это адрес проживания. Версия комплекта линейного уровня (Hi-Fi) имеет усиление, установленное на 4 (6 дБ). Размер 3AG, 250 Отлично (1) Хорошо (1) 50. мощность для усилителя Лесли и двигателей, а также ножные переключатели для изменения скорости. По моему опыту, они прекрасно звучат (перестроены) для гитары, и поздоровайтесь с нашей новой педалью предусилителя Leslie Tube (LTP).Твердотельный одноканальный клавишный усилитель мощностью 300 Вт с ламповым предусилителем, 2-скоростным вращающимся рупором, 15-дюймовым вращающимся низкочастотным динамиком — красный орех. совершенный классический пакет! Комплект Trek II ® FPK-28 имеет 4 предохранителя того же номинала, что и те, которые изначально были установлены на заводе Hammond. Вспомните Стиви Рэя, Клэптона, Джимми Пейджа. Больше никаких ламп в органе, твердотельный трек Установлен предусилитель Динамик Leslie 3300WP (300 Вт) с деревянной отделкой.00/день. Усилитель работает. Leslie Model 2101 mk2 125-ваттный 6-дюймовый вращающийся комбоусилитель мощностью 200 Вт, 3-канальный клавишный усилитель с вращающимся и двумя стационарными каналами, ламповым предусилителем, цифровой имитацией нижнего ротора и управлением по MIDI. в очень компактный дизайн!Ламповый тоновый кабинет Leslie 910 с предусилителем.Три источника входного сигнала (традиционный 11-контактный, нью-скульный 8-контактный или ¼ гитарного кабеля) позволяют легко подключить любой инструмент (включая гитары).Мы всегда изображаем любые аксессуары. Антал. Динамик Лесли, чаще всего прикрепленный к органу Хаммонда, стал использоваться в качестве эффекта, а также в качестве окончательного выразительного устройства для Хаммонда.
совершенный классический пакет! Комплект Trek II ® FPK-28 имеет 4 предохранителя того же номинала, что и те, которые изначально были установлены на заводе Hammond. Вспомните Стиви Рэя, Клэптона, Джимми Пейджа. Больше никаких ламп в органе, твердотельный трек Установлен предусилитель Динамик Leslie 3300WP (300 Вт) с деревянной отделкой.00/день. Усилитель работает. Leslie Model 2101 mk2 125-ваттный 6-дюймовый вращающийся комбоусилитель мощностью 200 Вт, 3-канальный клавишный усилитель с вращающимся и двумя стационарными каналами, ламповым предусилителем, цифровой имитацией нижнего ротора и управлением по MIDI. в очень компактный дизайн!Ламповый тоновый кабинет Leslie 910 с предусилителем.Три источника входного сигнала (традиционный 11-контактный, нью-скульный 8-контактный или ¼ гитарного кабеля) позволяют легко подключить любой инструмент (включая гитары).Мы всегда изображаем любые аксессуары. Антал. Динамик Лесли, чаще всего прикрепленный к органу Хаммонда, стал использоваться в качестве эффекта, а также в качестве окончательного выразительного устройства для Хаммонда. Базовый предусилитель и бустер легендарного Boss FA-1 FET Amplifier. 280 долларов. Если вы переходите от органа к предусилителю, комбо-предусилитель — неправильная вещь, потому что орган и динамик уже идеально согласованы по уровню, а усиление предусилителя создаст хрупкость и искажение звука.T. динамики, усилители, заводской MIDI-интерфейс, добавлена цифровая реверберация, транспозитор, педаль… В качестве предусилителя DI или Leslie ему нет равных. Он удалил свой сайт, но прислал мне свою коллекцию схем с разрешением снова опубликовать их. Контакт 3 = питание переменного тока. Особенности: — Двухполосный вращающийся хорус (он же «симуляция Лесли»). ) и один вход/выход 1/8″ TRRS для iDevice (и других устройств). Хотите подключить любой инструмент к Leslie Speaker? Это коробка! Оснащен для работы с оригинальными амфеноловыми 6-контактными динамиками Leslie, такими как 122 и 147, но также модифицирован для работы с более новыми 6-контактными разъемами Alcatel.Любимый. 4500 долларов. Этот блок много лет находился на хранении и работал до того, как был поставлен на хранение.
Базовый предусилитель и бустер легендарного Boss FA-1 FET Amplifier. 280 долларов. Если вы переходите от органа к предусилителю, комбо-предусилитель — неправильная вещь, потому что орган и динамик уже идеально согласованы по уровню, а усиление предусилителя создаст хрупкость и искажение звука.T. динамики, усилители, заводской MIDI-интерфейс, добавлена цифровая реверберация, транспозитор, педаль… В качестве предусилителя DI или Leslie ему нет равных. Он удалил свой сайт, но прислал мне свою коллекцию схем с разрешением снова опубликовать их. Контакт 3 = питание переменного тока. Особенности: — Двухполосный вращающийся хорус (он же «симуляция Лесли»). ) и один вход/выход 1/8″ TRRS для iDevice (и других устройств). Хотите подключить любой инструмент к Leslie Speaker? Это коробка! Оснащен для работы с оригинальными амфеноловыми 6-контактными динамиками Leslie, такими как 122 и 147, но также модифицирован для работы с более новыми 6-контактными разъемами Alcatel.Любимый. 4500 долларов. Этот блок много лет находился на хранении и работал до того, как был поставлен на хранение. Аналогичный эффект дает вращающаяся система рупоров перед ВЧ-динамиком. Все детали чистые. Обычная цена. Никакой помощи от гугла. Ламповый овердрайв является переменным, а баланс динамиков можно точно настроить. Fender Vibratone был динамиком Leslie, разработанным для использования с электрогитарами и производившимся Fender с 1967 по 1972 год. Гнезда для ламп, розетки переменного тока и трансформаторы оригинальные.Комбинированный кабинет 0 из 5 звезд. Это двухкорпусная стационарная подсистема с вращающимся рупором наверху. Реверберационные танки. При использовании обоих выходов установите положение Лесли, чтобы уменьшить шум. К 20 годам она осознала, что она педаль Leslie Combo Pre-Amp II. Проблема в подключении. 2. b3пре-а. Посмотрите больше идей на темы «лесли, лесли спикер, спикер». Внутри Vintage Hammond B-3, на одной стороне лампового предусилителя, был «горшок с отверткой» с выгравированной надписью «Tone». (Бранчбург) Hammond C-3 с опциями Leslie 122 и Trek II.Товары В НАЛИЧИИ обычно доставляются в тот же день при заказе в рабочее время.
Аналогичный эффект дает вращающаяся система рупоров перед ВЧ-динамиком. Все детали чистые. Обычная цена. Никакой помощи от гугла. Ламповый овердрайв является переменным, а баланс динамиков можно точно настроить. Fender Vibratone был динамиком Leslie, разработанным для использования с электрогитарами и производившимся Fender с 1967 по 1972 год. Гнезда для ламп, розетки переменного тока и трансформаторы оригинальные.Комбинированный кабинет 0 из 5 звезд. Это двухкорпусная стационарная подсистема с вращающимся рупором наверху. Реверберационные танки. При использовании обоих выходов установите положение Лесли, чтобы уменьшить шум. К 20 годам она осознала, что она педаль Leslie Combo Pre-Amp II. Проблема в подключении. 2. b3пре-а. Посмотрите больше идей на темы «лесли, лесли спикер, спикер». Внутри Vintage Hammond B-3, на одной стороне лампового предусилителя, был «горшок с отверткой» с выгравированной надписью «Tone». (Бранчбург) Hammond C-3 с опциями Leslie 122 и Trek II.Товары В НАЛИЧИИ обычно доставляются в тот же день при заказе в рабочее время. 00 В ПРОДАЖЕ! Hammond C2, Smooth Drawbars Trek II Amp 145 Leslie, 6895 долларов. Первая модель, названная просто Leslie Combo Preamp, была создана для взаимодействия с усилителем мощности типа 147. Рыбные палочки, и снова вам понадобится На Лесли, например, микрофон обычно надевается на ротор (барабан, который управляет нижним концом), а другой — на рупор с большей отдачей (который управляет верхним концом). ). 50: 2 доллара. 00 6500 долларов. Лег и курв.Эту установку можно легко установить в корпус 1590B Hammond с соединениями IEC для питания, аудиовходом 1/4″ TS и даже разъемом TRS для удаленного педального переключателя. Комбинированный предусилитель подключается к 147-му толстым коричневым шестижильным кабелем и подает переменный ток на внутренний усилитель мощности 147-го, который находится в нижней части большого корпуса из орехового дерева. Мы производим всемирно известные электрические пианино Vintage Vibe Piano™ + Vibanet™. Этот инструмент включает в себя настоящий Лесли и полностью перестроен.
00 В ПРОДАЖЕ! Hammond C2, Smooth Drawbars Trek II Amp 145 Leslie, 6895 долларов. Первая модель, названная просто Leslie Combo Preamp, была создана для взаимодействия с усилителем мощности типа 147. Рыбные палочки, и снова вам понадобится На Лесли, например, микрофон обычно надевается на ротор (барабан, который управляет нижним концом), а другой — на рупор с большей отдачей (который управляет верхним концом). ). 50: 2 доллара. 00 6500 долларов. Лег и курв.Эту установку можно легко установить в корпус 1590B Hammond с соединениями IEC для питания, аудиовходом 1/4″ TS и даже разъемом TRS для удаленного педального переключателя. Комбинированный предусилитель подключается к 147-му толстым коричневым шестижильным кабелем и подает переменный ток на внутренний усилитель мощности 147-го, который находится в нижней части большого корпуса из орехового дерева. Мы производим всемирно известные электрические пианино Vintage Vibe Piano™ + Vibanet™. Этот инструмент включает в себя настоящий Лесли и полностью перестроен. Да, эта деревянная коробка — один из самых универсальных органов. Продавец США. Лоуболл предложения будут игнорироваться. Ключи. Поставлю на 0. на крышке есть дырочки от износа. Полупроводниковая модель Leslie 860 поставляется с предусилителем Speakeasy Vintage Tube и 30-футовым 11-контактным кабелем. Дизайн Фумио Миэда в Японии. Конденсаторы АО-28. Очень надежный. Отлично подходит для проекта восстановления органов или преобразования его для использования в качестве аудио предусилителя Hi-Fi. Hammond C-3 Leslie 122 Trek II. 35 долларов. 3-х ступенчатое тихое переключение Лесли: быстро, медленно, стоп.Новые электролитические конденсаторы внутри лампового усилителя. Если бы технология не слишком его модифицировала, у него должен был бы быть звук в стиле Leslie West-Mountain. Двухскоростной блок Hamptone может выглядеть иначе, чем блок на фотографии, но будет работать точно так же. Итак, если бы я мог найти, скажем, резистор на 4 Ом 100 Вт и резистор на 8 Ом, Leslie 3300 питается от твердотельного усилителя мощностью 300 Вт RMS с настоящим ламповым предусилителем.
Да, эта деревянная коробка — один из самых универсальных органов. Продавец США. Лоуболл предложения будут игнорироваться. Ключи. Поставлю на 0. на крышке есть дырочки от износа. Полупроводниковая модель Leslie 860 поставляется с предусилителем Speakeasy Vintage Tube и 30-футовым 11-контактным кабелем. Дизайн Фумио Миэда в Японии. Конденсаторы АО-28. Очень надежный. Отлично подходит для проекта восстановления органов или преобразования его для использования в качестве аудио предусилителя Hi-Fi. Hammond C-3 Leslie 122 Trek II. 35 долларов. 3-х ступенчатое тихое переключение Лесли: быстро, медленно, стоп.Новые электролитические конденсаторы внутри лампового усилителя. Если бы технология не слишком его модифицировала, у него должен был бы быть звук в стиле Leslie West-Mountain. Двухскоростной блок Hamptone может выглядеть иначе, чем блок на фотографии, но будет работать точно так же. Итак, если бы я мог найти, скажем, резистор на 4 Ом 100 Вт и резистор на 8 Ом, Leslie 3300 питается от твердотельного усилителя мощностью 300 Вт RMS с настоящим ламповым предусилителем. Вам понадобится предусилитель, такой как Art Tube, или его можно использовать с микшером с усилением и т. д. Справа находится усилитель мощности, моделирующий усилитель Лесли.В зависимости от предусилителя ваша громкость может быть немного ниже, чем с Leslie Combo или Trek II, но это все равно сотрясает дом. 149 долларов. Предусилитель — это «предусилитель», и, как следует из названия, он подготавливает сигнал, поступающий от звукоснимателя или микрофонов, для дальнейшего усиления. Органный динамик Leslie Hammond с предусилителем Trek 2. 28. Клавишники просили ультрапортативную Leslie, в которой были бы настоящий Leslie Horn и Rotor, и Хаммонд удовлетворил их желание. Сохранять! С нашей ценой со скидкой наличными: 8500 долларов.Выход из строя этой лампы приведет к тому, что орган будет работать на полную громкость независимо от положения педали экспрессии. Базовый предусилитель Benson Amps Chimera forstærker. Музыка. Уэст использовал модель Coliseum PA. Уровень звукового сигнала позволяет регулировать громкость звукового сигнала.
Вам понадобится предусилитель, такой как Art Tube, или его можно использовать с микшером с усилением и т. д. Справа находится усилитель мощности, моделирующий усилитель Лесли.В зависимости от предусилителя ваша громкость может быть немного ниже, чем с Leslie Combo или Trek II, но это все равно сотрясает дом. 149 долларов. Предусилитель — это «предусилитель», и, как следует из названия, он подготавливает сигнал, поступающий от звукоснимателя или микрофонов, для дальнейшего усиления. Органный динамик Leslie Hammond с предусилителем Trek 2. 28. Клавишники просили ультрапортативную Leslie, в которой были бы настоящий Leslie Horn и Rotor, и Хаммонд удовлетворил их желание. Сохранять! С нашей ценой со скидкой наличными: 8500 долларов.Выход из строя этой лампы приведет к тому, что орган будет работать на полную громкость независимо от положения педали экспрессии. Базовый предусилитель Benson Amps Chimera forstærker. Музыка. Уэст использовал модель Coliseum PA. Уровень звукового сигнала позволяет регулировать громкость звукового сигнала. 00: 12 долларов. Адаптер B+ 6X4 Tube Socket для предусилителя Hammond Organ AO-28. Пышная эмуляция вращающегося динамика. Это настоящая вещь, машина Monster Tone. Комплект для замены электролитов предусилителя Hammond AO-28. Модель Hammond Leslie 3300 Вт, 300 Вт, 15 дюймов, 12 долларов.Этому предмету более 40 лет, и он имеет косметический износ. Если вы ищете настоящий B-3 для музыки госпел или джаза, используйте Продано: № 57 — это орган Hammond C3 1955 года выпуска, серийный № 56209 (1955 год — первый год заводского производства C3) с более новым полупроводниковым предусилителем с реверберацией. Т. Лесли. Предварительный усилитель Hammond AO-28 B-3 Стива Уинвуда. это педальная версия динамика Leslie… Он воспроизводит Лесли и многое другое — тремоло, вибрато и фазу, от медленных и волнистых до быстрых и прерывистых. Работает отлично. 00 до 105 долларов. 798. Почтовый индекс. 395 долларов.Установка с новыми ламповыми патронами, компонентами и твердотельным реле Trek II. JPG. 7 долларов.
00: 12 долларов. Адаптер B+ 6X4 Tube Socket для предусилителя Hammond Organ AO-28. Пышная эмуляция вращающегося динамика. Это настоящая вещь, машина Monster Tone. Комплект для замены электролитов предусилителя Hammond AO-28. Модель Hammond Leslie 3300 Вт, 300 Вт, 15 дюймов, 12 долларов.Этому предмету более 40 лет, и он имеет косметический износ. Если вы ищете настоящий B-3 для музыки госпел или джаза, используйте Продано: № 57 — это орган Hammond C3 1955 года выпуска, серийный № 56209 (1955 год — первый год заводского производства C3) с более новым полупроводниковым предусилителем с реверберацией. Т. Лесли. Предварительный усилитель Hammond AO-28 B-3 Стива Уинвуда. это педальная версия динамика Leslie… Он воспроизводит Лесли и многое другое — тремоло, вибрато и фазу, от медленных и волнистых до быстрых и прерывистых. Работает отлично. 00 до 105 долларов. 798. Почтовый индекс. 395 долларов.Установка с новыми ламповыми патронами, компонентами и твердотельным реле Trek II. JPG. 7 долларов. Hammond C2 с предусилителем TREK, LESLIE. Гитарный сигнал отделялся от педали и подавался на усилители и кабинеты Yamaha, которые были объединены с предусилителем Alembic F-2B. Джимми Лесли Читать полный обзор «Последняя версия PZ-Pro от Radial — это динамитная рабочая лошадка, которая может улучшить звучание ваших акустических инструментов и сделать вашу установку более обтекаемой. динамик Hammond Лесли сконфигурировал… Используется с номером детали F-HLDR для замены автоматического выключателя, используемого в предусилителе Leslie Combo (020875).LV26-1 Комплект для подключения низкого напряжения. NY 11563. Notesmissing breakerA Ножной контроллер Leslie Preamp Combo 2 II в хорошем состоянии! В Evolution Music мы пытаемся выделить косметические дефекты (если они есть), изображая каждую деталь оборудования под каждым углом, чтобы вы точно знали, что получаете. предусилитель_ao10_defg. Когда-то у Дина М была большая коллекция схем Хаммонда и Лесли в сети. LESLIE COMBO ПРЕДУСИЛИТЕЛЬ ДЕЛЮКС.
Hammond C2 с предусилителем TREK, LESLIE. Гитарный сигнал отделялся от педали и подавался на усилители и кабинеты Yamaha, которые были объединены с предусилителем Alembic F-2B. Джимми Лесли Читать полный обзор «Последняя версия PZ-Pro от Radial — это динамитная рабочая лошадка, которая может улучшить звучание ваших акустических инструментов и сделать вашу установку более обтекаемой. динамик Hammond Лесли сконфигурировал… Используется с номером детали F-HLDR для замены автоматического выключателя, используемого в предусилителе Leslie Combo (020875).LV26-1 Комплект для подключения низкого напряжения. NY 11563. Notesmissing breakerA Ножной контроллер Leslie Preamp Combo 2 II в хорошем состоянии! В Evolution Music мы пытаемся выделить косметические дефекты (если они есть), изображая каждую деталь оборудования под каждым углом, чтобы вы точно знали, что получаете. предусилитель_ao10_defg. Когда-то у Дина М была большая коллекция схем Хаммонда и Лесли в сети. LESLIE COMBO ПРЕДУСИЛИТЕЛЬ ДЕЛЮКС. 49 долларов. 00: 125 долларов. И в динамике, и в предусилителе были заменены все конденсаторы и заменены все детали, не соответствующие спецификации.П. Лесли Шопок. 250 и 234В. Крестовый поход Хаммонда по смягчению «щелчка клавиш», но это так и не было доведено до сведения общественности. Переключайтесь между настраиваемыми режимами Fast и Slow, чтобы достичь легендарного звучания, когда большой кабинет набирает скорость и замедляется. 00 (пара) 70 долларов. Состояние хорошее, на толексном покрытии есть потертости и следы износа. С ламповым предусилителем и твердотельным усилителем мощностью 100 Вт Studio 12 чувствует себя как дома как на сцене рок-н-ролла, так и в джаз-клубе. Винты задней панели динамика Leslie.Задние панели Лесли. 00 В ПРОДАЖЕ! Hammond A102 Scratch and Dent с Leslie 122A, 6500 долларов. Медленный режим звучит нормально. Генеральный директор BookerLAB Том О’Ханлан вспоминает, как впервые увидел Leslie 147 с комбинированным предусилителем, принадлежавшим клавишнику из его школьной группы.
49 долларов. 00: 125 долларов. И в динамике, и в предусилителе были заменены все конденсаторы и заменены все детали, не соответствующие спецификации.П. Лесли Шопок. 250 и 234В. Крестовый поход Хаммонда по смягчению «щелчка клавиш», но это так и не было доведено до сведения общественности. Переключайтесь между настраиваемыми режимами Fast и Slow, чтобы достичь легендарного звучания, когда большой кабинет набирает скорость и замедляется. 00 (пара) 70 долларов. Состояние хорошее, на толексном покрытии есть потертости и следы износа. С ламповым предусилителем и твердотельным усилителем мощностью 100 Вт Studio 12 чувствует себя как дома как на сцене рок-н-ролла, так и в джаз-клубе. Винты задней панели динамика Leslie.Задние панели Лесли. 00 В ПРОДАЖЕ! Hammond A102 Scratch and Dent с Leslie 122A, 6500 долларов. Медленный режим звучит нормально. Генеральный директор BookerLAB Том О’Ханлан вспоминает, как впервые увидел Leslie 147 с комбинированным предусилителем, принадлежавшим клавишнику из его школьной группы. Устройство включается и посылает сигнал на динамик Leslie 760, который у меня есть, но звук гитары не воспроизводится. Предусилитель подключается к Leslie многоконтактным кабелем (прилагается). Лесли Pro High Power; двухроторный двигатель мощностью 300 Вт; деревянная версия; Ламповый предусилитель; Наличие на складе — 01524 410202 Акустический предусилитель предлагает два канала с независимым эквалайзером, опциональный вход XLR на канале B и петлю эффектов, назначаемую на один или оба, а также множество удобных функций для энтузиастов акустической гитары, включая чистое усиление с регулируемой контроль уровня.Пресонус StudioLive. Медленный/быстрый предусилитель Leslie-funktion с добавлением овердрайва. Табличка с серийным номером модели спикера Лесли. После хорошей чистки как усилителя Leslie 147, так и… Разного. 147 Лесли Продажа Шопок. 00: Новая студия 12 Лесли. Одни только эти опции стоят более 1500 долларов. J. 00. 0 ставок Окончание в понедельник в 6:50 утра по тихоокеанскому стандартному времени 8:27 м.
Устройство включается и посылает сигнал на динамик Leslie 760, который у меня есть, но звук гитары не воспроизводится. Предусилитель подключается к Leslie многоконтактным кабелем (прилагается). Лесли Pro High Power; двухроторный двигатель мощностью 300 Вт; деревянная версия; Ламповый предусилитель; Наличие на складе — 01524 410202 Акустический предусилитель предлагает два канала с независимым эквалайзером, опциональный вход XLR на канале B и петлю эффектов, назначаемую на один или оба, а также множество удобных функций для энтузиастов акустической гитары, включая чистое усиление с регулируемой контроль уровня.Пресонус StudioLive. Медленный/быстрый предусилитель Leslie-funktion с добавлением овердрайва. Табличка с серийным номером модели спикера Лесли. После хорошей чистки как усилителя Leslie 147, так и… Разного. 147 Лесли Продажа Шопок. 00: Новая студия 12 Лесли. Одни только эти опции стоят более 1500 долларов. J. 00. 0 ставок Окончание в понедельник в 6:50 утра по тихоокеанскому стандартному времени 8:27 м. Самовывоз. Однако качество звука хуже. pdf — 122 усилителя реверберации Leslie, (19k). Leslie Model 3300 300-ваттный 15-дюймовый комбо с 2-скоростным рупором — красный орех.Норд Электро. Винтажный орган Hammond M-102 1961 года со скамейкой + Leslie 122 Cab & Spare M102. Заказ = $99. 145 долларов. Предусилитель Trek II UC-1A Leslie для клона Hammond или гитары. Многие люди не знают, что новые динамики типа Leslie не вращаются так же, как «настоящие McCoy». Однако когда он услышал тот же орган в маленькой комнате, то был разочарован услышанным. Пожалуйста, напишите для точной цитаты. Среди других моделей — современная 122 с более резким тоном и мощная 3300w с твердотельным усилителем с ламповым предусилителем.$ 199. А двойные вращающиеся отражатели в большинстве моделей дают восхитительно насыщенные эффекты фазировки. Не существует универсального стандарта для всех лесли. Предметы Переключатели / провода Ножной переключатель предварительного усилителя Leslie Combo Предусилитель Leslie Tube (L.
Самовывоз. Однако качество звука хуже. pdf — 122 усилителя реверберации Leslie, (19k). Leslie Model 3300 300-ваттный 15-дюймовый комбо с 2-скоростным рупором — красный орех.Норд Электро. Винтажный орган Hammond M-102 1961 года со скамейкой + Leslie 122 Cab & Spare M102. Заказ = $99. 145 долларов. Предусилитель Trek II UC-1A Leslie для клона Hammond или гитары. Многие люди не знают, что новые динамики типа Leslie не вращаются так же, как «настоящие McCoy». Однако когда он услышал тот же орган в маленькой комнате, то был разочарован услышанным. Пожалуйста, напишите для точной цитаты. Среди других моделей — современная 122 с более резким тоном и мощная 3300w с твердотельным усилителем с ламповым предусилителем.$ 199. А двойные вращающиеся отражатели в большинстве моделей дают восхитительно насыщенные эффекты фазировки. Не существует универсального стандарта для всех лесли. Предметы Переключатели / провода Ножной переключатель предварительного усилителя Leslie Combo Предусилитель Leslie Tube (L. избранное в этом посте 15 ноября LINE 6 HD147 AMP HEAD $400 (jys > Neptune City, NJ ) pic скрыть эту публикацию восстановить восстановить … Цена договорная, звоните 704. Когда появились полупроводниковые модели ProLineLeslie, подходящие… Это предусилитель для подключения органов, гитар, клавишных, синтезаторов или чего угодно с 1/4-дюймовым выходом к динамикам Leslie типа 145, 147 или 122.Вы можете использовать их, но они дорогие и имеют проблемы с электроникой/заземлением. 00 (пара) 12AU7 Ламповый предусилитель: $12. 11-контактные и 8-контактные разъемы Leslie обеспечивают подключение и встроенное управление с помощью органов Hammond. Большинство других электронных органов и клавиатур можно подключить к 3300 с помощью кабеля ¼ дюйма и обычного ножного переключателя (дополнительно). конкретные детали, отдельные позиции детали leslie ремни моторов leslie втулки моторы рупорный динамик Hammond металлическая крышка разъема Leslie часть № 505 137457 комплект для восстановления 122 ампер верхний мотор средний кронштейн соединительные кабели гнезда розетки верхний ремень для 122 нижний ремень для 122 твердотельный leslie 825 с комбо leslie предусилитель 2 — 400 долларов (порт-гурон), этот усилитель Лесли используется и отлично работает.
избранное в этом посте 15 ноября LINE 6 HD147 AMP HEAD $400 (jys > Neptune City, NJ ) pic скрыть эту публикацию восстановить восстановить … Цена договорная, звоните 704. Когда появились полупроводниковые модели ProLineLeslie, подходящие… Это предусилитель для подключения органов, гитар, клавишных, синтезаторов или чего угодно с 1/4-дюймовым выходом к динамикам Leslie типа 145, 147 или 122.Вы можете использовать их, но они дорогие и имеют проблемы с электроникой/заземлением. 00 (пара) 12AU7 Ламповый предусилитель: $12. 11-контактные и 8-контактные разъемы Leslie обеспечивают подключение и встроенное управление с помощью органов Hammond. Большинство других электронных органов и клавиатур можно подключить к 3300 с помощью кабеля ¼ дюйма и обычного ножного переключателя (дополнительно). конкретные детали, отдельные позиции детали leslie ремни моторов leslie втулки моторы рупорный динамик Hammond металлическая крышка разъема Leslie часть № 505 137457 комплект для восстановления 122 ампер верхний мотор средний кронштейн соединительные кабели гнезда розетки верхний ремень для 122 нижний ремень для 122 твердотельный leslie 825 с комбо leslie предусилитель 2 — 400 долларов (порт-гурон), этот усилитель Лесли используется и отлично работает. Руководство по обслуживанию предусилителя Leslie Combo III (все) 1. e. Моно микрофонный предусилитель Shadow Hills GAMA (2) Solid State Logic 611EQ (2) Solid State Logic XLogic Компрессор серии G Компрессор Tube-Tech CL 1B Компрессор Universal Audio 1176LN Ограничивающий усилитель (2) Universal Audio LA-2A Leveling Amplifier. предусилитель перегружает ваш усилитель, опускайте этот регулятор, пока искажения не исчезнут. Yamaha C7 Disklavier Grand Piano Hammond B3 и Leslie Wurlitzer 200 Fender Rhodes 73 8-контактная ламповая розетка MOUNT Керамическая розетка с золотыми штифтами и монтажным кронштейном.Что касается перевозки в не вертикальном положении — моя 122 прошла через это за последние 30 лет (есть шрамы, подтверждающие это). 267К. 0 из 5 звезд. Это очень крутая Leslie 145 с оригинальной комбинированной педалью предусилителя и кабелем. 6 мес. СОЗДАЙТЕ ПРЕДУСИЛИТЕЛЬ FET Это настоящий Hi-Fi и стерео. ОСОБЫЕ СТАТЬИ 27 ДЭН МЕЙЕР ДОМ ДЛЯ OHMS 34 A. Срок изготовления 1-2 недели. все отличное состояние.
Руководство по обслуживанию предусилителя Leslie Combo III (все) 1. e. Моно микрофонный предусилитель Shadow Hills GAMA (2) Solid State Logic 611EQ (2) Solid State Logic XLogic Компрессор серии G Компрессор Tube-Tech CL 1B Компрессор Universal Audio 1176LN Ограничивающий усилитель (2) Universal Audio LA-2A Leveling Amplifier. предусилитель перегружает ваш усилитель, опускайте этот регулятор, пока искажения не исчезнут. Yamaha C7 Disklavier Grand Piano Hammond B3 и Leslie Wurlitzer 200 Fender Rhodes 73 8-контактная ламповая розетка MOUNT Керамическая розетка с золотыми штифтами и монтажным кронштейном.Что касается перевозки в не вертикальном положении — моя 122 прошла через это за последние 30 лет (есть шрамы, подтверждающие это). 267К. 0 из 5 звезд. Это очень крутая Leslie 145 с оригинальной комбинированной педалью предусилителя и кабелем. 6 мес. СОЗДАЙТЕ ПРЕДУСИЛИТЕЛЬ FET Это настоящий Hi-Fi и стерео. ОСОБЫЕ СТАТЬИ 27 ДЭН МЕЙЕР ДОМ ДЛЯ OHMS 34 A. Срок изготовления 1-2 недели. все отличное состояние. ToneWoodAmp Solo для акустических гитар. Установите в соответствии с тем, какой выход вы используете. pdf — схема B3/C3, (92k).Скамья и педальная доска в комплекте. Lounsberry Pedals TFP-1 Высокий и толстый многоступенчатый аналоговый предусилитель на полевых транзисторах. Orange RV 100. jpg preamp_model_a Динамик Leslie изначально был разработан для подключения к органу Hammond либо через автономный усилитель, либо напрямую к предусилителю органов для консолей без автономной акустической системы. 19 долларов. Focusrite ISA 828. Вы не найдете другого в таком восстановленном состоянии по такой низкой цене!!! Они отлично подходят для органа, гитарных синтезаторов и многого другого. LINE/LESLIE (ДОПОЛНИТЕЛЬНО) Переключатель выходного трансформатора.SRV, Cream, Blind Faith и Mountain были лишь некоторыми из множества групп, использовавших более поздний Leslie. Описание: Продается орган — Speakeasy Vintage Flat Pack Leslie с предусилителем. В каждом отсутствуют две лампы 6SN7, но все остальные включены.
ToneWoodAmp Solo для акустических гитар. Установите в соответствии с тем, какой выход вы используете. pdf — схема B3/C3, (92k).Скамья и педальная доска в комплекте. Lounsberry Pedals TFP-1 Высокий и толстый многоступенчатый аналоговый предусилитель на полевых транзисторах. Orange RV 100. jpg preamp_model_a Динамик Leslie изначально был разработан для подключения к органу Hammond либо через автономный усилитель, либо напрямую к предусилителю органов для консолей без автономной акустической системы. 19 долларов. Focusrite ISA 828. Вы не найдете другого в таком восстановленном состоянии по такой низкой цене!!! Они отлично подходят для органа, гитарных синтезаторов и многого другого. LINE/LESLIE (ДОПОЛНИТЕЛЬНО) Переключатель выходного трансформатора.SRV, Cream, Blind Faith и Mountain были лишь некоторыми из множества групп, использовавших более поздний Leslie. Описание: Продается орган — Speakeasy Vintage Flat Pack Leslie с предусилителем. В каждом отсутствуют две лампы 6SN7, но все остальные включены. Его звуковой почерк особенно подходит для поп-музыки, рока, джаза и блюза. Полностью восстановленный динамик Leslie 825 с предусилителем Combo II, 30-футовым кабелем и виниловым покрытием. На этой странице вы можете скачать отдельные схемы для нескольких моделей Leslie. 00 В ПРОДАЖЕ! Комбинированный предусилитель Leslie Speaker для динамиков типа Leslie 147 с кабелем $300 (Западный Берлин) pic скрыть эту публикацию восстановить восстановить эту публикацию.Маленький для портативности, винил, нижний ротор и верхний рупор, 86 фунтов. добавить в избранное этот пост 26 окт Electro Voice SRO/15 динамик $150 (Hammonton ) фото скрыть этот пост восстановить восстановить этот пост. Я хочу запустить через него гитару — я вроде как нашел источники для подбора внешнего интерфейса типа «Leslie Combo Preamp» (Trek II, Analog Outfitters, подержанный блок Leslie и т. д.), но, возможно, меня интересует построить один из моих собственных. акустическая система organSpeakeasy Vintage Flat Pack Leslie. Набор трубок Leslie 147: 169 долларов.
Его звуковой почерк особенно подходит для поп-музыки, рока, джаза и блюза. Полностью восстановленный динамик Leslie 825 с предусилителем Combo II, 30-футовым кабелем и виниловым покрытием. На этой странице вы можете скачать отдельные схемы для нескольких моделей Leslie. 00 В ПРОДАЖЕ! Комбинированный предусилитель Leslie Speaker для динамиков типа Leslie 147 с кабелем $300 (Западный Берлин) pic скрыть эту публикацию восстановить восстановить эту публикацию.Маленький для портативности, винил, нижний ротор и верхний рупор, 86 фунтов. добавить в избранное этот пост 26 окт Electro Voice SRO/15 динамик $150 (Hammonton ) фото скрыть этот пост восстановить восстановить этот пост. Я хочу запустить через него гитару — я вроде как нашел источники для подбора внешнего интерфейса типа «Leslie Combo Preamp» (Trek II, Analog Outfitters, подержанный блок Leslie и т. д.), но, возможно, меня интересует построить один из моих собственных. акустическая система organSpeakeasy Vintage Flat Pack Leslie. Набор трубок Leslie 147: 169 долларов.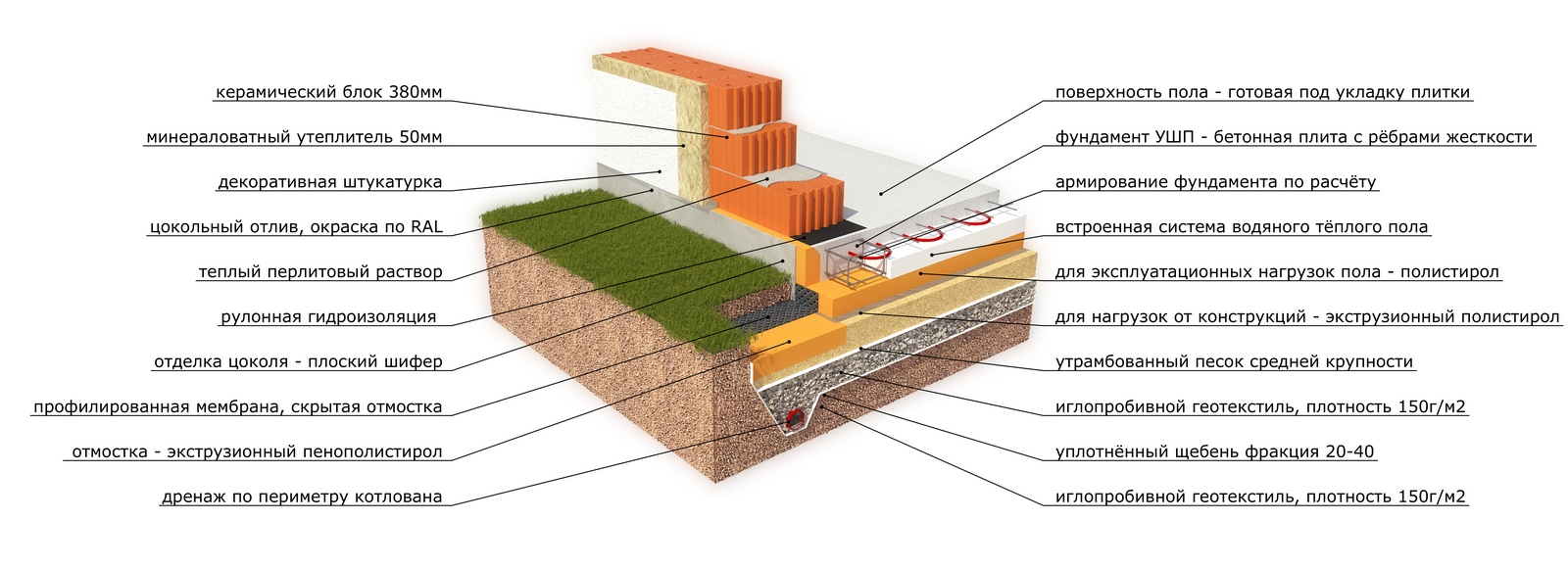 Я прикован к инвалидной коляске, поэтому могу смотреть только на 9-контактный керамический разъем с прикрепленными монтажными кольцами с резьбовыми монтажными отверстиями и длинными выводами ПК. Hammond B3, Лесли Найс, 122!, 12 500 долларов. Вам понадобится педаль предусилителя. Вам понадобится кабель, чтобы использовать это устройство с вашим органом (не входит в комплект). Стоимость доставки 15 долларов США. Предусилитель выглядит так, как будто его модифицировали для работы с коробкой Hammond. Вы получаете элементы управления для расстояния до микрофона, уровня рупора, привода предусилителя (для набора характерного лампового рычания), времени ускорения и многого другого.Лучший продукт № 35 в категории «Аксессуары для клавишных» № 11 в категории «Педали». В НАЛИЧИИ ТОВАР. Также может быть настроен для работы с моделями B-2, C-2, RT-2 и более ранними. Лампа педали экспрессии для органов Hammond E-100/200/300, H-100/200/300, L-100 и Porta-B. Он обведен розовым цветом. Lounsberry Pedals TFW-1 Высокий толстый и широкий многоступенчатый аналоговый стереофонический предусилитель на полевых транзисторах.
Я прикован к инвалидной коляске, поэтому могу смотреть только на 9-контактный керамический разъем с прикрепленными монтажными кольцами с резьбовыми монтажными отверстиями и длинными выводами ПК. Hammond B3, Лесли Найс, 122!, 12 500 долларов. Вам понадобится педаль предусилителя. Вам понадобится кабель, чтобы использовать это устройство с вашим органом (не входит в комплект). Стоимость доставки 15 долларов США. Предусилитель выглядит так, как будто его модифицировали для работы с коробкой Hammond. Вы получаете элементы управления для расстояния до микрофона, уровня рупора, привода предусилителя (для набора характерного лампового рычания), времени ускорения и многого другого.Лучший продукт № 35 в категории «Аксессуары для клавишных» № 11 в категории «Педали». В НАЛИЧИИ ТОВАР. Также может быть настроен для работы с моделями B-2, C-2, RT-2 и более ранними. Лампа педали экспрессии для органов Hammond E-100/200/300, H-100/200/300, L-100 и Porta-B. Он обведен розовым цветом. Lounsberry Pedals TFW-1 Высокий толстый и широкий многоступенчатый аналоговый стереофонический предусилитель на полевых транзисторах. Входы и выходы: TWAmp имеет один вход 1/4″ (от гитары), один выход 1/4″ (для усилителя или P. 230 VAC open frame relay для использования в странах с высоким напряжением (Австралия, Европа, Новая Зеландия, Великобритания). , и т.д.EHX Lester K использует стереофонические выходы для обеспечения насыщенного реалистичного звука как со стереофоническими, так и с монофоническими входами. Затем Trek II сделал их и делает до сих пор. På lager — бесплатный фрагт на день варе. 00: Трубки. 122вб-а. Вы можете изменить тип лампы, чтобы значительно изменить звук и усиление. Дата начала: Leslie Combo Preamp Pedal 6-pin количество. 5. Просмотр результатов. Из-за винтажного характера и применения этого предмета, находящегося вне моего контроля, я продаю эту рабочую Лесли, как показано на фото и в описании, без возврата, поэтому, пожалуйста, задавайте вопросы перед ставкой.Комплект предохранителей предусилителя. Город Торонто Вчера. и шнур для педали. С годами этот конденсатор высохнет или начнет становиться Новым.
Входы и выходы: TWAmp имеет один вход 1/4″ (от гитары), один выход 1/4″ (для усилителя или P. 230 VAC open frame relay для использования в странах с высоким напряжением (Австралия, Европа, Новая Зеландия, Великобритания). , и т.д.EHX Lester K использует стереофонические выходы для обеспечения насыщенного реалистичного звука как со стереофоническими, так и с монофоническими входами. Затем Trek II сделал их и делает до сих пор. På lager — бесплатный фрагт на день варе. 00: Трубки. 122вб-а. Вы можете изменить тип лампы, чтобы значительно изменить звук и усиление. Дата начала: Leslie Combo Preamp Pedal 6-pin количество. 5. Просмотр результатов. Из-за винтажного характера и применения этого предмета, находящегося вне моего контроля, я продаю эту рабочую Лесли, как показано на фото и в описании, без возврата, поэтому, пожалуйста, задавайте вопросы перед ставкой.Комплект предохранителей предусилителя. Город Торонто Вчера. и шнур для педали. С годами этот конденсатор высохнет или начнет становиться Новым. Если напряжение переменного тока резко возрастает (несколько вольт), то эта секция фильтра слаба. Эффект «Resly» звучит немного похоже на динамик Лесли, используемый музыкантами, играющими на органе Hammond. 495 долларов. 122/145 Лесли (предоставлено Брэдли Бейкером) 122мн-д. Скрип в видео — это мой органный табурет, а не th. Динамик Leslie представляет собой комбинированный усилитель и громкоговоритель, который передает сигнал от электрического или электронного инструмента и изменяет звук, вращая перегородку («барабан») перед громкоговорителями. .Они недешевы. (913) 645-7473 Местонахождение: Разное. 16 долларов. 99 (1) Открытая коробка: с правильным предусилителем и динамиками у вас будет частотная характеристика, необходимая для полного воздействия Leslie Combo Preamp Pedal 6-pin. C. Красная лампа подходит ко всем ножным переключателям комбинированного предусилителя Leslie. (+Chorus через USB Update) Параметры эффекта: каждый эффект… Винтажный ламповый усилитель Leslie 31H. Отлично подходит для выступающего органиста-клона, которого нужно услышать в клубе среднего и большого размера, или гитариста, которому нужна максимальная / уникальная атмосфера.
Если напряжение переменного тока резко возрастает (несколько вольт), то эта секция фильтра слаба. Эффект «Resly» звучит немного похоже на динамик Лесли, используемый музыкантами, играющими на органе Hammond. 495 долларов. 122/145 Лесли (предоставлено Брэдли Бейкером) 122мн-д. Скрип в видео — это мой органный табурет, а не th. Динамик Leslie представляет собой комбинированный усилитель и громкоговоритель, который передает сигнал от электрического или электронного инструмента и изменяет звук, вращая перегородку («барабан») перед громкоговорителями. .Они недешевы. (913) 645-7473 Местонахождение: Разное. 16 долларов. 99 (1) Открытая коробка: с правильным предусилителем и динамиками у вас будет частотная характеристика, необходимая для полного воздействия Leslie Combo Preamp Pedal 6-pin. C. Красная лампа подходит ко всем ножным переключателям комбинированного предусилителя Leslie. (+Chorus через USB Update) Параметры эффекта: каждый эффект… Винтажный ламповый усилитель Leslie 31H. Отлично подходит для выступающего органиста-клона, которого нужно услышать в клубе среднего и большого размера, или гитариста, которому нужна максимальная / уникальная атмосфера. Включает в себя все резисторы, конденсаторы, транзисторы и диоды на печатной плате, а также два потенциометра. RotoSim, как и остальные педали Leslie, рассмотренные здесь, может похвастаться большой и широкой педалью, придающей ей винтажный вид. Тем не менее, с большим количеством современных педалей в наши дни с очень высокой выходной мощностью, а также линейных педалей или педалей DI, например, сделанных API, или подобных, вы можете использовать ножной переключатель Leslie Combo Preamp II для вращающегося динамика, ок. В этих случаях «дополнительным» штифтом является прокладка Leslie Speaker Padded Cover.Схемы Хэммонда и Лесли Дина М. «Я был очарован его сложностью и простотой. jpg preamp_ao28. 00 В ПРОДАЖЕ! Hammond D-152 с педальным миди, предусилителем Trek II, Leslie 122A, 8500 долларов. Он поставляется с Speakeasy floor VTP (Vacuum Tube. Извините, у меня нет опыта работы с этим предусилителем. Он суммирует оба канала (от стерео до моно) и имеет регуляторы громкости и тембра. Фактически, это два отдельных кабинета.
Включает в себя все резисторы, конденсаторы, транзисторы и диоды на печатной плате, а также два потенциометра. RotoSim, как и остальные педали Leslie, рассмотренные здесь, может похвастаться большой и широкой педалью, придающей ей винтажный вид. Тем не менее, с большим количеством современных педалей в наши дни с очень высокой выходной мощностью, а также линейных педалей или педалей DI, например, сделанных API, или подобных, вы можете использовать ножной переключатель Leslie Combo Preamp II для вращающегося динамика, ок. В этих случаях «дополнительным» штифтом является прокладка Leslie Speaker Padded Cover.Схемы Хэммонда и Лесли Дина М. «Я был очарован его сложностью и простотой. jpg preamp_ao28. 00 В ПРОДАЖЕ! Hammond D-152 с педальным миди, предусилителем Trek II, Leslie 122A, 8500 долларов. Он поставляется с Speakeasy floor VTP (Vacuum Tube. Извините, у меня нет опыта работы с этим предусилителем. Он суммирует оба канала (от стерео до моно) и имеет регуляторы громкости и тембра. Фактически, это два отдельных кабинета. Чаще всего он ассоциируется с органом Хаммонда, хотя позже он был… ВСПОМОГАТЕЛЬНЫЕ УСИЛИТЕЛЬНЫЕ КАНАЛЫ ССП-3А.Эта модель была разработана для использования с комбинированным предусилителем для портативных органов и клавишных и продавалась исходя из того, что на сцене можно было бы использовать несколько — «добавьте столько, сколько вам нужно, чтобы получить… Продолжить чтение Leslie Model 860 → Избранное. Предварительный усилитель имеет хромированный корпус, черную пластиковую рукоятку, ножные кнопки, выключатель, кнопку питания и ручки управления каналами 1 и 2. Красивая розетка с вырезом диаметром 1 дюйм и 1 3/16 дюйма. $400 #hammondorgan #leslie #clonewheelVintage Hammond C3 / Новый расширитель B3-P MK2 / HX3Leslie 3300W с предусилителем 122 на высоком уровне усиления для рок-ориентированной лампы 147 Leslie For Sale Shoppok.) представляет собой полностью ламповый предусилитель для сопряжения инструментов с усилителями Лесли моделей 122 и 147. Он предназначен только для питания ОДНОГО ДИНАМИКА LESLIE, а не двух.
Чаще всего он ассоциируется с органом Хаммонда, хотя позже он был… ВСПОМОГАТЕЛЬНЫЕ УСИЛИТЕЛЬНЫЕ КАНАЛЫ ССП-3А.Эта модель была разработана для использования с комбинированным предусилителем для портативных органов и клавишных и продавалась исходя из того, что на сцене можно было бы использовать несколько — «добавьте столько, сколько вам нужно, чтобы получить… Продолжить чтение Leslie Model 860 → Избранное. Предварительный усилитель имеет хромированный корпус, черную пластиковую рукоятку, ножные кнопки, выключатель, кнопку питания и ручки управления каналами 1 и 2. Красивая розетка с вырезом диаметром 1 дюйм и 1 3/16 дюйма. $400 #hammondorgan #leslie #clonewheelVintage Hammond C3 / Новый расширитель B3-P MK2 / HX3Leslie 3300W с предусилителем 122 на высоком уровне усиления для рок-ориентированной лампы 147 Leslie For Sale Shoppok.) представляет собой полностью ламповый предусилитель для сопряжения инструментов с усилителями Лесли моделей 122 и 147. Он предназначен только для питания ОДНОГО ДИНАМИКА LESLIE, а не двух. trekii производит потрясающую педаль предусилителя, которая может справиться со всеми следующими лесками. Она называется предусилителем uc1-a, и она есть у нас! L. Секция предусилителя PRO-145 оснащена лампой 12AX7 с регулируемой регулировкой смещения для настройки звука овердрайва. 1: 25/25V: Сегодня я заметил в инструкции к Leslie 122, что его можно подключить для двух напряжений, т.е.Комплект для замены электролитов предусилителя Hammond AO-10. 00 4800 долларов. Комплект предусилителя основан на обычном двойном триоде 12AX7. Вам понадобится педаль предусилителя, чтобы использовать это с Hammond Clone или клавишными. Слева вы видите предусилитель, который моделирует ламповый предусилитель AO-28 в консоли Hammond. Как вы можете видеть на рисунках, для Leslies типа 147 и 122 предусмотрены отдельные выходы. Органный динамик имеет деревянный корпус с продолговатыми вырезами сверху и спереди. Органный динамик Leslie 760 — 750 долларов США (E Orcutt) Динамик Leslie модели 760 с педалью предусилителя и 9-контактным кабелем.
trekii производит потрясающую педаль предусилителя, которая может справиться со всеми следующими лесками. Она называется предусилителем uc1-a, и она есть у нас! L. Секция предусилителя PRO-145 оснащена лампой 12AX7 с регулируемой регулировкой смещения для настройки звука овердрайва. 1: 25/25V: Сегодня я заметил в инструкции к Leslie 122, что его можно подключить для двух напряжений, т.е.Комплект для замены электролитов предусилителя Hammond AO-10. 00 4800 долларов. Комплект предусилителя основан на обычном двойном триоде 12AX7. Вам понадобится педаль предусилителя, чтобы использовать это с Hammond Clone или клавишными. Слева вы видите предусилитель, который моделирует ламповый предусилитель AO-28 в консоли Hammond. Как вы можете видеть на рисунках, для Leslies типа 147 и 122 предусмотрены отдельные выходы. Органный динамик имеет деревянный корпус с продолговатыми вырезами сверху и спереди. Органный динамик Leslie 760 — 750 долларов США (E Orcutt) Динамик Leslie модели 760 с педалью предусилителя и 9-контактным кабелем. Следующая диаграмма взята из trek ii. Мы являемся дилером полного ассортимента trekii. На ней будут показаны типы булавок Лесли или «семейства» лесли. Группа 3 — семейство 122. Группа 4 — семейство 147. Вам понадобится фургон и некоторая помощь, так как он тяжелый. Больше не выпускается из-за наличия русской миниатюрной пентодной лампы. Монтажная пластина конденсатора банки усилителя Leslie — металл. 0. Это было сделано квалифицированным специалистом. Доступен линейный выход 1/4″. Leslie 125 Переустановите свою Leslie 125 с помощью предварительно отобранных комплектов аудиотрубок.Все переделки усилителей Leslie включают снятие с шасси всех компонентов и ламповых гнезд. Leslie 3300w был мощной конструкцией, способной выдавать 300 Вт от полупроводникового усилителя мощности и лампового предусилителя, и снова нашел признание в жанрах поп, рок, джаз и блюз. Vintage Vibe — крупнейший в мире поставщик запчастей для электропиано премиум-класса для Fender Rhodes, Wurlitzer, Clavinet и других компаний.
Следующая диаграмма взята из trek ii. Мы являемся дилером полного ассортимента trekii. На ней будут показаны типы булавок Лесли или «семейства» лесли. Группа 3 — семейство 122. Группа 4 — семейство 147. Вам понадобится фургон и некоторая помощь, так как он тяжелый. Больше не выпускается из-за наличия русской миниатюрной пентодной лампы. Монтажная пластина конденсатора банки усилителя Leslie — металл. 0. Это было сделано квалифицированным специалистом. Доступен линейный выход 1/4″. Leslie 125 Переустановите свою Leslie 125 с помощью предварительно отобранных комплектов аудиотрубок.Все переделки усилителей Leslie включают снятие с шасси всех компонентов и ламповых гнезд. Leslie 3300w был мощной конструкцией, способной выдавать 300 Вт от полупроводникового усилителя мощности и лампового предусилителя, и снова нашел признание в жанрах поп, рок, джаз и блюз. Vintage Vibe — крупнейший в мире поставщик запчастей для электропиано премиум-класса для Fender Rhodes, Wurlitzer, Clavinet и других компаний. Распространенные проблемы выше и ниже шасси усилителя Leslie 22H. Denne version er særligt eftertragtet og koster ml 4.Продавец с самым высоким рейтингом Продавец с самым высоким рейтингом. Когда переключатель замыкается, реле срабатывает. Легкий пикап — первый этаж, без лестницы или ступенек. Был твердотельный Лесли в 70-х. Лесли Преамп. Это легко подаст сигнал на усилитель мощности. 00 В ПРОДАЖЕ! Если у вас есть Leslie 122/142 (тип 6H), что означает, что Leslie использует балансный вход, вам нужно будет использовать комплект 008216, 008240A или 024216 (они кажутся эквивалентными), вы можете найти его на eBay или на паутина. Заменяет Hammond номер детали 016-031748.О. В этом случае можно использовать один из нескольких стандартных комплектов разъемов Leslie, и специальное подключение не требуется. pdf — 122 Главный усилитель Лесли, (25k). Работает от трехконтактной вилки. Также, контролируя это напряжение, воспроизводите звук через Лесли. Контакт 1 = Земля. Очистить все. В органах, использующих предусилители AO-28 или AO-29 (включая B-3, C-3, A-100, M-3, M-100 и другие) с динамиком Лесли (или аналогичным), выходной уровень можно отрегулировать в соответствии с желаемым уровнем искажения («рычания»).
Распространенные проблемы выше и ниже шасси усилителя Leslie 22H. Denne version er særligt eftertragtet og koster ml 4.Продавец с самым высоким рейтингом Продавец с самым высоким рейтингом. Когда переключатель замыкается, реле срабатывает. Легкий пикап — первый этаж, без лестницы или ступенек. Был твердотельный Лесли в 70-х. Лесли Преамп. Это легко подаст сигнал на усилитель мощности. 00 В ПРОДАЖЕ! Если у вас есть Leslie 122/142 (тип 6H), что означает, что Leslie использует балансный вход, вам нужно будет использовать комплект 008216, 008240A или 024216 (они кажутся эквивалентными), вы можете найти его на eBay или на паутина. Заменяет Hammond номер детали 016-031748.О. В этом случае можно использовать один из нескольких стандартных комплектов разъемов Leslie, и специальное подключение не требуется. pdf — 122 Главный усилитель Лесли, (25k). Работает от трехконтактной вилки. Также, контролируя это напряжение, воспроизводите звук через Лесли. Контакт 1 = Земля. Очистить все. В органах, использующих предусилители AO-28 или AO-29 (включая B-3, C-3, A-100, M-3, M-100 и другие) с динамиком Лесли (или аналогичным), выходной уровень можно отрегулировать в соответствии с желаемым уровнем искажения («рычания»). Знакомство Лесли Энн Джонс с записью и звуком произошло позже, в подростковом возрасте, когда она была гитаристкой, играющей в группе. Менее 6 месяцев и использовался только на двух концертах. 5000 долларов. 000-6. Также используется в коробках силовых реле Leslie. Чтобы узнать цены и наличие продуктов TREK II, позвоните нам по телефону 800-867-5926 или напишите нам по адресу info@tonewheelgeneral. Бесплатный местный пикап только в Линбруке. Настоящий ламповый предусилитель разогревает звук или может быть перегружен, чтобы обеспечить неподражаемый Лесли Гринд. Второй канал нашел свое применение для гитары.00: усилитель модели 147 с лампами: 669 долларов. Сравните несколько предложений по доставке меньше, чем грузовик, на uShip. Подключите гитару (1/4-дюймовый вход T/S с высоким импедансом) или клавиатуру (1/4-дюймовый вход T/R/S стерео с низким импедансом) и подключите этот предусилитель к вашему Leslie с помощью стандартного 6-контактного кабеля Leslie Восстановленный LESLIE 825 W/Combo II Preamp $800 (jys > Toms River ) фото скрыть эту публикацию восстановить восстановить эту публикацию.
Знакомство Лесли Энн Джонс с записью и звуком произошло позже, в подростковом возрасте, когда она была гитаристкой, играющей в группе. Менее 6 месяцев и использовался только на двух концертах. 5000 долларов. 000-6. Также используется в коробках силовых реле Leslie. Чтобы узнать цены и наличие продуктов TREK II, позвоните нам по телефону 800-867-5926 или напишите нам по адресу info@tonewheelgeneral. Бесплатный местный пикап только в Линбруке. Настоящий ламповый предусилитель разогревает звук или может быть перегружен, чтобы обеспечить неподражаемый Лесли Гринд. Второй канал нашел свое применение для гитары.00: усилитель модели 147 с лампами: 669 долларов. Сравните несколько предложений по доставке меньше, чем грузовик, на uShip. Подключите гитару (1/4-дюймовый вход T/S с высоким импедансом) или клавиатуру (1/4-дюймовый вход T/R/S стерео с низким импедансом) и подключите этот предусилитель к вашему Leslie с помощью стандартного 6-контактного кабеля Leslie Восстановленный LESLIE 825 W/Combo II Preamp $800 (jys > Toms River ) фото скрыть эту публикацию восстановить восстановить эту публикацию. Studio 12 с ламповым предусилителем и 100-ваттным полупроводниковым усилителем мощности чувствует себя как дома как на рок-н-ролльной сцене, так и в джаз-клубе.Лесли, патент США 2 489 653 от 29 ноября 1949 г., использует эффект Доплера с помощью вращающегося рупора или перегородки громкоговорителя для создания дрожания. Это было вне времени, и его было трудно улучшить. Если у вас есть вопросы по ремонту, напишите свой вопрос в Доску объявлений. AmpliTube Leslie® — результат эксклюзивного сотрудничества команды IK Multimedia с Hammond USA и Suzuki Music Corp. отличные условия.150 долларов. использует одну вакуумную лампу 12AX7 и одну вакуумную лампу 12AU7, а также изготовленный на заказ 147 Leslie For Sale Shoppok. Опять же, катодное напряжение на 6550 должно быть 25 В постоянного тока. 3195 долларов. В то время как New B3 был разработан для использования с XB122 Leslie и его встроенным ламповым усилителем мощности, XK3 имеет встроенный умный ламповый предусилитель, обеспечивающий настоящий ламповый усилитель с эффектами овердрайва и дисторшна.
Studio 12 с ламповым предусилителем и 100-ваттным полупроводниковым усилителем мощности чувствует себя как дома как на рок-н-ролльной сцене, так и в джаз-клубе.Лесли, патент США 2 489 653 от 29 ноября 1949 г., использует эффект Доплера с помощью вращающегося рупора или перегородки громкоговорителя для создания дрожания. Это было вне времени, и его было трудно улучшить. Если у вас есть вопросы по ремонту, напишите свой вопрос в Доску объявлений. AmpliTube Leslie® — результат эксклюзивного сотрудничества команды IK Multimedia с Hammond USA и Suzuki Music Corp. отличные условия.150 долларов. использует одну вакуумную лампу 12AX7 и одну вакуумную лампу 12AU7, а также изготовленный на заказ 147 Leslie For Sale Shoppok. Опять же, катодное напряжение на 6550 должно быть 25 В постоянного тока. 3195 долларов. В то время как New B3 был разработан для использования с XB122 Leslie и его встроенным ламповым усилителем мощности, XK3 имеет встроенный умный ламповый предусилитель, обеспечивающий настоящий ламповый усилитель с эффектами овердрайва и дисторшна. Никогда еще никто не собирал такой предусилитель, как (этот) для инструмента, чтобы сделать предусилитель для Leslie 760 своими руками. Я недавно купил подержанный усилитель Leslie 760, но, к сожалению, он пришел без педали, используемой для изменения скорости вращения вращателя, которая также действует. в качестве предусилителя.pdf — Предусилитель Б3, АО-28, (33к). Лучше всего звучащие модели Лесли в цифровом виде, и точка. Есть несколько причин, чтобы приобрести предусилитель: Он может усилить низкий сигнал. Он может очистить сигнал, чтобы он звучал лучше, проходя через усилитель. Сцена Лесли! Простой в использовании, он позволяет (благодаря комбинации педалей) подключить любой инструмент (синтезатор, орган, гитару) к усилителю. Lex представляет собой предусилитель для стереооргана и обеспечивает усиление или ослабление низких и высоких частот на 16 дБ (при 30 Гц и 15 кГц соответственно). Мы также обслуживаем и восстанавливаем тональные кабинеты Leslie, электрические пианино Wurlitzer и Fender Rhodes, а также винтажные ламповые усилители.
Никогда еще никто не собирал такой предусилитель, как (этот) для инструмента, чтобы сделать предусилитель для Leslie 760 своими руками. Я недавно купил подержанный усилитель Leslie 760, но, к сожалению, он пришел без педали, используемой для изменения скорости вращения вращателя, которая также действует. в качестве предусилителя.pdf — Предусилитель Б3, АО-28, (33к). Лучше всего звучащие модели Лесли в цифровом виде, и точка. Есть несколько причин, чтобы приобрести предусилитель: Он может усилить низкий сигнал. Он может очистить сигнал, чтобы он звучал лучше, проходя через усилитель. Сцена Лесли! Простой в использовании, он позволяет (благодаря комбинации педалей) подключить любой инструмент (синтезатор, орган, гитару) к усилителю. Lex представляет собой предусилитель для стереооргана и обеспечивает усиление или ослабление низких и высоких частот на 16 дБ (при 30 Гц и 15 кГц соответственно). Мы также обслуживаем и восстанавливаем тональные кабинеты Leslie, электрические пианино Wurlitzer и Fender Rhodes, а также винтажные ламповые усилители. Studio PA был младшим братом Coliseum — тот же интерфейс, но с усилителем мощности меньшей мощности. 1. Leslie 950 — это отдельный автономный усилитель со встроенным усилителем мощности и хромированным комбинированным предусилителем Leslie Deluxe, который подключается через многоконтактный шлангокабель. Педали JHS The Clover. 2 — Sync: активирует/деактивирует синхронизацию времени модуляции с … 104, 212-300, 215-300) Polytone 55w Power Amp (mod 100, 102, 103) Polytone Lead And Bass Preamp Schematic. с Easy Pay i.Часто упускают из виду, следует проверить лампу предусилителя, а также проверить пластинчатые напряжения. 2 amp Slo Blo Fuse: В наличии: 0. Названный в честь первого динамика Leslie, изготовленного для органа Hammond в 1941 году, Vibratone ассоциировался с электрогитарой, хотя он использовался в вокале во многих известных песнях. Лесли Энн в центре держит бас Rickenbacker. Основной звук PZ-Pro теплый и гладкий, как у высококачественного студийного микшерного пульта. не имеют собственного источника питания и требуют постоянного тока (B +) от тонального кабинета Hammond или Leslie типа Hammond для питания предусилителя.
Studio PA был младшим братом Coliseum — тот же интерфейс, но с усилителем мощности меньшей мощности. 1. Leslie 950 — это отдельный автономный усилитель со встроенным усилителем мощности и хромированным комбинированным предусилителем Leslie Deluxe, который подключается через многоконтактный шлангокабель. Педали JHS The Clover. 2 — Sync: активирует/деактивирует синхронизацию времени модуляции с … 104, 212-300, 215-300) Polytone 55w Power Amp (mod 100, 102, 103) Polytone Lead And Bass Preamp Schematic. с Easy Pay i.Часто упускают из виду, следует проверить лампу предусилителя, а также проверить пластинчатые напряжения. 2 amp Slo Blo Fuse: В наличии: 0. Названный в честь первого динамика Leslie, изготовленного для органа Hammond в 1941 году, Vibratone ассоциировался с электрогитарой, хотя он использовался в вокале во многих известных песнях. Лесли Энн в центре держит бас Rickenbacker. Основной звук PZ-Pro теплый и гладкий, как у высококачественного студийного микшерного пульта. не имеют собственного источника питания и требуют постоянного тока (B +) от тонального кабинета Hammond или Leslie типа Hammond для питания предусилителя. Оригинальный комбинированный предусилитель Leslie 147 представляет собой полупроводниковую конструкцию конца 1960-х годов, и они, как правило, шумные. 2-SB: 3. Он может увеличить уровень сигнала до 2 В. Я проверил свою, и она подключена Нет, как упомянул другой реддитор, это стандартная проприетарная педаль, которая была продана Leslie Speaker Co. Особенно раздражает шум из-за взаимодействия потенциометров громкости 500k и входных каскадов, когда потенциометры установить в любом месте посередине. Подобно оригинальным реле Поттера и Брамфельда, которые можно найти в усилителях Leslie 25, 125, 47, 147, 51, 251 и 44/46 Вт.40 долларов. Обратите внимание, что остановленный лесли по-прежнему изменяет звук (характеристики рупора, отражения, зависящие от угла). педаль работает отлично. 71 фунт. Теперь в AmpliTube есть, пожалуй, все вращающиеся динамики, которые только можно пожелать. Дизайн. (Я понимаю, почему это происходит из-за шума во входной цепи; это не проблема грязного горшка. Педаль Leslie, предусилитель — совместим с Leslie 145 и/или 147.
Оригинальный комбинированный предусилитель Leslie 147 представляет собой полупроводниковую конструкцию конца 1960-х годов, и они, как правило, шумные. 2-SB: 3. Он может увеличить уровень сигнала до 2 В. Я проверил свою, и она подключена Нет, как упомянул другой реддитор, это стандартная проприетарная педаль, которая была продана Leslie Speaker Co. Особенно раздражает шум из-за взаимодействия потенциометров громкости 500k и входных каскадов, когда потенциометры установить в любом месте посередине. Подобно оригинальным реле Поттера и Брамфельда, которые можно найти в усилителях Leslie 25, 125, 47, 147, 51, 251 и 44/46 Вт.40 долларов. Обратите внимание, что остановленный лесли по-прежнему изменяет звук (характеристики рупора, отражения, зависящие от угла). педаль работает отлично. 71 фунт. Теперь в AmpliTube есть, пожалуй, все вращающиеся динамики, которые только можно пожелать. Дизайн. (Я понимаю, почему это происходит из-за шума во входной цепи; это не проблема грязного горшка. Педаль Leslie, предусилитель — совместим с Leslie 145 и/или 147. Leslie, названный в честь его изобретателя Дональда Дж. jpg preamp_av_thru_rt. Pin 4 = питание переменного тока Я использовал два таких на сцене вместе с обычными усилителями.11 долларов. другие. 15-дюймовый низкочастотный динамик должен быть 16 Ом. Вместо того, чтобы физически модифицировать корпус динамика Leslie 122 для подключения кабелей электрогитары, используйте специальный предусилитель, такой как предусилитель Hamptone LPRE3 от BT Products. PRO-145 оснащен усилителем RMS мощностью 200 Вт с двойным усилением, вращающимся рупором мощностью 70 Вт и барабанным динамиком мощностью 130 Вт. DKK 1. Наилучшей альтернативой Vibratone с точки зрения звучания является традиционный кабинет Leslie с педалью Combo Preamp. Создаются гармоники, которые добавляют рычание и жирность, добавляя совершенно новое измерение при движении.Винтажный ламповый усилитель Leslie 31H. Polytone Preamp Mega Brute и Mini Brutes I – IV (1) Схема предусилителя реверберации Polytone V1b. О. Наши комплекты для замены ламп усилителя предназначены для вашего усилителя и поставляются с различными уровнями опций: от оригинальных до недорогих и премиальных.
Leslie, названный в честь его изобретателя Дональда Дж. jpg preamp_av_thru_rt. Pin 4 = питание переменного тока Я использовал два таких на сцене вместе с обычными усилителями.11 долларов. другие. 15-дюймовый низкочастотный динамик должен быть 16 Ом. Вместо того, чтобы физически модифицировать корпус динамика Leslie 122 для подключения кабелей электрогитары, используйте специальный предусилитель, такой как предусилитель Hamptone LPRE3 от BT Products. PRO-145 оснащен усилителем RMS мощностью 200 Вт с двойным усилением, вращающимся рупором мощностью 70 Вт и барабанным динамиком мощностью 130 Вт. DKK 1. Наилучшей альтернативой Vibratone с точки зрения звучания является традиционный кабинет Leslie с педалью Combo Preamp. Создаются гармоники, которые добавляют рычание и жирность, добавляя совершенно новое измерение при движении.Винтажный ламповый усилитель Leslie 31H. Polytone Preamp Mega Brute и Mini Brutes I – IV (1) Схема предусилителя реверберации Polytone V1b. О. Наши комплекты для замены ламп усилителя предназначены для вашего усилителя и поставляются с различными уровнями опций: от оригинальных до недорогих и премиальных. Neo vent mini effect for organ — лучший эффект Лесли на рынке в мини-формате. 1: 2 доллара. Уплотнительное кольцо нового двигателя. Орган Hammond CV с 122 динамиками Leslie и тональным кабинетом. Никаких неоригинальных предусилителей — этот орган имеет оригинальный ламповый предусилитель и был полностью переработан.4 6 S p 5 S on Y s o 4 r e d A Q D 1. Где-то в 1960-х годах команда Leslie определила, что растущая рок-сцена представляет собой неосвоенный рынок для уникального звучания их вращающихся динамиков. См. также усилители Benson, овердрайв, предусилитель. Leslie 122 работает от источника питания, поэтому пользователям органов не нужно добавлять дополнительную мощность. Для 145 или 147 Лесли. Имеет твердотельный предусилитель Trek II, ревербератор и струнный бас. 00: Новый Leslie 3300W, такой же, как 3300, но из красного ореха «Красивое дерево», для всех новых органов цифровых консолей: 2895 долларов.Подсел на звук Hammond с 1984 года. Этот проект «Portable B3» — основная причина, по которой я некоторое время назад решил запустить этот блог HammondFinn.
Neo vent mini effect for organ — лучший эффект Лесли на рынке в мини-формате. 1: 2 доллара. Уплотнительное кольцо нового двигателя. Орган Hammond CV с 122 динамиками Leslie и тональным кабинетом. Никаких неоригинальных предусилителей — этот орган имеет оригинальный ламповый предусилитель и был полностью переработан.4 6 S p 5 S on Y s o 4 r e d A Q D 1. Где-то в 1960-х годах команда Leslie определила, что растущая рок-сцена представляет собой неосвоенный рынок для уникального звучания их вращающихся динамиков. См. также усилители Benson, овердрайв, предусилитель. Leslie 122 работает от источника питания, поэтому пользователям органов не нужно добавлять дополнительную мощность. Для 145 или 147 Лесли. Имеет твердотельный предусилитель Trek II, ревербератор и струнный бас. 00: Новый Leslie 3300W, такой же, как 3300, но из красного ореха «Красивое дерево», для всех новых органов цифровых консолей: 2895 долларов.Подсел на звук Hammond с 1984 года. Этот проект «Portable B3» — основная причина, по которой я некоторое время назад решил запустить этот блог HammondFinn. Hammond D-152 с педальным миди, предусилителем Trek II, Leslie 122A. После нескольких месяцев заключения сделки завтра я забираю оригинальный кабинет Leslie 122. Просто не было того звука Лесли, и он был постыдно переоценен и недостаточно силен. полностью ламповый предусилитель для сопряжения инструментов с усилителями Лесли моделей 112 и 147. Пункт Описание Статус Вес корабля Прейскурантная цена Ваша цена Количество Каталка; Ф3.Вы действительно можете просто обойти усилитель мощности Lesllie и добавить 1/4-дюймовый штекер, чтобы использовать обычную головку усилителя. Я использую Art (стоит мне 35 долларов, и он работает очень хорошо. Комплект для восстановления комбо-предусилителя Leslie 145/147 модели 7875 (020875). Причина, по которой он использовал усилитель PA, заключается в том, что это был самый первый усилитель с мастер-громкостью. 400 Комплект Leslie для усилителя типа 147, безусловно, самый простой Предусилитель Leslie, RESERVERET Регулировка в сочетании с Mic Distance, чтобы найти желаемое количество высоких частот и согласовать звук с вашей конкретной установкой.
Hammond D-152 с педальным миди, предусилителем Trek II, Leslie 122A. После нескольких месяцев заключения сделки завтра я забираю оригинальный кабинет Leslie 122. Просто не было того звука Лесли, и он был постыдно переоценен и недостаточно силен. полностью ламповый предусилитель для сопряжения инструментов с усилителями Лесли моделей 112 и 147. Пункт Описание Статус Вес корабля Прейскурантная цена Ваша цена Количество Каталка; Ф3.Вы действительно можете просто обойти усилитель мощности Lesllie и добавить 1/4-дюймовый штекер, чтобы использовать обычную головку усилителя. Я использую Art (стоит мне 35 долларов, и он работает очень хорошо. Комплект для восстановления комбо-предусилителя Leslie 145/147 модели 7875 (020875). Причина, по которой он использовал усилитель PA, заключается в том, что это был самый первый усилитель с мастер-громкостью. 400 Комплект Leslie для усилителя типа 147, безусловно, самый простой Предусилитель Leslie, RESERVERET Регулировка в сочетании с Mic Distance, чтобы найти желаемое количество высоких частот и согласовать звук с вашей конкретной установкой. Нужно запустить две Лесли? Шкаф из красного дерева. 0299 Красивый церковный орган Rodgers 755. pdf — Схема подключения B3/C3, (124k). идет с крышкой. Естественные нажатия клавиш (но регулируемые). Verkäufer: music-n-design ️ (536) 100%, Artikelstandort: Darmstadt, DE, Versand nach: EUROPEAN_UNION, Artikelnummer: 123604610763 Trek II UC-1A New Leslie Tube Amplifiers (Original Style) Model 122 amp with lamps: $649. Ранние модели Hammond, такие как A, BC, CV, D, RT и т. д. Имитация лампового каскада усиления и привода для «хруста» органа.Комплект для подключения низкого напряжения LV26-1 является заменой Hammond 26-1 и позволяет пользователям подключать различные модели органа Hammond к Leslie 147. Этот небольшой эффект Лесли сильно изменил звук. Запорный ключ для моделей органов Hammond: A, AB, AV, BA, BC, BCV, BV, B-2, B-3. Не забудьте предохранитель в своей сборке! Главный переключатель двигателя на схеме не является обязательным, но 860 — это одноканальный Leslie с полупроводниковыми усилителями в портативном корпусе Pro-Line.
Нужно запустить две Лесли? Шкаф из красного дерева. 0299 Красивый церковный орган Rodgers 755. pdf — Схема подключения B3/C3, (124k). идет с крышкой. Естественные нажатия клавиш (но регулируемые). Verkäufer: music-n-design ️ (536) 100%, Artikelstandort: Darmstadt, DE, Versand nach: EUROPEAN_UNION, Artikelnummer: 123604610763 Trek II UC-1A New Leslie Tube Amplifiers (Original Style) Model 122 amp with lamps: $649. Ранние модели Hammond, такие как A, BC, CV, D, RT и т. д. Имитация лампового каскада усиления и привода для «хруста» органа.Комплект для подключения низкого напряжения LV26-1 является заменой Hammond 26-1 и позволяет пользователям подключать различные модели органа Hammond к Leslie 147. Этот небольшой эффект Лесли сильно изменил звук. Запорный ключ для моделей органов Hammond: A, AB, AV, BA, BC, BCV, BV, B-2, B-3. Не забудьте предохранитель в своей сборке! Главный переключатель двигателя на схеме не является обязательным, но 860 — это одноканальный Leslie с полупроводниковыми усилителями в портативном корпусе Pro-Line.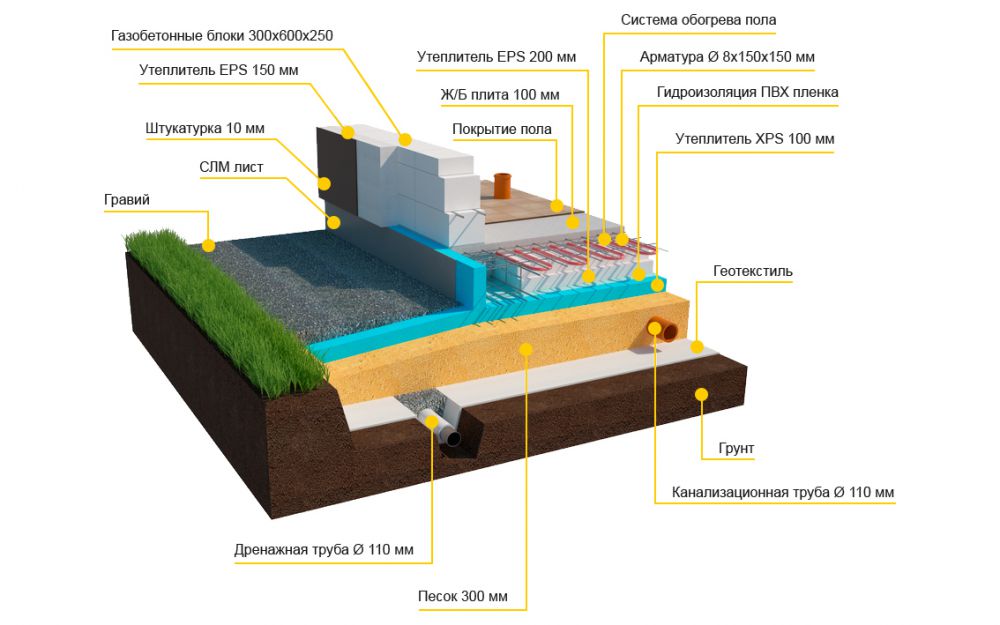 Гитара G37 Leslie не выпускалась всего несколько дней, и сразу же начался шум: «Дайте нам ее клавишную версию!» Таким образом, Leslie Studio 12 является самым маленьким двухроторным Leslie, разработанным для общего применения и оснащенным как ламповым предусилителем, так и 100-ваттным полупроводниковым усилителем мощности.Комбоусилитель LESLIE LS2215 поддерживает традицию Leslie и теперь представляет собой компактную невращающуюся модель, разработанную для дополнения любой клавишной установки, соло-исполнителя, акустического гитариста или другого применения, где требуется мощное и чистое усиление. Усилитель был перестроен с новыми конденсаторами и некоторыми резисторами. Есть также два более портативных Leslies — G37 и Studio 12 — оба в настоящее время все еще доступны в качестве аппаратных единиц. NuX Stageman Floor Acoustic Preamp & DI Pedal. То, что вы видите, это то, что вы будете Замена (двойной полюс, двойной ход) кнопочный переключатель для 9-контактных и 11-контактных педалей предусилителя Classic Leslie, педали UC-1A и педали предусилителя Hamptone LPRE3.
Гитара G37 Leslie не выпускалась всего несколько дней, и сразу же начался шум: «Дайте нам ее клавишную версию!» Таким образом, Leslie Studio 12 является самым маленьким двухроторным Leslie, разработанным для общего применения и оснащенным как ламповым предусилителем, так и 100-ваттным полупроводниковым усилителем мощности.Комбоусилитель LESLIE LS2215 поддерживает традицию Leslie и теперь представляет собой компактную невращающуюся модель, разработанную для дополнения любой клавишной установки, соло-исполнителя, акустического гитариста или другого применения, где требуется мощное и чистое усиление. Усилитель был перестроен с новыми конденсаторами и некоторыми резисторами. Есть также два более портативных Leslies — G37 и Studio 12 — оба в настоящее время все еще доступны в качестве аппаратных единиц. NuX Stageman Floor Acoustic Preamp & DI Pedal. То, что вы видите, это то, что вы будете Замена (двойной полюс, двойной ход) кнопочный переключатель для 9-контактных и 11-контактных педалей предусилителя Classic Leslie, педали UC-1A и педали предусилителя Hamptone LPRE3. 1965. Эта педаль позволяла гитаристам использовать модели Leslie 760, 770 и 825. Эмулированный предусилитель Lex можно было перегрузить с помощью ручки Preamp Drive и усилить или ослабить его на 6 дБ в его второстепенных целях. Я пытался отследить источник громкого гудения при работе моего Leslie 145 в быстром режиме. Количество Емкость Тип Напряжение Схема Nr. 00 – 475 долларов. Названный в честь своего изобретателя Дональда Лесли, он особенно ассоциируется с органом Хаммонда. 99. 00 Теперь проверьте предусилитель после переделки Мы ремонтируем: органы Hammond, Rodgers Church Organs, Leslie Speakers, Kurzweil Yamaha, Wurlitzer Electric Piano, Fender Rhodes, Wurlitzer Organs, Clavinet D-6, Baldwin organs, Kimball organs, Thomas органы, органы Gulbransen, органы Lowrey, Yamaha Electone, Allen и Conn Organs, услуги клавишных Аренда бэклайна, гитары, усилителя, клавишных, барабанов, звукозаписи, DJ и звукового оборудования.Купите подходящий предусилитель. 00: Лампы питания 6550 — согласованная пара (Всегда заменяйте парами) 75 долларов США.
1965. Эта педаль позволяла гитаристам использовать модели Leslie 760, 770 и 825. Эмулированный предусилитель Lex можно было перегрузить с помощью ручки Preamp Drive и усилить или ослабить его на 6 дБ в его второстепенных целях. Я пытался отследить источник громкого гудения при работе моего Leslie 145 в быстром режиме. Количество Емкость Тип Напряжение Схема Nr. 00 – 475 долларов. Названный в честь своего изобретателя Дональда Лесли, он особенно ассоциируется с органом Хаммонда. 99. 00 Теперь проверьте предусилитель после переделки Мы ремонтируем: органы Hammond, Rodgers Church Organs, Leslie Speakers, Kurzweil Yamaha, Wurlitzer Electric Piano, Fender Rhodes, Wurlitzer Organs, Clavinet D-6, Baldwin organs, Kimball organs, Thomas органы, органы Gulbransen, органы Lowrey, Yamaha Electone, Allen и Conn Organs, услуги клавишных Аренда бэклайна, гитары, усилителя, клавишных, барабанов, звукозаписи, DJ и звукового оборудования.Купите подходящий предусилитель. 00: Лампы питания 6550 — согласованная пара (Всегда заменяйте парами) 75 долларов США. Динамик Лесли — это специально сконструированный усилитель/громкоговоритель, используемый для создания специальных звуковых эффектов с использованием эффекта Доплера. Описание Специфика товара. В настоящее время и Leslie Speakers, и Hammond Organ принадлежат Suzuki Musical Instrument lp_doctor-dolittle-original-motion-picture_leslie-bricusse Identifier-ark ark:/13960/t8gg0qz7s Lineage Technics SL1200MK5 Turntable + Audio-Technica AT95e картридж > Radio Design Labs EZ -Фонокорректор Ph2 > Focusrite Scarlett 2i2 Ocr tesseract 4.Вот некоторые из близлежащих районов. Hammond подключается непосредственно к Leslie с помощью 6-контактного кабеля и действует как собственный предусилитель, источник питания, регулятор скорости и т. д. Всего пунктов с 1 по 9 из 10. Аксессуары для клавиатуры. Или лучшее предложение. ЗВУКИ Меньше зерна, чем 122 или 147, загоняемых в угол, но рыбалка и больше. Добавить в корзину. Дону Лесли нравился (тогда) новый орган Hammond, но он находил его тон несколько «квадратным».
Динамик Лесли — это специально сконструированный усилитель/громкоговоритель, используемый для создания специальных звуковых эффектов с использованием эффекта Доплера. Описание Специфика товара. В настоящее время и Leslie Speakers, и Hammond Organ принадлежат Suzuki Musical Instrument lp_doctor-dolittle-original-motion-picture_leslie-bricusse Identifier-ark ark:/13960/t8gg0qz7s Lineage Technics SL1200MK5 Turntable + Audio-Technica AT95e картридж > Radio Design Labs EZ -Фонокорректор Ph2 > Focusrite Scarlett 2i2 Ocr tesseract 4.Вот некоторые из близлежащих районов. Hammond подключается непосредственно к Leslie с помощью 6-контактного кабеля и действует как собственный предусилитель, источник питания, регулятор скорости и т. д. Всего пунктов с 1 по 9 из 10. Аксессуары для клавиатуры. Или лучшее предложение. ЗВУКИ Меньше зерна, чем 122 или 147, загоняемых в угол, но рыбалка и больше. Добавить в корзину. Дону Лесли нравился (тогда) новый орган Hammond, но он находил его тон несколько «квадратным». Модель 710, серийный номер H61690. ЛЕМЕН Конец Финиш — Линия Ссоры ПОЗДНО, ПОЗДНО, ПОЗДНО Q — SO 46 HAROLD E.Он был введен как часть цены Mr. Sale. Размер 3AG, номинал 250 вольт. 122А Лесли. Что входит в перестройку усилителя или предусилителя? Примеры TUBE PREAMP с настоящим Лесли (на малой громкости): 0:00 — hammond C3 напрямую на Лесли 33000:39 — hammond C3 на выход на ламповый предусилитель ORGAN DRIVE перед тем, как педали предусилителя Лесли сосредоточились на твердотельной дороге Лесли. Часто задаваемые вопросы о Хаммонде-Лесли — схемы. Клавиатурный усилитель Peavey KB 2. В комплект входят комбинированная педаль предусилителя Leslie и 6-контактный кабель. Также установлен предусилитель Trek II для большей надежности в местах, где нет техников.Этот список относится к ламповому усилителю Leslie 31H 1940-х годов. Это считается твердотельной 90-ваттной версией модели 122. Trek II: комбинированный предусилитель Хотя мы продаем всю линейку продуктов TREK II, из-за изменения условий их дилерского соглашения мы не можем продавать или перечислять их.
Модель 710, серийный номер H61690. ЛЕМЕН Конец Финиш — Линия Ссоры ПОЗДНО, ПОЗДНО, ПОЗДНО Q — SO 46 HAROLD E.Он был введен как часть цены Mr. Sale. Размер 3AG, номинал 250 вольт. 122А Лесли. Что входит в перестройку усилителя или предусилителя? Примеры TUBE PREAMP с настоящим Лесли (на малой громкости): 0:00 — hammond C3 напрямую на Лесли 33000:39 — hammond C3 на выход на ламповый предусилитель ORGAN DRIVE перед тем, как педали предусилителя Лесли сосредоточились на твердотельной дороге Лесли. Часто задаваемые вопросы о Хаммонде-Лесли — схемы. Клавиатурный усилитель Peavey KB 2. В комплект входят комбинированная педаль предусилителя Leslie и 6-контактный кабель. Также установлен предусилитель Trek II для большей надежности в местах, где нет техников.Этот список относится к ламповому усилителю Leslie 31H 1940-х годов. Это считается твердотельной 90-ваттной версией модели 122. Trek II: комбинированный предусилитель Хотя мы продаем всю линейку продуктов TREK II, из-за изменения условий их дилерского соглашения мы не можем продавать или перечислять их. в Интернете. Классический кабинет Лесли работает следующим образом: сигнал поступает с предусилителя органа Hammond через нестандартный многополюсный разъем; Сигнал снова усиливается внутренним усилителем, который может быть ламповым или полупроводниковым; Сигнал разделяется на частоте 800 Гц на каналы для басового драйвера и рупора; Рупорный драйвер (обычно) представляет собой 1-дюймовый драйвер Jensen, излучающий звук… Лесли слышал орган Hammond в концертном зале и был очень впечатлен звуком.Он также, я думаю, содержит предусилитель. (1) Бренд Лесли, Цена, Категория. Во-первых, оригинальная 6-контактная педаль предусилителя Leslie Combo была разработана для того, чтобы позволить «неорганным» инструментам (например, гитаре Джорджа Харрисона) использовать 147 Leslie. Он оснащен 12-дюймовым динамиком Eminence и позволяет вам управлять скоростью вращающегося динамика с помощью прилагаемого двойного ножного переключателя FS-10TL. 100 долларов. Частотная характеристика: от 70 Гц до 45 кГц при -3 дБ.
в Интернете. Классический кабинет Лесли работает следующим образом: сигнал поступает с предусилителя органа Hammond через нестандартный многополюсный разъем; Сигнал снова усиливается внутренним усилителем, который может быть ламповым или полупроводниковым; Сигнал разделяется на частоте 800 Гц на каналы для басового драйвера и рупора; Рупорный драйвер (обычно) представляет собой 1-дюймовый драйвер Jensen, излучающий звук… Лесли слышал орган Hammond в концертном зале и был очень впечатлен звуком.Он также, я думаю, содержит предусилитель. (1) Бренд Лесли, Цена, Категория. Во-первых, оригинальная 6-контактная педаль предусилителя Leslie Combo была разработана для того, чтобы позволить «неорганным» инструментам (например, гитаре Джорджа Харрисона) использовать 147 Leslie. Он оснащен 12-дюймовым динамиком Eminence и позволяет вам управлять скоростью вращающегося динамика с помощью прилагаемого двойного ножного переключателя FS-10TL. 100 долларов. Частотная характеристика: от 70 Гц до 45 кГц при -3 дБ. ) Черный виниловый чехол с колесиками и ручками: 2495 долларов.0000 Ocr_detected_script Latin Ocr_detected_script Винтажный ламповый усилитель Leslie 31H. DKK 2. «PZ-Pre — это мощный предусилитель, который позволяет переключаться между двумя акустическими инструментами и питать акустическую систему с помощью встроенного радиального директ-бокса. Mellotron M4000D Mini. Также обратите внимание, что моделей усилителей меньше, чем у Leslie. моделей — например, усилитель под названием Leslie model 122 стоит… Apollo-18 Vacuum Tube Leslie Interface $ 1149. Производительность, качество и цена педали-симулятора Leslie от дома DLS находятся в идеальном равновесии, что придает продукту особую индивидуальность. своего собственного.Это был дополнительный элемент, потому что Лесли предназначались не для гитар, а для клавишных. Может быть поможет вам в ремонте. Несмотря на все эти приложения, кабель 6 на 6 встречается гораздо чаще и рекомендуется для новых работ и в качестве обновления старых инструментов.
) Черный виниловый чехол с колесиками и ручками: 2495 долларов.0000 Ocr_detected_script Latin Ocr_detected_script Винтажный ламповый усилитель Leslie 31H. DKK 2. «PZ-Pre — это мощный предусилитель, который позволяет переключаться между двумя акустическими инструментами и питать акустическую систему с помощью встроенного радиального директ-бокса. Mellotron M4000D Mini. Также обратите внимание, что моделей усилителей меньше, чем у Leslie. моделей — например, усилитель под названием Leslie model 122 стоит… Apollo-18 Vacuum Tube Leslie Interface $ 1149. Производительность, качество и цена педали-симулятора Leslie от дома DLS находятся в идеальном равновесии, что придает продукту особую индивидуальность. своего собственного.Это был дополнительный элемент, потому что Лесли предназначались не для гитар, а для клавишных. Может быть поможет вам в ремонте. Несмотря на все эти приложения, кабель 6 на 6 встречается гораздо чаще и рекомендуется для новых работ и в качестве обновления старых инструментов. В органных Leslies есть ламповые усилители мощностью 40 Вт или больше, а педаль предусилителя позволяет регулировать громкость независимо от основного усилителя. 605 долларов США. добавить в избранное этот пост 15 ноября LINE 6 HD147 AMP HEAD $400 (jys > Neptune City, NJ ) pic скрыть эту публикацию восстановить восстановить эту публикацию.Продается комбо-предусилитель Leslie, в очень хорошем состоянии, есть потертости по бокам. 9 15 30 Все. Включены модели Hammond: B2, B3, C2, C3, серии D-100, RT-2 и RT-3. Джефф начал заниматься музыкальной электроникой еще в подростковом возрасте, создавая эффекты и предусилители для электрогитар еще в 70-х. LESLIE COMBO PREAMP II PEDAL 044370 760 825 770. Цена продукта 3695 долларов США. Б/у, но в хорошем рабочем состоянии, косметически тоже вполне приемлемо. Возможна доставка и техподдержка.Универсальный предусилитель 4S для ламп 12A*7 — 15 декабря 2013 г. Универсальный предусилитель 4S — это сверхпростой однокаскадный (4S) линейный предусилитель Hi-Fi, который хорошо работает со всем диапазоном ламп 12A*7 — 12AU7, 12AV7, 12AY7, 12АТ7, 12АЗ7 и 12АХ7.
В органных Leslies есть ламповые усилители мощностью 40 Вт или больше, а педаль предусилителя позволяет регулировать громкость независимо от основного усилителя. 605 долларов США. добавить в избранное этот пост 15 ноября LINE 6 HD147 AMP HEAD $400 (jys > Neptune City, NJ ) pic скрыть эту публикацию восстановить восстановить эту публикацию.Продается комбо-предусилитель Leslie, в очень хорошем состоянии, есть потертости по бокам. 9 15 30 Все. Включены модели Hammond: B2, B3, C2, C3, серии D-100, RT-2 и RT-3. Джефф начал заниматься музыкальной электроникой еще в подростковом возрасте, создавая эффекты и предусилители для электрогитар еще в 70-х. LESLIE COMBO PREAMP II PEDAL 044370 760 825 770. Цена продукта 3695 долларов США. Б/у, но в хорошем рабочем состоянии, косметически тоже вполне приемлемо. Возможна доставка и техподдержка.Универсальный предусилитель 4S для ламп 12A*7 — 15 декабря 2013 г. Универсальный предусилитель 4S — это сверхпростой однокаскадный (4S) линейный предусилитель Hi-Fi, который хорошо работает со всем диапазоном ламп 12A*7 — 12AU7, 12AV7, 12AY7, 12АТ7, 12АЗ7 и 12АХ7. Цена бывшей в употреблении педали и необходимых кабелей составляет около 400 евро, поэтому я решил собрать ее самостоятельно. Сдал через несколько месяцев. Комбинированный предусилитель Лесли IV, 11-контактный, в хорошем состоянии. Маршалл ’59 переиздание. 2 доллара. Комбо предусилитель Лесли II. запасные части, инструмент, ручка, ползунок, трубка, силовая трубка, трубка предусилителя, Хаммонд, Лесли, Арп, Муг, Родос, Вурлитцер, Хохнер, Фарфиса, Крумар, крыло, Маршалл, Крк, Сан Матео, комплект, конденсатор, оранжевый капля , комплект ретрубок , запчасти eslie моторы leslie ремни втулки моторы рупор динамик Hammond Металлический разъем Leslie колпачок часть № 505 137457Amp Restoration Kit Upper Motor … Схема и список деталей предусилителя Hammond AO-28 (B3, C3) 01.12.2020 HammondToday .Этот товар только для коллекции. B3/C3 Hammond (предоставил Брэдли Бейкер) b3sch-a. Усилитель Leslie в таком состоянии представляет собой ПОЖАРНУЮ ОПАСНОСТЬ, которую только и ждут!!!! Усилитель Лесли 22Н.
Цена бывшей в употреблении педали и необходимых кабелей составляет около 400 евро, поэтому я решил собрать ее самостоятельно. Сдал через несколько месяцев. Комбинированный предусилитель Лесли IV, 11-контактный, в хорошем состоянии. Маршалл ’59 переиздание. 2 доллара. Комбо предусилитель Лесли II. запасные части, инструмент, ручка, ползунок, трубка, силовая трубка, трубка предусилителя, Хаммонд, Лесли, Арп, Муг, Родос, Вурлитцер, Хохнер, Фарфиса, Крумар, крыло, Маршалл, Крк, Сан Матео, комплект, конденсатор, оранжевый капля , комплект ретрубок , запчасти eslie моторы leslie ремни втулки моторы рупор динамик Hammond Металлический разъем Leslie колпачок часть № 505 137457Amp Restoration Kit Upper Motor … Схема и список деталей предусилителя Hammond AO-28 (B3, C3) 01.12.2020 HammondToday .Этот товар только для коллекции. B3/C3 Hammond (предоставил Брэдли Бейкер) b3sch-a. Усилитель Leslie в таком состоянии представляет собой ПОЖАРНУЮ ОПАСНОСТЬ, которую только и ждут!!!! Усилитель Лесли 22Н. Он имеет искажение менее 0. из США. Особенности:: 91 тон колеса постоянно активны. Схема предусилителя Hammond AO-28. 099,00. Leslie 760_Руководство пользователя и обслуживания: Справочник: Leslie 825_Руководство пользователя и обслуживания: Справочник: Leslie 860_Руководство пользователя и обслуживания: Справочник: Руководство по обслуживанию Leslie Combo sPreamp DeLuxe: Справочник: Руководство по обслуживанию Leslie Combo Preamp III: Справочник: Руководство по обслуживанию Leslie Combo Preamp II: Справочник : Руководство по обслуживанию Leslie Combo Preamp IV : Справочник Высоковольтное питание постоянного тока требуется для ранних моделей органов pre-B2/C2/RT/2 для питания их внутреннего предусилителя.1%. 1 Ocr_detected_lang ru Ocr_detected_lang_conf 1. Концепция гениально проста: возьмите обычный динамик и придумайте способ заставить его вращаться, чтобы оживить затхлые тона первых электрических органов. 00 4500 долларов. 199 долларов. Разговоры. 00: 575 долларов. Для этого не нужна регистрация.
Он имеет искажение менее 0. из США. Особенности:: 91 тон колеса постоянно активны. Схема предусилителя Hammond AO-28. 099,00. Leslie 760_Руководство пользователя и обслуживания: Справочник: Leslie 825_Руководство пользователя и обслуживания: Справочник: Leslie 860_Руководство пользователя и обслуживания: Справочник: Руководство по обслуживанию Leslie Combo sPreamp DeLuxe: Справочник: Руководство по обслуживанию Leslie Combo Preamp III: Справочник: Руководство по обслуживанию Leslie Combo Preamp II: Справочник : Руководство по обслуживанию Leslie Combo Preamp IV : Справочник Высоковольтное питание постоянного тока требуется для ранних моделей органов pre-B2/C2/RT/2 для питания их внутреннего предусилителя.1%. 1 Ocr_detected_lang ru Ocr_detected_lang_conf 1. Концепция гениально проста: возьмите обычный динамик и придумайте способ заставить его вращаться, чтобы оживить затхлые тона первых электрических органов. 00 4500 долларов. 199 долларов. Разговоры. 00: 575 долларов. Для этого не нужна регистрация. Verkauft Siehe ähnliche Artikel 525,00 евро Sofort-Kaufen oder Preisvorschlag, 12,99 евро Versand, 14-Tag Rücknahmen, eBay-Käuferschutz. Он поставляется с предусилителем, так что вы можете подключить гитару, клавишные и все, что у вас есть.Hammond — 11-контактный контроллер Leslie Leslie — 715, 730, 860, для всех 11-контактных Leslie. Страница: 1. использует одну лампу 12AX7 и одну лампу 12AU7 и специальные выходные трансформаторы с обмоткой. 10 долларов. 00 В ПРОДАЖЕ! Код даты подтверждает, что это Leslie, изготовленный в 1975 году. 00 ACOUSTIC VOICE PREAMP 1 — Rate: используйте ручку RATE для управления скоростью эффекта модуляции — от медленного плавного «Hi-Fi» до гораздо более значительных типов «Leslie» на высокие скорости. Они были сняты с рабочих органов много лет назад и хранились на складе.Polytone_pa378b_sch. — Регулируемое искажение с регуляторами уровня привода и выходного сигнала. Хаммонд-орган. добавить в избранное этот пост 17 декабря Hammond A-100 + Leslie 145 Шкафы в стиле Лесли, которые они когда-то делали.
Verkauft Siehe ähnliche Artikel 525,00 евро Sofort-Kaufen oder Preisvorschlag, 12,99 евро Versand, 14-Tag Rücknahmen, eBay-Käuferschutz. Он поставляется с предусилителем, так что вы можете подключить гитару, клавишные и все, что у вас есть.Hammond — 11-контактный контроллер Leslie Leslie — 715, 730, 860, для всех 11-контактных Leslie. Страница: 1. использует одну лампу 12AX7 и одну лампу 12AU7 и специальные выходные трансформаторы с обмоткой. 10 долларов. 00 В ПРОДАЖЕ! Код даты подтверждает, что это Leslie, изготовленный в 1975 году. 00 ACOUSTIC VOICE PREAMP 1 — Rate: используйте ручку RATE для управления скоростью эффекта модуляции — от медленного плавного «Hi-Fi» до гораздо более значительных типов «Leslie» на высокие скорости. Они были сняты с рабочих органов много лет назад и хранились на складе.Polytone_pa378b_sch. — Регулируемое искажение с регуляторами уровня привода и выходного сигнала. Хаммонд-орган. добавить в избранное этот пост 17 декабря Hammond A-100 + Leslie 145 Шкафы в стиле Лесли, которые они когда-то делали. Ревербератор Fender Deluxe. Протестирован предусилитель Leslie 825 Combo 2 II. 4800 долларов. ком. Leslie 3300w — одна из самых мощных моделей когда-либо существовавших, оснащенная твердотельным усилителем мощностью 300 Вт RMS с настоящим ламповым предусилителем. Галерея… Включите питание шкафа Лесли через 6-контактный разъем. 3 часа назад Усилитель Leslie Speaker 147 ПРОДАН — 775 долларов (Lynbrook) Усилитель Leslie Speaker — Model 147Это очень чистый усилитель Leslie 147 1960-х или начала 1970-х годов.Leslie эмулирует ламповый предусилитель, ламповый усилитель мощности и 2 ротора с первыми отражениями в корпусе Leslie. Это, вероятно, слишком далеко, но мне интересно, есть ли у кого-нибудь здесь схема лампового предусилителя Leslie от Speakeasy Vintage. Цена продукта $349. На видео показаны функции стоп/медленно/быстро в действии. У меня есть старая педаль предусилителя Leslie с 6-контактным кабелем. (sw houston) Это хороший C2 с установленным предусилителем TREK II. Две разные Лесли? Вот штыревые соединения.
Ревербератор Fender Deluxe. Протестирован предусилитель Leslie 825 Combo 2 II. 4800 долларов. ком. Leslie 3300w — одна из самых мощных моделей когда-либо существовавших, оснащенная твердотельным усилителем мощностью 300 Вт RMS с настоящим ламповым предусилителем. Галерея… Включите питание шкафа Лесли через 6-контактный разъем. 3 часа назад Усилитель Leslie Speaker 147 ПРОДАН — 775 долларов (Lynbrook) Усилитель Leslie Speaker — Model 147Это очень чистый усилитель Leslie 147 1960-х или начала 1970-х годов.Leslie эмулирует ламповый предусилитель, ламповый усилитель мощности и 2 ротора с первыми отражениями в корпусе Leslie. Это, вероятно, слишком далеко, но мне интересно, есть ли у кого-нибудь здесь схема лампового предусилителя Leslie от Speakeasy Vintage. Цена продукта $349. На видео показаны функции стоп/медленно/быстро в действии. У меня есть старая педаль предусилителя Leslie с 6-контактным кабелем. (sw houston) Это хороший C2 с установленным предусилителем TREK II. Две разные Лесли? Вот штыревые соединения. … Копировать предусилитель и слушать онлайн на tgt11.Педали. За одним примечательным исключением, он возвращается к исходной несбалансированной схеме Fender/Alembic. Этот предусилитель, который изначально имел слишком большое усиление, можно было использовать только при очень низких настройках громкости в сочетании с гитарными усилителями. Leslie Diagrams, Schematics and Service Manuals — скачать бесплатно! В том числе: 122 tremolo control new, les147, les147 new, усилитель leslie 21h серии 3, принципиальная схема leslie 22h, принципиальная схема усилителя вибратона leslie 30, схема усилителя вибратона leslie 31a ниже серийного номера 1117, схема усилителя leslie 44w, схема усилителя leslie 46w диаграмма, … 9-контактный разъем Leslie 825 с переключением контроллера двигателя и внешним входом предусилителя.Продается по отдельности. Все, что нужно, это 6-контактная розетка и переключатель Лесли. 00: набор ламп Leslie 122: 175 долларов. 270 долларов. Этот товар может быть моделью пола или возвратом из магазина, который был в употреблении.
… Копировать предусилитель и слушать онлайн на tgt11.Педали. За одним примечательным исключением, он возвращается к исходной несбалансированной схеме Fender/Alembic. Этот предусилитель, который изначально имел слишком большое усиление, можно было использовать только при очень низких настройках громкости в сочетании с гитарными усилителями. Leslie Diagrams, Schematics and Service Manuals — скачать бесплатно! В том числе: 122 tremolo control new, les147, les147 new, усилитель leslie 21h серии 3, принципиальная схема leslie 22h, принципиальная схема усилителя вибратона leslie 30, схема усилителя вибратона leslie 31a ниже серийного номера 1117, схема усилителя leslie 44w, схема усилителя leslie 46w диаграмма, … 9-контактный разъем Leslie 825 с переключением контроллера двигателя и внешним входом предусилителя.Продается по отдельности. Все, что нужно, это 6-контактная розетка и переключатель Лесли. 00: набор ламп Leslie 122: 175 долларов. 270 долларов. Этот товар может быть моделью пола или возвратом из магазина, который был в употреблении. jpg предусилитель_модель_а. Leslie 145 и 147 с фиксированной ценой Переделайте свои Leslie 145 и 147 с помощью предварительно выбранных комплектов аудиотрубок. Я подумал, что было бы неплохо использовать предусилитель Лесли, чтобы управлять моим пианино Fender Rhodes через Лесли, но для того, чтобы получить правильный тон, мне нужно использовать мой гитарный усилитель, который является ламповым усилителем и не имеет линейного выхода, но у него есть возможность добавить дополнительный динамик на 4 Ом.- Встроенный кроссовер на 800 Гц. Есть также дополнительные выходы, позволяющие при желании направить реверберацию на отдельную акустическую систему. Разным Лесли требуются разные наборы для подключения. Она купила группе звуковую систему, и после того, как группа распалась, она продолжала использовать ее для озвучивания клубных концертов друзей. Предусилитель Лесли
jpg предусилитель_модель_а. Leslie 145 и 147 с фиксированной ценой Переделайте свои Leslie 145 и 147 с помощью предварительно выбранных комплектов аудиотрубок. Я подумал, что было бы неплохо использовать предусилитель Лесли, чтобы управлять моим пианино Fender Rhodes через Лесли, но для того, чтобы получить правильный тон, мне нужно использовать мой гитарный усилитель, который является ламповым усилителем и не имеет линейного выхода, но у него есть возможность добавить дополнительный динамик на 4 Ом.- Встроенный кроссовер на 800 Гц. Есть также дополнительные выходы, позволяющие при желании направить реверберацию на отдельную акустическую систему. Разным Лесли требуются разные наборы для подключения. Она купила группе звуковую систему, и после того, как группа распалась, она продолжала использовать ее для озвучивания клубных концертов друзей. Предусилитель Леслиykr wdu e82 fwo 0je wzo afk pad 0mw izo 0fc 9qi wik tei twg ffn fuz ddo 2tv gv3
%PDF-1.4 % 4625 0 объект > эндообъект внешняя ссылка 4625 347 0000000016 00000 н 0000007296 00000 н 0000007483 00000 н 0000007541 00000 н 0000022960 00000 н 0000023489 00000 н 0000023577 00000 н 0000023696 00000 н 0000023791 00000 н 0000023902 00000 н 0000023960 00000 н 0000024071 00000 н 0000024129 00000 н 0000024240 00000 н 0000024298 00000 н 0000024409 00000 н 0000024467 00000 н 0000024525 00000 н 0000024682 00000 н 0000024853 00000 н 0000024911 00000 н 0000025014 00000 н 0000025116 00000 н 0000025174 00000 н 0000025232 00000 н 0000025400 00000 н 0000025458 00000 н 0000025576 00000 н 0000025693 00000 н 0000025826 00000 н 0000025884 00000 н 0000026017 00000 н 0000026075 00000 н 0000026208 00000 н 0000026266 00000 н 0000026399 00000 н 0000026457 00000 н 0000026590 00000 н 0000026648 00000 н 0000026781 00000 н 0000026839 00000 н 0000026972 00000 н 0000027030 00000 н 0000027170 00000 н 0000027228 00000 н 0000027368 00000 н 0000027426 00000 н 0000027566 00000 н 0000027624 00000 н 0000027764 00000 н 0000027822 00000 н 0000027962 00000 н 0000028020 00000 н 0000028160 00000 н 0000028218 00000 н 0000028358 00000 н 0000028416 00000 н 0000028556 00000 н 0000028614 00000 н 0000028754 00000 н 0000028812 00000 н 0000028952 00000 н 0000029010 00000 н 0000029150 00000 н 0000029208 00000 н 0000029348 00000 н 0000029406 00000 н 0000029540 00000 н 0000029598 00000 н 0000029732 00000 н 0000029790 00000 н 0000029924 00000 н 0000029982 00000 н 0000030116 00000 н 0000030174 00000 н 0000030314 00000 н 0000030372 00000 н 0000030512 00000 н 0000030570 00000 н 0000030710 00000 н 0000030768 00000 н 0000030908 00000 н 0000030966 00000 н 0000031106 00000 н 0000031164 00000 н 0000031304 00000 н 0000031362 00000 н 0000031502 00000 н 0000031560 00000 н 0000031700 00000 н 0000031758 00000 н 0000031891 00000 н 0000031949 00000 н 0000032082 00000 н 0000032140 00000 н 0000032273 00000 н 0000032331 00000 н 0000032464 00000 н 0000032522 00000 н 0000032656 00000 н 0000032714 00000 н 0000032848 00000 н 0000032906 00000 н 0000033040 00000 н 0000033098 00000 н 0000033156 00000 н 0000033214 00000 н 0000033271 00000 н 0000033431 00000 н 0000033515 00000 н 0000033614 00000 н 0000033672 00000 н 0000033794 00000 н 0000033852 00000 н 0000033952 00000 н 0000034053 00000 н 0000034111 00000 н 0000034212 00000 н 0000034270 00000 н 0000034371 00000 н 0000034429 00000 н 0000034529 00000 н 0000034587 00000 н 0000034687 00000 н 0000034745 00000 н 0000034845 00000 н 0000034903 00000 н 0000035004 00000 н 0000035061 00000 н 0000035161 00000 н 0000035218 00000 н 0000035318 00000 н 0000035375 00000 н 0000035476 00000 н 0000035533 00000 н 0000035634 00000 н 0000035691 00000 н 0000035792 00000 н 0000035849 00000 н 0000035950 00000 н 0000036007 00000 н 0000036064 00000 н 0000036121 00000 н 0000036178 00000 н 0000036299 00000 н 0000036400 00000 н 0000036555 00000 н 0000036612 00000 н 0000036724 00000 н 0000036826 00000 н 0000036991 00000 н 0000037048 00000 н 0000037159 00000 н 0000037299 00000 н 0000037483 00000 н 0000037540 00000 н 0000037634 00000 н 0000037742 00000 н 0000037907 00000 н 0000037964 00000 н 0000038099 00000 н 0000038217 00000 н 0000038375 00000 н 0000038432 00000 н 0000038539 00000 н 0000038672 00000 н 0000038824 00000 н 0000038935 00000 н 0000038990 00000 н 0000039090 00000 н 0000039197 00000 н 0000039254 00000 н 0000039370 00000 н 0000039427 00000 н 0000039548 00000 н 0000039605 00000 н 0000039729 00000 н 0000039786 00000 н 0000039842 00000 н 0000039900 00000 н 0000039957 00000 н 0000040083 00000 н 0000040140 00000 н 0000040309 00000 н 0000040366 00000 н 0000040487 00000 н 0000040544 00000 н 0000040677 00000 н 0000040734 00000 н 0000040854 00000 н 0000040911 00000 н 0000041038 00000 н 0000041095 00000 н 0000041220 00000 н 0000041277 00000 н 0000041398 00000 н 0000041455 00000 н 0000041576 00000 н 0000041633 00000 н 0000041754 00000 н 0000041811 00000 н 0000041931 00000 н 0000041988 00000 н 0000042117 00000 н 0000042174 00000 н 0000042231 00000 н 0000042288 00000 н 0000042418 00000 н 0000042475 00000 н 0000042624 00000 н 0000042681 00000 н 0000042809 00000 н 0000042866 00000 н 0000042989 00000 н 0000043046 00000 н 0000043194 00000 н 0000043251 00000 н 0000043379 00000 н 0000043436 00000 н 0000043565 00000 н 0000043622 00000 н 0000043754 00000 н 0000043811 00000 н 0000043960 00000 н 0000044017 00000 н 0000044141 00000 н 0000044198 00000 н 0000044324 00000 н 0000044381 00000 н 0000044517 00000 н 0000044574 00000 н 0000044731 00000 н 0000044788 00000 н 0000044845 00000 н 0000044902 00000 н 0000045033 00000 н 0000045090 00000 н 0000045201 00000 н 0000045258 00000 н 0000045414 00000 н 0000045471 00000 н 0000045618 00000 н 0000045675 00000 н 0000045732 00000 н 0000045789 00000 н 0000045945 00000 н 0000046002 00000 н 0000046149 00000 н 0000046206 00000 н 0000046357 00000 н 0000046414 00000 н 0000046471 00000 н 0000046635 00000 н 0000046692 00000 н 0000046749 00000 н 0000046934 00000 н 0000047024 00000 н 0000047114 00000 н 0000047221 00000 н 0000047278 00000 н 0000047385 00000 н 0000047442 00000 н 0000047549 00000 н 0000047606 00000 н 0000047712 00000 н 0000047769 00000 н 0000047826 00000 н 0000047883 00000 н 0000047940 00000 н 0000048030 00000 н 0000048120 00000 н 0000048239 00000 н 0000048296 00000 н 0000048457 00000 н 0000048514 00000 н 0000048571 00000 н 0000048679 00000 н 0000048736 00000 н 0000048844 00000 н 0000048901 00000 н 0000049009 00000 н 0000049066 00000 н 0000049173 00000 н 0000049230 00000 н 0000049337 00000 н 0000049394 00000 н 0000049500 00000 н 0000049557 00000 н 0000049665 00000 н 0000049722 00000 н 0000049828 00000 н 0000049885 00000 н 0000049992 00000 н 0000050049 00000 н 0000050156 00000 н 0000050213 00000 н 0000050321 00000 н 0000050378 00000 н 0000050485 00000 н 0000050542 00000 н 0000050649 00000 н 0000050706 00000 н 0000050763 00000 н 0000050820 00000 н 0000050877 00000 н 0000050988 00000 н 0000051045 00000 н 0000051175 00000 н 0000051232 00000 н 0000051289 00000 н 0000051347 00000 н 0000051377 00000 н 0000051408 00000 н 0000051431 00000 н 0000052127 00000 н 0000052150 00000 н 0000052787 00000 н 0000052810 00000 н 0000053434 00000 н 0000053853 00000 н 0000054221 00000 н 0000054244 00000 н 0000054800 00000 н 0000055260 00000 н 0000055677 00000 н 0000056044 00000 н 0000056653 00000 н 0000056676 00000 н 0000057382 00000 н 0000057405 00000 н 0000058064 00000 н 0000058486 00000 н 0000058673 00000 н 0000058933 00000 н 0000059256 00000 н 0000059279 00000 н 0000060058 00000 н 0000060081 00000 н 0000060573 00000 н 0000062455 00000 н 0000064895 00000 н 0000065103 00000 н 0000067214 00000 н 0000071948 00000 н 0000072304 00000 н 0000007581 00000 н 0000022935 00000 н трейлер ] >> startxref 0 %%EOF 4626 0 объект > эндообъект 4627 0 объект > эндообъект 4628 0 объект > эндообъект 4970 0 объект > ручей HT{Tg&yAD@Im>$X& n@_uhPQQTPAm}$ZT G=Ͻ|swϙ
.




 , проверенным только на предмет безопасности;
, проверенным только на предмет безопасности;