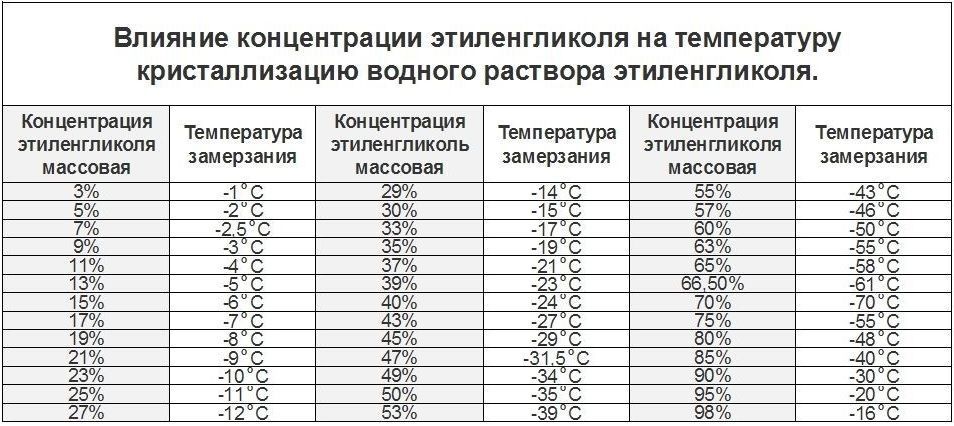
Чтобы не замерзал раствор: Незамерзайки в бетон сравнительные характеристики присадок — купить добавки в Москве
Добавки в бетон при минусовых температурах: особенности заливки
Согласно строительным нормам, понятие зимних условий несколько отличается от общепринятых, календарных. В частности холодным временем принято считать условия со среднесуточной температурой около +5ºС и возможностью ночного понижения до 0ºС. Как известно при низких температурах вода кристаллизуется и процессы гидратации в цементно-содержащих составах значительно замедляются или вообще приостанавливаются.
Но на большей территории нашей страны это время является достаточно продолжительным. Останавливать работу и ждать когда потеплеет нерентабельно. Поэтому с момента появления бетона специалисты ищут решение данной проблемы.
Фото противоморозной добавки.
Распространенные виды заливки бетона на холоде
До недавнего времени, наиболее распространенным и действенным считался способ предварительного разогрева составляющих раствора до определенной температуры, после чего готовился теплый раствор и заливался.
Температура монолита поддерживалась искусственным путем до набора прочности не менее 50%.
Схема парогенератора для прогрева бетона.
- Но с каждым годом цена на энергоносители растет, и такие технологии сильно увеличивают себестоимость строительства. Здесь уже не столь важно, чем разогревать бетон — электричеством, паром или иными энергоемкими способами.
- В середине прошлого века нашим ученым И.А.Кириенко был предложен еще один действенный способ прогрева монолита. Условно его назвали методом «Термоса». Общая инструкция достаточно проста, вокруг ЖБИ создается теплоизолирующее покрывало. В зависимости от температуры окружающей среды бетон мог прогреваться за счет внутренних процессов или энергоносителем извне.
- В последнее же время наука сделала качественный рывок в создании химически активных добавок, которые позволяют вести работы при круглосуточной минусовой температуре. Безусловно, это очень удобно, присадок существует несколько и о наиболее распространенных мы сейчас побеседуем.

Принцип действия и виды морозостойких составов
Загрузка в бетономешалку.
Что добавлять в бетон при минусовой температуре, вопрос далеко не праздный. Полностью, на 100% универсального состава не существует.
Выбор зависит от многих факторов, прежде всего от самой температуры.
- Также большое влияние оказывает размер монолита. Плюс следует учесть предназначение изделия, дело в том, что разные добавки могут менять некоторые физические качества бетона и то, что подойдет для ленточного фундамента в частном доме, может не подойти для возведения моста или крупного наливного цоколя.
Прогрев методом «Термос».
Как это работает
Как известно основной задачей воды в растворе является создание условий для кристаллизации составляющих раствора, силикатов, алюминатов и так далее. На языке профессионалов это называется гидратацией цемента.
Наиболее комфортно, без добавок, раствор застывает при температуре 15 — 20 ºС, все что выше и особенно ниже, нуждается в создании специальных условий.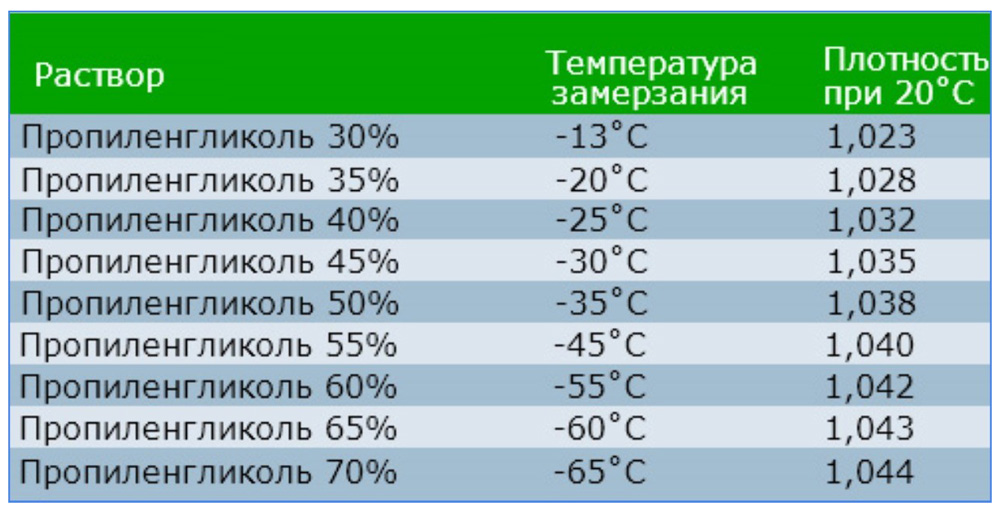
- Главной задачей подобного рода присадок является снижение периода схватывания раствора и уменьшение времени созревания бетона при низких температурах. То есть снизить уровень замерзания воды и при этом не навредить остальным процессам, происходящим в растворе.
Зависимость набора прочности от температуры.
Распространенные составы и способы работы
- Наиболее распространенными материалами для изготовления морозоустойчивых присадок смело можно считать соли монокарбоновых кислот, среди профессионалов этот состав известен как «Поташ». Цена на данные составы на отечественном рынке вполне приемлемая.
- Когда выполняется заливка бетона при минусовой температуре добавки монокарбоновых кислот, должны строго дозироваться. Для каждой температуры количество присадок разное, Такими добавками можно подготовить раствор к температуре до минус 30ºС. Чем ниже температура, тем больше состава потребуется.
Соль монокарбоновой кислоты.
Важно: как говорилось ранее, присадка при неграмотном использовании может понизить другие характеристики раствора.

Поэтому принцип, чем больше, тем лучше здесь может навредить.
- Следующим лидером нашего рынка является нитрит натрия. Цена на него также не сильно высока, но это вещество обладает сильным, едким, неприятным запахом. Кроме того данный состав легко может воспламениться. При контакте с некоторыми видами современных пластификаторов могут выделяться ядовитые, токсичные газы.
Нитрит натрия.
- Максимальная температура, которую может держать нитрат натрия, составляет не ниже -15ºС. Специалисты рекомендуют его использование при приготовлении растворов на портландцементе или на шлакопортландцементе. Добавлять эту присадку в глиноземистые цементы строго запрещено.
- Широкий спектр использования имеет формиат натрия и нитрат кальция. Кроме производства ЖБИ, эти присадки могут применяться в штукатурных растворах и растворах предназначенных для кладки кирпича. Но данные составы используются только в комплексе с пластификатором, так как из-за скопления солей, в монолите могут образовываться пустоты и высолы.

Формиат натрия.
Важно: растворы с добавлением присадок должны готовиться своими руками при температуре не ниже 5 — 10 ºС.
Кроме того, они не могут долго храниться, раствор нужно использовать в течение часа после замешивания.
Строительный тепловентилятор.
- Не стоит забывать об отечественных производителях, добавки из линейки морозо-пласт, морозо-стирол и т.д. Являются составами комплексного действия, после заливки благодаря процессам, происходящим внутри монолита, температура поддерживается естественным образом и при небольших морозах, вам достаточно просто хорошо укрыть бетон.
Зависимость от марки бетона
Конструкции для электроподогрева монолита.
- По нормам СНиП 111-1-76, мороз опасен для бетона только на стадии набора прочности. Поддерживать определенную температуру в монолите нужно до определенного % крепости. Для каждой марки бетона этот процент индивидуален.
- После того, как монолит схватился, замораживание ему уже не настолько страшно, но и эксплуатировать ЖБИ еще не рекомендуется.

- Если в состав не вводились морозоустойчивые присадки, то для растворов с маркой М150 достаточно 50% прочности. Марки М200 – М300, могут замораживаться при 40% прочности. Для М400 и более, достаточно 30%. Но при использовании присадки, допустимая прочность перед замораживанием падает в среднем на 10%.
Совет: время вымешивания состава в зимних условиях должно быть увеличено минимум в 2 раза.
Мифы, связанные с добавками
График прогрева бетонного монолита.
- В широком использовании данный вид присадок появился не так давно. Народ еще не успел, как следует разобраться в том насколько это удобно и на этой благодатной почве родилось несколько предубеждений.
- Первый распространенный миф родился уже давно, периодически с появлением каждого нового состава подымается данный вопрос, не стали исключением и морозоустойчивые добавки.
 Кустарные мастера «авторитетно» заявляют о том, что такие добавки вызывают повышенную коррозию арматурного каркаса.
Кустарные мастера «авторитетно» заявляют о том, что такие добавки вызывают повышенную коррозию арматурного каркаса. - Возьмем самый простой и доступный в России нитрит натрия. Любой средний химик или специалист по металловеденью вам скажет, что это один из ингибиторов способных замедлять процессы коррозии. Более того, в соединении с пластификаторами и усадочными добавками для работы с монолитами, в виду повышения крепости может применяться только алмазное бурение отверстий в бетоне, а также резка железобетона алмазными кругами.
Соотношение компонентов в разных марках чистого бетона.
- Вторым распространенным мифом можно назвать снижение прочности бетона. Родилось это утверждение из-за того, что на первых этапах схватывания раствора действительно наблюдается некоторое запоздание по сравнению с чистым бетоном. Но зато впоследствии скорость набора прочности значительно увеличивается. Особенно это относится к комбинированным составам.
- Все специалисты, с самого начала советуют одно, внимательно изучить инструкцию.
 При недостаточном количестве присадки в растворе, он может замерзнуть. Но если заложить чрезмерно много добавки, то вы рискуете увеличить время схватывания или потерять определенный процент крепости из-за образования газов.
При недостаточном количестве присадки в растворе, он может замерзнуть. Но если заложить чрезмерно много добавки, то вы рискуете увеличить время схватывания или потерять определенный процент крепости из-за образования газов.
Вывод
В качестве вывода хочется отметить, когда вы решаете что добавить в бетон при минусовой температуре, не забывайте о том, что в этой сфере производства контрафактная продукция, к сожалению еще не исчезла с прилавков. Заложив неизвестно что в фундамент зимой, вы рискуете переделывать всю работу летом, тем более что цена на настоящие, качественные составы вполне доступная.
Утепление фундамента зимой.
Добавить в избранное Версия для печати
Поделитесь:
Статьи по теме
Все материалы по теме
Противоморозные добавки в бетон, против застывания воды
Задать вопрос
Наши специалисты ответят на любой интересующий вопрос по услуге
При строительстве зачастую используют бетон, и порой строительство проходит при низких температурах, а поэтому целесообразно сделать так, чтобы вода под цементный раствор не замерзала. Для этого существуют различные противоморозные добавки.
Для этого существуют различные противоморозные добавки.
Основой для противоморозных добавок являются два вещества (так как они используются наиболее чаще) – нитрит натрия и формиат.
Итак, первая добавка – формиат. Данное вещество представляет собой кристаллический порошок. При добавлении формиата в воду точка замерзания воды будет снижена. Кроме того, добавление формиата в бетон имеет свои положительные стороны: прочность бетона будет на порядок выше, сам бетон «прослужит» дольше, добавлять формиат можно при температуре до –15 градусов. Если сравнивать формиат с аналогичными ему веществами, то он имеет ряд преимуществ:
- Формиат не взрывоопасен, не воспламеняется.
- При соединении с водой или воздухом формиат не выделяет токсинов.
- В бетонную смесь количество добавляемого формиата натрия как сухого вещества гораздо меньше в сравнении с его аналогами.
Несмотря на то, что формиат натрия «безвреден», всё же определённые правила безопасности имеются. Во-первых, на руках должны быть перчатки, на лице маска и одет строительный халат. Во-вторых, несмотря не негорючесть вещества, не рекомендуется, чтобы формиат натрия находился вблизи открытого огня. В-третьих, использование формиата является не допустимым для бетонных конструкций, которые в последствие будут эксплуатироваться в водной или газовой среде, или влажность воздуха будет повышенной – свыше 60%. Такая я же ситуации обстоит для предприятий, которые используют постоянный ток или электрифицированный транспорт.
Во-первых, на руках должны быть перчатки, на лице маска и одет строительный халат. Во-вторых, несмотря не негорючесть вещества, не рекомендуется, чтобы формиат натрия находился вблизи открытого огня. В-третьих, использование формиата является не допустимым для бетонных конструкций, которые в последствие будут эксплуатироваться в водной или газовой среде, или влажность воздуха будет повышенной – свыше 60%. Такая я же ситуации обстоит для предприятий, которые используют постоянный ток или электрифицированный транспорт.
Вторая добавка, которая также используется довольно часто – нитрит натрия. Сам по себе нитрит натрия является токсичным противоморозным компонентом. Кроме того нитрит натрия взрывоопасен и предрасположен к горению. Приготовление смеси проводится в специально отведенном помещении. Категорически запрещено, чтобы смесь готовилась там, где могут находиться люди или имеется источник открытого пламени.
Несмотря на то, что данное вещество довольно опасно и токсично, его применение обуславливается рядом следующих преимуществ:
- Бетон становится водонепроницаемым и прочным.

- Снижается коррозия металла, уменьшается пылеобразование.
- Значительная морозостойкость – допускается проводить строительство при достаточно низких температурах (до –20 градусов).
В зависимости от того, каков эффект требуется от противоморозной добавки, выбирается тот или иной вид указанных добавок.
Поделиться ссылкой:
Вернуться к списку
неорганическая химия — Всегда ли замораживание раствора водой приводит к тому, что вода отделяется и образует ледяную решетку?
спросил
Изменено 2 месяца назад
Просмотрено 5к раз
$\begingroup$
Мне любопытно, я пытался изучить эффект замораживания раствора с водой, даже если раствор полностью смешивается. Я наткнулся на что-то, в котором это подробно описывалось в отношении соленой воды, и в основном говорилось, что когда она становится достаточно низкой, чтобы замерзнуть, вода образует контрольную решетку, в основном выталкивая соли, поэтому сам лед представляет собой чистую воду и менее плотный (значительно менее плотный, потому что раствор соли позволял увеличивать плотность вплоть до пониженной температуры замерзания).
Я наткнулся на что-то, в котором это подробно описывалось в отношении соленой воды, и в основном говорилось, что когда она становится достаточно низкой, чтобы замерзнуть, вода образует контрольную решетку, в основном выталкивая соли, поэтому сам лед представляет собой чистую воду и менее плотный (значительно менее плотный, потому что раствор соли позволял увеличивать плотность вплоть до пониженной температуры замерзания).
Мне любопытно, является ли это общим фактом поведения любого раствора с водой независимо от смешиваемости? Существуют ли водные растворы, которые разрушают решетку, но при этом допускают замерзание, или блокирование образования этой решетки полностью блокирует замерзание раствора, несмотря ни на что? Существуют ли водные растворы, которые замерзают даже с решеткой, не отделяя неводные соединения?
Примечание: я понимаю, что аморфный лед можно создать с помощью волшебства, но мой вопрос больше касается типичного поведения на Земле.
- неорганическая химия
- вода
- растворы
$\endgroup$
4
$\begingroup$
Очистка, происходящая при замораживании водного раствора, называется фракционной заморозкой и основана на идее, что примеси растворителя (а это может быть любой растворитель, а не только вода) имеют значительно меньшую растворимость в твердой фазе растворителя относительно жидкой фазы. Здесь можно найти несколько методов фракционного замораживания в целях очистки. По мере образования твердого вещества примеси вытесняются в жидкость, которая еще не затвердела. Затем очищенные кристаллы можно удалить физическими методами (например, фильтрацией). В случае воды, где лед менее плотный, чем жидкая фаза, очищенные кристаллы всплывают на поверхность насыщенной примесями жидкости. Вероятно, поэтому некоторые люди наблюдали слой примесей глубоко внутри глыбы льда. Как упоминалось выше, процесс не ограничивается только водой, а кристаллизация замораживанием используется для устранения чистоты кремниевых пластин и уже много лет известна как способ получения крепких напитков. Это последнее использование частичного замораживания близко к вопросу OP, который касается смешивающихся веществ (в данном случае этанола и воды). Несмотря на их смешиваемость, этанол и воду можно разделить фракционным замораживанием так же, как их можно разделить фракционной перегонкой. Некоторые вещества нельзя полностью разделить перегонкой, и эти вещества называются азеотропами.
Здесь можно найти несколько методов фракционного замораживания в целях очистки. По мере образования твердого вещества примеси вытесняются в жидкость, которая еще не затвердела. Затем очищенные кристаллы можно удалить физическими методами (например, фильтрацией). В случае воды, где лед менее плотный, чем жидкая фаза, очищенные кристаллы всплывают на поверхность насыщенной примесями жидкости. Вероятно, поэтому некоторые люди наблюдали слой примесей глубоко внутри глыбы льда. Как упоминалось выше, процесс не ограничивается только водой, а кристаллизация замораживанием используется для устранения чистоты кремниевых пластин и уже много лет известна как способ получения крепких напитков. Это последнее использование частичного замораживания близко к вопросу OP, который касается смешивающихся веществ (в данном случае этанола и воды). Несмотря на их смешиваемость, этанол и воду можно разделить фракционным замораживанием так же, как их можно разделить фракционной перегонкой. Некоторые вещества нельзя полностью разделить перегонкой, и эти вещества называются азеотропами. Вода и этанол образуют азеотропную смесь приблизительно 95% воды. (Таким образом, самогон, который вы думали сделать, используя приведенную выше ссылку, будет ограничен крепостью 190.) Что мне кажется интересным, так это следующая цифра,
Вода и этанол образуют азеотропную смесь приблизительно 95% воды. (Таким образом, самогон, который вы думали сделать, используя приведенную выше ссылку, будет ограничен крепостью 190.) Что мне кажется интересным, так это следующая цифра,
, которая показывает точку замерзания смесей вода/этанол в зависимости от содержания этанола. . В точке около 95% наблюдается значительное падение температуры замерзания. В этот момент, называемый точкой эвтектики, раствор ведет себя так, как будто он представляет собой один компонент (во многом как азеотроп), и вряд ли его можно будет разделить с помощью «простых» средств фракционного замораживания. Примечание. Я использую термин «простой», потому что азеотропы можно разделить с помощью специальных методов дистилляции.
Итак, в заключение: фракционное замораживание будет работать с любым водным раствором, независимо от смешиваемости компонентов, если соотношение компонентов не близко к эвтектической точке. Нам не нужно ограничиваться водными растворами, так как многие виды могут быть очищены таким образом. Механизм очистки зависит не столько от кристаллической решетки, сколько от относительной растворимости растворенного вещества в твердой и жидкой фазах растворителя. Наконец, многие водные растворы замерзают даже с примесями. Этот и другие типы разделения работают на равновесных процессах, и для «полного» удаления примесей необходимо несколько итераций. (или, правильнее, удалить примеси до уровня, приемлемого для вашего применения.)
Механизм очистки зависит не столько от кристаллической решетки, сколько от относительной растворимости растворенного вещества в твердой и жидкой фазах растворителя. Наконец, многие водные растворы замерзают даже с примесями. Этот и другие типы разделения работают на равновесных процессах, и для «полного» удаления примесей необходимо несколько итераций. (или, правильнее, удалить примеси до уровня, приемлемого для вашего применения.)
$\endgroup$
4
$\begingroup$
Ситуация, которую вы описываете, известна как эвтектическая система. Находится ли система в точке эвтектики, зависит как от материалов, составляющих раствор, так и от относительных количеств каждого из них. Растворы $\bf{A}$ и $\bf{B}$, не имеющие эвтектического состава, будут вымораживать один компонент до тех пор, пока не будет достигнут эвтектический состав. В то время как эвтектическая система затвердевает одновременно с обоими компонентами, многие системы замерзают в твердом состоянии $\bf{A}$ и в твердом состоянии $\bf{B}$ (оба взаимно диспергированы), а не в твердом состоянии $\bf{AB}$, хотя некоторые системы затвердевают как смешанные (металлические сплавы, например).
В то время как эвтектическая система затвердевает одновременно с обоими компонентами, многие системы замерзают в твердом состоянии $\bf{A}$ и в твердом состоянии $\bf{B}$ (оба взаимно диспергированы), а не в твердом состоянии $\bf{AB}$, хотя некоторые системы затвердевают как смешанные (металлические сплавы, например).
Вода и хлорид натрия образуют эвтектику при содержании около 23% $\ce{NaCl}$ по весу. Вы можете увидеть фазовую диаграмму для воды и $\ce{NaCl}$ на этой странице Университета Калгари. Обратите внимание, что эвтектика может состоять более чем из двух компонентов, как указано на странице Университета Калгари. Типичная фазовая диаграмма раствора $\ce{NaCl/h3O}$ показана ниже:
Примечание: Эвтектический состав составляет около 27% $\ce{NaCl}$ (по $w/v$) растворяется в воде (имейте в виду, что насыщенный раствор $\ce{NaCl}$ составляет около 30% при комнатной температуре).
$\endgroup$
5
$\begingroup$
Некоторые растворенные вещества, особенно под давлением, фактически включаются в структуру водяного льда с образованием клатратных гидратов . Из них наиболее известен гидрат метана, встречающийся в природе в океанах, где организмы вырабатывают метан под достаточным давлением для создания клатратной фазы. Эти иллюстрации из источника, указанного выше, показывают условия глубины и температуры океана, при которых образуются гидраты клатрата метана, и получающуюся в результате клатратную структуру.
Из них наиболее известен гидрат метана, встречающийся в природе в океанах, где организмы вырабатывают метан под достаточным давлением для создания клатратной фазы. Эти иллюстрации из источника, указанного выше, показывают условия глубины и температуры океана, при которых образуются гидраты клатрата метана, и получающуюся в результате клатратную структуру.
В клатратной фазе молекулы воды упакованы иначе, чем чистый водяной лед. В то время как структура обычного льда имеет много открытого пространства, требуется еще больше места для включения метана или других небольших молекул газа, и поэтому молекулы воды упакованы менее плотно, чтобы оставить отверстия для инородного материала.
$\endgroup$
Зарегистрируйтесь или войдите в систему
Зарегистрируйтесь с помощью Google
Зарегистрироваться через Facebook
Зарегистрируйтесь, используя электронную почту и пароль
Опубликовать как гость
Электронная почта
Требуется, но никогда не отображается
Опубликовать как гость
Электронная почта
Требуется, но не отображается
Нажимая «Опубликовать свой ответ», вы соглашаетесь с нашими условиями обслуживания, политикой конфиденциальности и политикой использования файлов cookie
.
Точка замерзания воды по сравнению с раствором соли
Обновлено 24 февраля 2020 г.
Автор: Riti Gupta
Когда растворитель замерзает, частицы этого растворителя становятся более упорядоченными. Межмолекулярные силы, действующие на эти частицы, становятся более «постоянными», так как частицы теперь находятся ближе друг к другу. Например, когда вода замерзает в лед, водородные связи, которые придают воде многие из ее уникальных свойств, образуют сеть молекул шестиугольной формы, присущую структуре льда.
Так что же происходит, когда растворенное вещество добавляется в воду или чистый растворитель? Добавление растворенного вещества приводит к нарушению упорядоченности молекул растворителя. Это означает, что для замораживания раствора необходимо удалить больше энергии.
Например, когда в воду добавляют соль, образующиеся в воде ионы разрушают обычную сеть водородных связей, образующихся при замерзании. В результате температура замерзания раствора ниже, чем у чистого растворителя. Это называется депрессией точки замерзания.
В результате температура замерзания раствора ниже, чем у чистого растворителя. Это называется депрессией точки замерзания.
Определение депрессии точки замерзания
Снижение точки замерзания прямо пропорционально моляльности растворенного вещества:
В этом уравнении K f — это молярная константа депрессии точки замерзания, а m — моляльность растворенного вещества. Помните, что моляльность — это количество молей растворенного вещества на кг растворителя. Коэффициент Вант-Гоффа равен i, который относится к количеству ионов в растворе на каждую растворенную молекулу растворенного вещества. Например, это будет 2 для NaCl.
По сути, это означает, что чем больше растворенного вещества, тем сильнее снижается температура замерзания.
Депрессия точки замерзания определяется как точка замерзания чистого растворителя минус точка замерзания рассматриваемого раствора:
Это позволяет вам определить новую точку замерзания по сравнению с чистым растворителем.
Чем полезна депрессия точки замерзания?
Двумя наиболее распространенными случаями понижения точки замерзания в реальном мире являются антифриз и засолка дорог зимой.
Этиленгликоль представляет собой соединение, часто используемое в антифризах, поскольку при добавлении его в воду температура замерзания воды снижается. Это может помочь гарантировать, что вода в радиаторе вашего автомобиля не замерзнет.
Когда зимой на дорогу добавляют соль, лед будет таять при более низкой температуре, что сделает ее более безопасной, поскольку на дороге не будет столько льда.
Взгляните на следующий пример, который показывает, как добавление соли в воду приводит к снижению точки замерзания раствора.
Какова температура замерзания раствора, в котором 100 г NaCl добавлены к 1 кг воды? Другими словами, какова температура замерзания соленой воды?
Вы можете использовать следующее уравнение:
K f для воды составляет 1,86 °C/м.





 Кустарные мастера «авторитетно» заявляют о том, что такие добавки вызывают повышенную коррозию арматурного каркаса.
Кустарные мастера «авторитетно» заявляют о том, что такие добавки вызывают повышенную коррозию арматурного каркаса. При недостаточном количестве присадки в растворе, он может замерзнуть. Но если заложить чрезмерно много добавки, то вы рискуете увеличить время схватывания или потерять определенный процент крепости из-за образования газов.
При недостаточном количестве присадки в растворе, он может замерзнуть. Но если заложить чрезмерно много добавки, то вы рискуете увеличить время схватывания или потерять определенный процент крепости из-за образования газов.